Introducción
Los divertículos esofágicos torácicos son raros, siendo observados en menos del 1% de los estudios del tracto gastrointestinal superior, y en menos del 3% de los pacientes que presentan disfagia [1]. Aproximadamente el 30% de los divertículos esofágicos son hallados en el esófago intratorácico [2].
Pueden ocurrir dos tipos de divertículos: de tracción y de pulsión.
Los divertículos de tracción son divertículos verdaderos, relacionados a menudo con procesos inflamatorios mediastinales.
Los divertículos de pulsión son divertículos falsos ocasionados por una presión intraluminal aumentada, que conduce a la herniación de la mucosa y submucosa a través de un área focalizada de la pared muscular esofágica [3].
Se cree que ese aumento de la presión intraluminal es causado por una obstrucción funcional originada en un desorden de la motilidad o por obstrucción mecánica distal [3,4]. Los desórdenes de la motilidad esofágica han sido identificados en la mayoría de los pacientes con divertículos medio esofágicos o epifrénicos que han sido sometidos a evaluación de la función esofágica [5,6]. En la población occidental, los divertículos esofágicos torácicos son más frecuentemente divertículos por pulsión [1,5].
Una revisión de la literatura, que consiste sólo en reportes de casos, series pequeñas y opiniones de expertos, muestra un escaso consenso en relación con la etiología y el manejo de los divertículos esofágicos torácicos. Cuando existe acuerdo en relación con los aspectos del tratamiento, esas conclusiones están a menudo basadas en datos limitados [7]. Los temas específicos de controversia relacionados con el manejo incluyen: indicación para la operación, procedimientos realizados y abordaje quirúrgico óptimo (transtorácico vs transabdominal, abierto vs mínimamente invasivo).
El objetivo de este estudio fue revisar la experiencia de 15 años de los autores con el tratamiento del divertículo esofágico torácico utilizando cirugía mínimamente invasiva (CMI). El objetivo primario del estudio fue evaluar los resultados perioperatorios después de la cirugía. Este estudio es una actualización de otro ya publicado de la experiencia temprana con la CMI para el divertículo esofágico torácico [8]. Los procedimientos quirúrgicos mínimamente invasivos tienen una curva de aprendizaje del operador significativa; por lo tanto, los autores creen que fue importante revisar este tema y examinar sus resultados actuales.
Material y métodos
Se revisaron retrospectivamente los resultados del tratamiento mínimamente invasivo de pacientes con divertículos esofágicos torácicos tratados en el University of Pittsburgh Medical Center, durante un período de 15 años, desde 1997 hasta 2012. Este estudio fue aprobado por el comité de revisión institucional. Dado que fue un estudio retrospectivo, se dispensó el consentimiento individual de los pacientes.
Evaluación preoperatoria e investigaciones
Los pacientes que eran candidatos para la cirugía fueron sometidos a una historia completa y examen físico. Las investigaciones realizadas incluyeron esofagograma con bario, esofagogastroduodenoscopía, manometría esofágica y estudio nuclear del tránsito esofágico. Se identificaron los desórdenes funcionales del esófago. Menos comúnmente se obtuvieron pruebas adicionales (por ejemplo, vaciamiento gástrico, monitoreo de pH de 24 horas).
Abordaje quirúrgico
La técnica de la operación ha sido detallada previamente [8,9]. En resumen, se efectúa una endoscopía flexible en la sala de operaciones para confirmar la localización del divertículo y evaluar cualquier anormalidad patológica esofágica (Fig. 1). Los autores favorecen la cirugía toracoscópica videoasistida (CTVA) desde el lado derecho, lo que permite una exposición adecuada de los divertículos tanto del lado derecho como del izquierdo. Independientemente del abordaje (CTVA, laparoscopía o combinado) los principios básicos del procedimiento permanecen constantes. El esófago es movilizado y se identifica el divertículo.
El divertículo es disecado meticulosamente lejos de la pleura y de las fibras musculares adherentes, con tijeras ultrasónicas hacia su cuello, evitando la perforación dentro de la luz (Fig. 2). Se debe exponer todo el cuello diverticular para evitar dejar un divertículo residual, lo que es facilitado realizando una miotomía proximal y distal en donde protruyen la mucosa y submucosa a través de la pared muscular. Después de colocar una bujía de 48F a 54F para evitar el estrechamiento de la luz, se usa una engrampadora endo-GIA (Covidien, Dublín, Irlanda) para seccionar el cuello del divertículo (Fig. 3).
El músculo y la pleura suprayacentes son luego reaproximados sobre la línea de engrampado. Cuando está indicada, puede realizarse una miotomía del lado contralateral o ipsilateral (Fig. 4). La miotomía se extiende típicamente proximal al cuello del divertículo, mientras que la extensión distal se basa en los hallazgos preoperatorios e intraoperatorios.
Si se requiere, la miotomía se extiende a través del esfínter esofágico inferior (EEI) y en el estómago. Luego se efectúa una fundoplicatura parcial, cuando está indicado un procedimiento antirreflujo. Se deja un drenaje aspirativo cerrado adyacente a la línea de engrampado, paralelo al esófago. Cuando se emplea un abordaje con CTVA, también se coloca un tubo torácico.
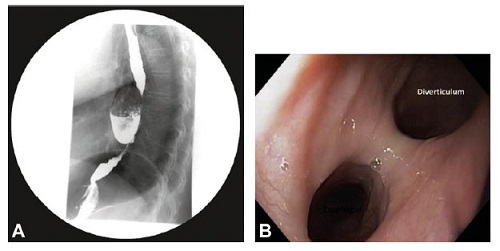
• FIGURA 1: (A) esofagograma con bario de un divertículo epifrénico. (B) Visión endoscópica de un divertículo epifrénico. El divertículo está en el ángulo superior derecho.

• FIGURA 2: Exposición de la base de un divertículo epifrénico.
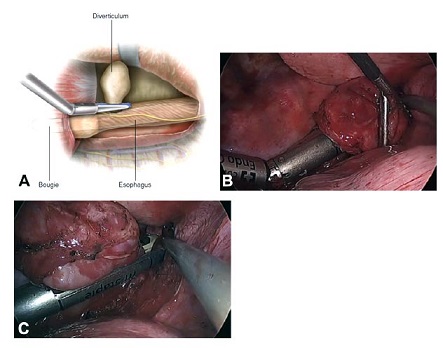
• FIGURA 3: (A) una bujía es colocada en el esófago y se usa una engrampadora endoscópica para resecar el divertículo. (B) La engrampadora es posicionada sobre el cuello del divertículo. (C) La resección del divertículo es realizada con la engrampadora.
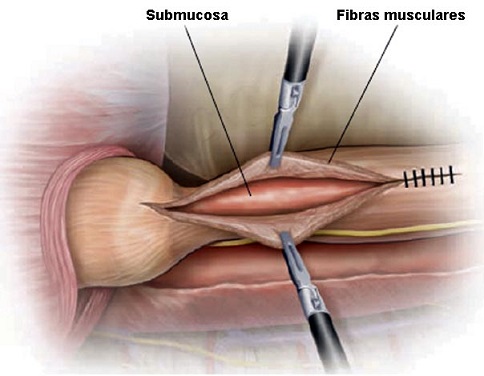
• FIGURA 4: Se realiza una miotomía con tijeras ultrasónicas o con gancho.
Seguimiento postoperatorio
Los pacientes fueron observados en la clínica para evaluar los síntomas y los puntajes de disfagia (escala: 1, sin disfagia; 2, disfagia para sólidos duros; 3, disfagia para sólidos blandos; 4, disfagia para líquidos; 5, disfagia para la saliva). El Gastroesophageal Reflux Disease-Health Related Quality of Life (GERD-HRQOL) fue administrado a un subgrupo de pacientes. Los autores clasifican los puntajes del GERD-HRQOL desde 0 a 9 como excelentes [11].
Análisis estadístico
Los datos de las variables preoperatorias, incluyendo síntomas, intervención quirúrgica y resultados postoperatorios, fueron recolectados. El objetivo final primario fue la mortalidad a 30 días. Las variables de resultado evaluadas incluyeron: resultados perioperatorios, puntaje de disfagia y calidad de vida después de la cirugía. Se realizó la comparación de los puntajes preoperatorios y postoperatorios de la disfagia usando la prueba de los rangos con signo.
Resultados
Características de los pacientes
Cincuenta y siete pacientes fueron sometidos a CMI por divertículos sintomáticos. Hubo 33 mujeres y 24 hombres, con una mediana para la edad de 71 años (rango: 26 a 96 años). La mayoría de los pacientes tenía divertículos epifrénicos (50 de 57 pacientes); 88%).
El síntoma presente más común fue la disfagia. El estudio preoperatorio incluyó un esofagograma con bario y una endoscopía alta en todos los pacientes (100%); la manometría se intentó en 42 pacientes, pero no pudo completarse por razones técnicas en 7. Se obtuvo un estudio nuclear del tránsito esofágico en 1 paciente. Los desórdenes funcionales del esófago, aislados o en combinación con obstrucción mecánica distal, fueron identificados en 49 pacientes (86%).
Abordajes y procedimientos quirúrgicos
Se usó un abordaje de CTVA en la mayoría de los pacientes (68%; 39 de 57 pacientes), ya sea aislada o en combinación con laparoscopía. Los autores fueron aumentando el uso de la CTVA durante la última década. Tres pacientes (5%) requirieron una conversión abierta.
Un caso laparoscópico requirió conversión a una toracotomía izquierda debido a densas adherencias rodeando al divertículo; una toracotomía izquierda fue requerida en un paciente con síndrome de Scimitar abordado inicialmente mediante CTVA, y se necesitó una laparotomía para revisión de una fundoplicatura previa en un paciente abordado inicialmente con una combinación de CTVA y laparoscopía.
El procedimiento más comúnmente realizado fue la diverticulectomía con miotomía (47 de 57 pacientes; 82%). Se efectuó una fundoplicatura parcial en 20 pacientes (35%). La diverticulectomía sin miotomía y revisión de una fundoplicatura de Nissen previa fue realizada en 4 pacientes (7%). En 1 de los pacientes, la fundoplicatura de Nissen fue convertida en una fundoplicatura de Dor, y los otros 3, que tenían obstruido el esófago, fueron convertidos a un Nissen flojo.
Resultados perioperatorios
La mediana de la duración de la estadía hospitalaria fue de 5 días. La mortalidad perioperatoria a 30 días fue del 0%. La mortalidad intrahospitalaria (1 paciente) fue del 1,75%. Cuatro pacientes (7%) experimentaron una filtración que requirió reoperación. Dos pacientes (3,5%) tuvieron filtraciones que fueron manejadas con drenajes.
Mejora de los síntomas
Los pacientes fueron seguidos en la clínica (media, 20,8 meses). Durante el seguimiento alejado mejoraron significativamente los puntajes de disfagia (p < 0,001). Los resultados de la calidad de vida estuvieron disponibles en un subgrupo de pacientes. Durante el seguimiento alejado, la mediana del puntaje GERD-HRQOL fue 5, lo que calificó como excelente, indicando una GERD-HRQOL preservada en la mayoría de los pacientes.
Comentarios
En esta serie, la más grande hasta la actualidad, enfocada sobre el tratamiento quirúrgico de los divertículos esofágicos torácicos, los autores han demostrado que el abordaje mediante CMI es seguro y efectivo durante el seguimiento alejado a mediano plazo. La morbilidad pareció aceptable y la mortalidad fue baja.
Existen varias controversias en el manejo de los divertículos esofágicos, incluyendo las indicaciones para la cirugía. Aunque la mayoría de los cirujanos concuerda en que la intervención quirúrgica está indicada para los pacientes sintomáticos [12-16], el manejo de los pacientes que presentan síntomas mínimos o ningún síntoma sigue siendo algo polémico.
Altorki y col. [16], apoyan fuertemente la intervención quirúrgica en todos los pacientes después de notar aspiración en 9 de 20 pacientes, 3 de los cuales experimentaron complicaciones con riesgo de vida. El abordaje actual de los autores del presente estudio es ofrecer la cirugía a todos los pacientes sintomáticos.
También consideran la cirugía en los pacientes asintomáticos con divertículos grandes y asociados con disfunción motora, que son considerados como buenos candidatos quirúrgicos (bajo riesgo). Todos los pacientes, en la presente serie, eran sintomáticos. Los pacientes verdaderamente asintomáticos, con mínimas quejas y divertículos pequeños, son observados de cerca por el desarrollo de síntomas, particularmente aquellos que son considerados como pacientes quirúrgicos de alto riesgo.
Existe una significativa variación en los procedimientos realizados para tratar los divertículos esofágicos torácicos. La miotomía es realizada típicamente en los pacientes en los que no se reseca un divertículo pequeño, dado que la bolsa típicamente retrocede si la causa del incremento de la presión intraluminal es aliviada [3,17].
La diverticulopexia [16,18-20] y la imbricación del divertículo [21], también han sido reportadas. Todos los pacientes en la presente serie fueron sometidos a diverticulectomía. Durante la diverticulectomía, es crítico que el cuello del divertículo esté completamente expuesto para identificar claramente la línea de transección.
Aunque el fracaso en lograrlo puede no afectar los resultados a corto plazo, los autores creen que un divertículo residual puede agrandarse con el tiempo y causar síntomas recurrentes. Rutinariamente pasan una bujía de 48F a 54F antes de aplicar la engrampadora al cuello del divertículo, para prevenir un estrechamiento intraluminal inadvertido.
La colocación de una bujía es también de ayuda para estabilizar la luz del esófago y puede ayudar para delinear el plano entre la mucosa y las capas de la pared muscular. Rutinariamente cubren la línea de engrampado con la reaproximación del músculo o la pleura sobre el sitio de la diverticulectomía, dado que han notado una tasa más alta de filtración en la línea de engrampado cuando ese paso era omitido en su serie más temprana [8].
Otro punto importante de discusión en la literatura es el uso de la miotomía de rutina versus selectiva. Existe una significativa variación en las tasas reportadas de desórdenes motores esofágicos identificables en esa población de pacientes, yendo desde el 45% al 100% [1,12-16,20,22-25]. Eso puede estar en parte relacionado con la naturaleza intermitente sospechada de algunos desórdenes motores, y el éxito técnico variable para pasar la sonda manométrica [7,18,19].
La obstrucción mecánica (esto es, estenosis, fundoplicatura ajustada), sola o en combinación con la obstrucción funcional, también puede conducir al incremento de la presión intraluminal y la subsiguiente formación del divertículo [7,23,24,26]. Se identificó un desorden funcional o una obstrucción mecánica en la mayoría de los pacientes.
Como señaló Belsey [3] hace casi medio siglo, debe abordarse la causa subyacente que conduce al estallido, si se espera una cirugía exitosa. Esa enseñanza, en combinación con un reporte previo de una alta tasa de filtración sin la inclusión de una miotomía [27], han llevado a muchos cirujanos a favorecer la realización de una miotomía independientemente de si es identificado o no un desorden motor [3,14,18-20,24,28]. En contraste, otros investigadores favorecen un abordaje más selectivo, realizando una miotomía sólo cuando es claramente identificado un desorden motor preoperatoriamente [12,13,21].
La extensión distal de la miotomía sigue siendo también controvertida. Algunos creen que una miotomía larga con extensión en el estómago (cardiomiotomía) es importante para un alivio completo de la obstrucción distal, independientemente de si se identifica o no un desorden motor subyacente [3,16,18,19,28]. No obstante, otros favorecen una miotomía más a la medida, basando la extensión distal en los resultados de la manometría preoperatoria [12,13].
Existen datos insuficientes para determinar cuál miotomía es superior. Los autores de este trabajo usaron los hallazgos en la esofagoscopia, esofagograma y manometría, para caracterizar las anormalidades de la motilidad, y esas investigaciones influenciaron el manejo. Por ejemplo, hallazgos sugestivos de acalasia impulsarían un abordaje laparoscópico con una miotomía distal extendiéndose más allá de la unión gastroesofágica y la construcción de una fundoplicatura parcial; la adición de CTVA puede ser considerada luego para la resección de un gran divertículo.
En pacientes con una manometría normal y esofagoscopia que no muestra evidencia de obstrucción distal, se efectúa sólo la diverticulectomía, al igual que en los casos de divertículo por tracción. En casos con evidencia convincente de motilidad y función del EEI normales, sólo con una obstrucción mecánica (esto es, una hernia hiatal obstructiva o una fundoplicatura previa), puede llevarse a cabo la diverticulectomía y el alivio de la obstrucción distal sin miotomía.
Otro tópico debatido es si la fundoplicatura debe ser o no incluida en el tratamiento quirúrgico. Thomas y col. [1] no notaron diferencia en la tasa de filtración después de la miotomía con o sin fundoplicatura (7% vs 8%), pero reportaron una tasa más alta de acidez postoperatoria cuando no se realizó la fundoplicatura (16% vs 9%).
En una serie más reciente de Rossetti y col. [29], se reportó una tasa de filtración del 24% después de la diverticulectomía, miotomía y fundoplicatura completa. Coincidiendo con las enseñanzas de Belsey [3] y las tasas altas reportadas de reflujo postoperatorio en los pacientes con acalasia que fueron sometidos a miotomía sin fundoplicaura, se recomienda típicamente una fundoplicatura parcial cuando se realiza la misma [30]. Los autores del presente trabajo favorecen en la actualidad un abordaje selectivo en relación con la fundoplicatura.
Cuando la realizan, favorecen una fundoplicatura parcial. La elección de la fundoplicatura (Dor, Toupet) depende del cirujano. Una fundoplicatura parcial es típicamente efectuada en pacientes con acalasia o quejas preoperatorias de reflujo, y en aquellos que son abordados laparoscópicamente, dado que la disección hiatal altera la función del EEI.
En algunos pacientes con una fundoplicatura muy ajustada, han optado por realizar una fundoplicatura floja de Nissen, que no es obstructiva. La fundoplicatura no es efectuada típicamente en pacientes abordados mediante CTVA cuando la miotomía no es realizada a través del EEI, que en la experiencia de los autores preserva un funcionamiento normal del EEI y, por lo tanto, previene la necesidad de una fundoplicatura. Cuando es necesario que la miotomía se extiende a través del EEI desde un abordaje por CTVA derecha, se puede añadir un abordaje laparoscópico selectivo para completar la miotomía distal, si es necesario, y realizar una fundoplicatura parcial.
Debe señalarse que la comparaciones directas entre los abordajes mínimamente invasivo y abierto son difíciles, debido a las diferentes poblaciones de pacientes y a la naturaleza retrospectiva de la mayoría de los estudios. Las ventajas de la CMI para las operaciones torácicas mayores han sido ampliamente reportadas [35-37].
Las tasas de morbilidad para los pacientes tratados quirúrgicamente van desde el 6% al 33% en las series abiertas, con tasas de filtración tan altas como el 18% [12-14,16,18-20,22,28]. Las tasas de morbilidad son similares con los abordajes por CMI, yendo desde el 7% al 29%, con tasas de filtración tan altas como el 24% en algunas series pequeñas [4,21,23,26,29,31-34].
Aunque las tasas de morbilidad y de filtración fueron comparables, se reportaron estadías hospitalarias más cortas y menor mortalidad a 30 días en las series con CMI. Los resultados de los autores durante los últimos 15 años demuestran la significativa curva de aprendizaje asociada con el abordaje de CMI. Sin embargo, con experiencia, fueron vistas mejoras en la morbilidad global, tasa de filtración y mortalidad en sus últimos 37 pacientes, cuando se las compara con su serie anterior de 20 pacientes [8]. Los autores continúan favoreciendo el abordaje de CMI dadas las ventajas bien documentadas vistas en otras operaciones intestinales y esofágicas.
Tradicionalmente, los pacientes eran abordados por una toracotomía derecha para el manejo de los divertículos en el esófago medio, y por una toracotomía izquierda para los divertículos distales [12-14,16,18-20,22,28]. Interesantemente, los cirujanos se mudaron lejos de esos abordajes transtorácicos hacia el abordaje laparoscópico con la introducción de las técnicas de CMI. Eso puede ser en parte atribuible al éxito de la miotomía laparoscópica para el tratamiento de la acalasia. No obstante, en contraste con la laparoscopía, la CTVA brinda una mejor visualización y una disección más fácil para los divertículos proximales epifrénicos y del esófago medio, particularmente para la disección del cuello del divertículo, divertículos grandes y divertículos rodeados por significativa inflamación.
La CTVA brinda también una extensión proximal más fácil de la miotomía y es útil para las reoperaciones después de procedimientos laparoscópicos fallidos. La desventaja primaria de la CTVA es la dificultad para realizar la reparación de una hernia hiatal concomitante o una fundoplicatura. Las mismas se efectúan más fácilmente laparoscópicamente. Una combinación del CTVA y abordaje laparoscópico puede ser el abordaje ideal cuando es necesaria una fundoplicatura.
La elección del abordaje y de los procedimientos realizados se determina mejor después de un estudio completo, con el conocimiento de la causa subyacente, funcional o mecánica, identificada o sospechada, del divertículo, la consideración de los hallazgos intraoperatorios, y los antecedentes de operaciones previas del paciente.
Fortalezas y limitaciones
Una de las fortalezas de este estudio es que es el más grande, hasta la actualidad, investigando el tratamiento quirúrgico de los divertículos esofágicos torácicos. Además, todos los pacientes fueron abordados de una manera mínimamente invasiva. Este estudio tiene varias limitaciones, que son las típicas de los estudios retrospectivos, tales como el sesgo en la selección. Además, se requirió de un largo seguimiento alejado para evaluar completamente la durabilidad del alivio de los síntomas y la mejora en la calidad de vida.
Conclusiones
En esta serie, la más grande hasta el presente reportando el tratamiento quirúrgico de los divertículos esofágicos torácicos, la CMI es segura y efectiva durante el seguimiento alejado de término intermedio. Se requiere un seguimiento adicional para evaluar la durabilidad de esos resultados. Un abordaje mínimamente invasivo para el manejo de los divertículos esofágicos torácicos es seguro y efectivo cuando es realizado por cirujanos experimentados en cirugía esofágica abierta y mínimamente invasiva. El abordaje óptimo y los procedimientos efectuados deberían determinarse sobre una base individualizada después de una completa investigación.
Comentario y resumen: Dr. Ricardo Altrudi