| Introducción |
El cáncer de próstata es uno de los cánceres más comunes en hombres a nivel mundial, con una incidencia estimada de 1,4 millones de nuevos casos anuales y aproximadamente 375 000 muertes relacionadas en 2020.
Aunque la mayoría de los casos se diagnostican en etapas tempranas, un subgrupo de pacientes desarrolla cáncer de próstata metastásico resistente a la castración (mCRPC), una forma agresiva de la enfermedad con opciones de tratamiento limitadas.
En los últimos años, los avances en terapias dirigidas, como los inhibidores de PARP (poli ADP-ribosa polimerasa), han transformado el manejo del cáncer de próstata avanzado, especialmente en pacientes con alteraciones en los genes de reparación de recombinación homóloga (HRR).
| Epidemiología del cáncer de próstata |
El cáncer de próstata es la segunda causa de muerte por cáncer en hombres en muchos países occidentales. La incidencia varía geográficamente, siendo más alta en América del Norte y Europa, y más baja en Asia.
Los factores de riesgo incluyen la edad (la mayoría de los casos se diagnostican después de los 65 años), antecedentes familiares y la genética, como las mutaciones en los genes BRCA1 y BRCA2. En pacientes con mCRPC, las alteraciones en los genes HRR, como BRCA2, ATM y CHEK2, están presentes en aproximadamente el 20-25 % de los casos, lo que subraya la importancia de las pruebas genómicas para guiar el tratamiento.
| Inhibidores de PARP en el cáncer de próstata |
Los inhibidores de PARP, como olaparib, rucaparib y talazoparib, han demostrado ser eficaces en el tratamiento del mCRPC con alteraciones en los genes HRR. Estos fármacos actúan bloqueando la reparación del ADN en células cancerosas con deficiencias en la reparación de recombinación homóloga, lo que lleva a la acumulación de daño en el ADN y la muerte celular.
Estudios recientes, como el ensayo TALAPRO-2, han demostrado que la combinación de talazoparib con enzalutamida mejora significativamente la supervivencia libre de progresión en pacientes con mCRPC, independientemente del estado de HRR.
| Estudios recientes y datos clave |
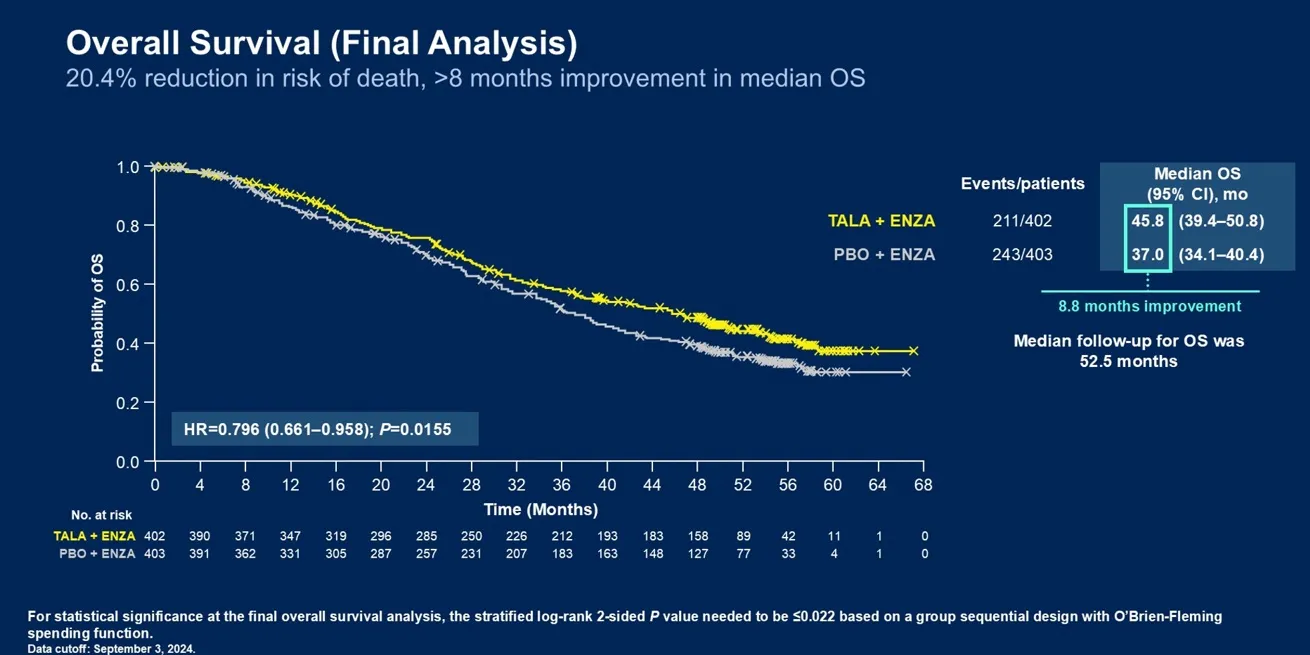
1. TALAPRO-2: Este estudio de fase 3 evaluó la combinación de talazoparib con enzalutamida frente a enzalutamida más placebo en pacientes con mCRPC. Los resultados mostraron una mejora significativa en la supervivencia libre de progresión basada en imágenes (ibPFS) en el grupo de talazoparib, con un HR de 0,63 (IC 95 %: 0,51-0,78; p<0,001). Este beneficio se observó tanto en pacientes con deficiencia en HRR como en aquellos sin deficiencia conocida. Recientemete se ha publicado que el beneficio en supervivencia global es de 45,8 meses vs. 37 meses.
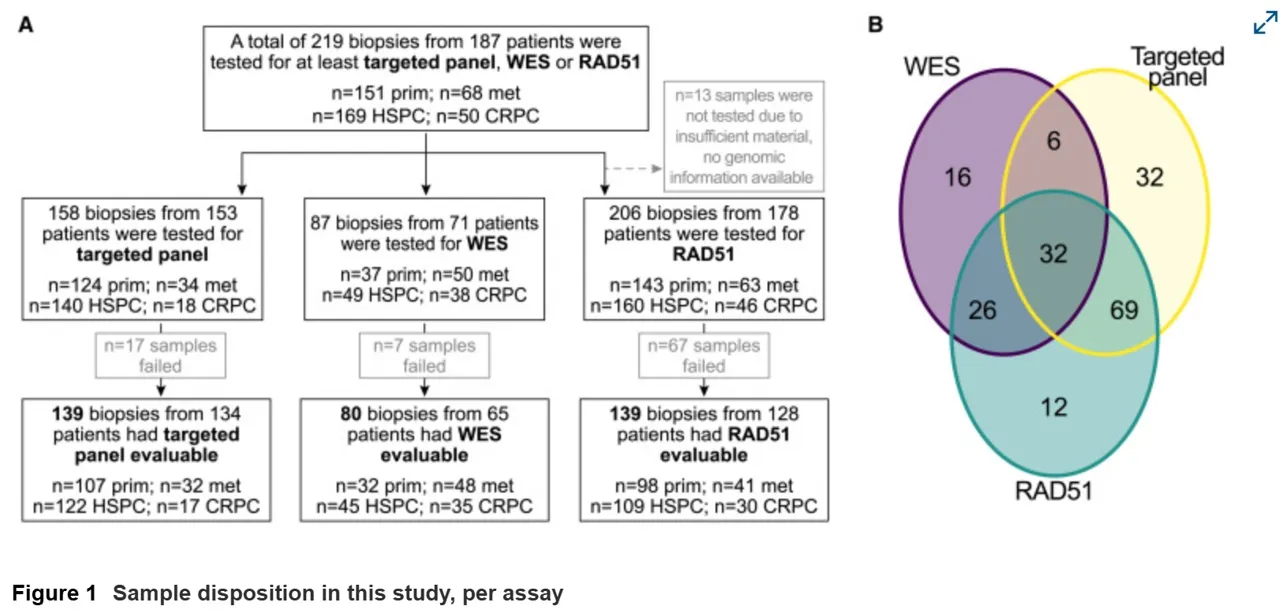
2. RAD51 y HRR: Un estudio publicado en Cell Reports Medicine evaluó el estado de reparación de recombinación homóloga (HRR) en el cáncer de próstata metastásico mediante secuenciación de próxima generación (NGS) y ensayos de inmunofluorescencia para RAD51. Los resultados mostraron que los bajos niveles de RAD51 se asociaron con alteraciones en BRCA1/2 y una mayor sensibilidad a los inhibidores de PARP y quimioterapia basada en platino. Este enfoque funcional complementa las pruebas genómicas y puede ayudar a identificar pacientes que se beneficiarían de terapias dirigidas.
3. Desafíos en el manejo del cáncer de próstata avanzado: A pesar de los avances, persisten desafíos en la adopción de terapias combinadas en la práctica clínica real. Un estudio reciente destacó que solo el 9,3 % al 38,1 % de los pacientes con cáncer de próstata metastásico sensible a la castración (mHSPC) reciben tratamiento intensificado con inhibidores de la vía de los receptores de andrógenos (ARPI) y terapia de privación de andrógenos (ADT). Además, la falta de datos comparativos sobre la secuencia de tratamientos en mCRPC complica la toma de decisiones clínicas.
| Conclusiones |
Los avances en el tratamiento del cáncer de próstata avanzado, particularmente con el uso de inhibidores de PARP, han mejorado significativamente los resultados clínicos. Sin embargo, la adopción de estas terapias en la práctica clínica real sigue siendo subóptima, debido a la falta de pruebas genómicas generalizadas y la ausencia de datos comparativos sobre la secuencia de tratamientos.
La educación continua de los médicos y la implementación de estrategias para mejorar el acceso a las pruebas genómicas son esenciales para maximizar los beneficios de estas terapias innovadoras.
Referencias
- TALAPRO-2: Agarwal, N., Azad, A., Carles, J., Fay, A. P., Matsubara, N., Szczylik, C., ... & Fizazi, K. (2025). Final overall survival (OS) with talazoparib (TALA)+ enzalutamide (ENZA) as first-line treatment in unselected patients with metastatic castration-resistant prostate cancer (mCRPC) in the phase 3 TALAPRO-2 trial.
- RAD51 y HRR: Arce-Gallego, S., Morgado, P. C., Delgado-Serrano, L., Simonetti, S., Gonzalez, M., Romero-Lozano, P., ... & Mateo, J. (2025). Homologous recombination repair status in metastatic prostate cancer by next-generation sequencing and functional immunofluorescence. Cell Reports Medicine.
- Desafíos en el Manejo: Ozay, Z. I., Swami, U., & Agarwal, N. (2025). Challenges in the Management of Advanced Prostate Cancer. JCO Oncology Practice, OP-25.