| Introducción |
A nivel mundial, el virus sincicial respiratorio (VSR) se asocia con una morbilidad y mortalidad considerables en lactantes y niños pequeños. Es uno de los patógenos más asociados con hospitalizaciones por neumonía en niños.
El diagnóstico clínico de la enfermedad por VSR en lactantes es difícil, debido a la inespecificidad de los síntomas que se asemejan a los de otras enfermedades respiratorias.
Los lactantes menores de 6 meses presentan la mayor carga de enfermedad, lo que representa una quinta parte de todas las infecciones y casi el 40 % de todas las hospitalizaciones por VSR. De estas hospitalizaciones, la mayoría (61 %) se producen durante los primeros 3 meses de vida. Asimismo, existe una alta carga de enfermedad en los niños nacidos prematuros. El número estimado mundial de IVRI por VSR en el primer año de vida entre los lactantes prematuros en 2019 fue de 1,6 millones, con 533 000 hospitalizaciones y 26 760 muertes atribuibles al VSR, de las cuales solo el 11 % fueron hospitalarias.
| Presentación clínica |
La enfermedad pediátrica grave por VSR puede clasificarse, según el síndrome clínico, en tres grupos de edad:
- Los neonatos con enfermedad similar a la sepsis o apneas.
- Los niños menores de 2 años con bronquiolitis.
- Los niños mayores con neumonía.
Los lactantes pueden desarrollar insuficiencia respiratoria, que puede ser potencialmente mortal. La bronquiolitis y la neumonía se diagnostican principalmente mediante evaluación clínica, y las pruebas de laboratorio podrían no modificar sustancialmente el tratamiento de estas afecciones.
Sin embargo, confirmar una causa viral mediante pruebas moleculares puede ser importante para evitar el uso innecesario de antibióticos durante las infecciones graves de las vías respiratorias inferiores (IVRI). Los avances en las pruebas del VSR en los últimos 10 años incluyen las pruebas moleculares en el punto de atención, con una sensibilidad y especificidad no inferiores a las de la prueba PCR.
La mayoría de las infecciones por VSR en bebés son asintomáticas o se manifiestan con síntomas leves y autolimitados. Sin embargo, el VSR también es una de las principales causas de IVRI grave en niños pequeños. La enfermedad grave por VSR suele presentarse con hipoxemia, sibilancias y tiraje torácico, que no se incluyen en las definiciones de caso de infección respiratoria aguda grave (IRAG) ni de enfermedad pseudogripal.
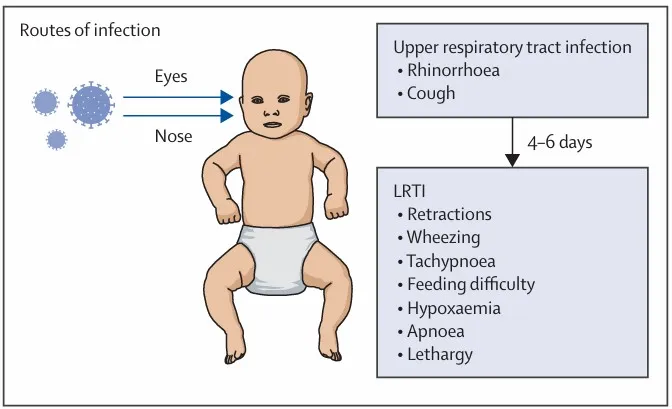
Aunque no existen signos clínicos patognomónicos para la enfermedad grave por VSR, esta se manifiesta principalmente con síntomas respiratorios superiores, como rinorrea y tos, antes de progresar a síntomas pulmonares. La fiebre no suele asociarse con la infección por VSR, presentándose en aproximadamente el 15 % de los casos sintomáticos.
Tras 4-6 días de signos clínicos respiratorios superiores, los niños pueden desarrollar un mayor esfuerzo respiratorio acompañado de retracciones, sibilancias, taquipnea y dificultad para alimentarse. Finalmente, los niños con progresión clínica grave pueden presentar hipoxemia, anorexia, apnea, letargo o irritabilidad, lo que indica la necesidad de hospitalización.
No se dispone de métodos estandarizados para evaluar la gravedad del VSR en lactantes. Además, no existen criterios estandarizados para los ingresos hospitalarios o en la unidad de cuidados intensivos pediátricos (UCIP).
| Manejo hospitalario |
Los cuidados de apoyo mediante hidratación con líquidos y soporte respiratorio son la base del manejo hospitalario de la bronquiolitis y la neumonía por VSR. Sin embargo, no existe una terapia basada en la evidencia para la infección por VSR. La solución salina hipertónica nebulizada sugirió una reducción de la duración de la estancia hospitalaria de 0,40 días, aunque esto no es clínicamente relevante.
Se estima que la incidencia de coinfecciones bacterianas en pacientes con infección por VSR es inferior al 11 %, pero casi un tercio de los niños con IVRI por VSR reciben tratamiento innecesario con antibióticos. La decisión de administrar antibióticos no solo debe basarse en la proteína C reactiva elevada, sino también en indicadores generales de infección bacteriana grave, como la edad neonatal y el deterioro durante la ventilación.
La oxigenoterapia es un pilar del manejo del VSR, tanto en salas de hospitalización general como en UCIP. Se ha establecido un umbral de saturación de oxígeno basado en la evidencia del 90 % para la suplementación.
La oxigenoterapia con cánula nasal de alto flujo (CNAF) se ha utilizado cada vez más en la última década para el manejo de lactantes hospitalizados, además de la oxigenoterapia estándar con cánula nasal de bajo flujo (BF). Las ventajas prácticas de la CNAF son la facilidad de uso para el personal hospitalario y una mayor comodidad. Pero el uso de CNAF puede retrasar la ventilación mecánica y poner al niño en una situación de riesgo.
Además de la CNAF, la ventilación mecánica mediante intubación endotraqueal se introdujo en el tratamiento de la bronquiolitis viral en la década de 1960, y desde la década de 1980 se utilizan cada vez más diversas opciones de soporte respiratorio no invasivo en la UCIP, debido a su potencial para evitar complicaciones asociadas con la ventilación mecánica invasiva. La ventilación no invasiva incluye opciones que proporcionan soporte de volumen o presión, o que proporcionan soporte de presión durante la respiración espontánea, incluyendo la presión positiva continua en la vía aérea (CPAP) nasal administrada a través de una mascarilla facial y la CNAF. Los profesionales sanitarios pueden ser reticentes a utilizar la CPAP para el tratamiento de la bronquiolitis, debido a los posibles efectos adversos (daño local de la mucosa nasal, aspiración secundaria a la insuflación gástrica y neumotórax) y al retraso en la atención definitiva. De igual manera, la evidencia insuficiente de eficacia, los altos costos y el aumento de los ingresos en la UCIP respaldan la eliminación de la CNAF de la atención estándar en las salas de pediatría general.
| Terapias emergentes |
La terapia antiviral no ha demostrado ser muy prometedora en el tratamiento de la infección por VSR. En general, la prevención de la infección es un enfoque más prometedor que el tratamiento, ya que administrar el tratamiento en las 24-48 horas siguientes al inicio de los síntomas rara vez es factible.
⮕ Intervenciones no farmacéuticas y transmisión
Aunque los estudios sobre la transmisibilidad aérea del VSR son escasos, se sabe que se transmite a través del contacto directo e indirecto con gotitas contaminadas con el virus en las manos o fómites. Las medidas que incluyeron distanciamiento físico, cuarentenas, uso de mascarillas y lavado de manos, redujeron notablemente la circulación del VSR y otros virus respiratorios. La desinfección de juguetes, superficies y fómites cada dos semanas redujo significativamente la presencia de material genético viral del VSR y otros virus respiratorios en el ambiente.
⮕ Anticuerpos monoclonales
Los avances en la investigación de vacunas contra el VSR se han visto impulsados por el conocimiento de las respuestas inmunitarias al VSR y las aplicaciones innovadoras de la inmunología estructural en el diseño de antígenos.
La profilaxis con anticuerpos monoclonales (AcMs) ha sido un método de eficacia comprobada para proteger a los lactantes del VSR. El uso de palivizumab se limita en gran medida a lactantes de alto riesgo en países de ingresos altos debido a los altos costos y a la administración mediante inyecciones mensuales durante la temporada de VSR. A principios de 2023, nirsevimab, un AcM de vida media prolongada, recibió la aprobación de comercialización en Europa y EE. UU. para todos los lactantes. Permite una mayor protección durante toda la temporada de VSR con una sola inyección. Se prevén otros AcMs contra el VSR.
⮕ Vacunación materna
Vacunar a las embarazadas es una estrategia alternativa para proteger a los lactantes contra el VSR. RSVpreF, una vacuna proteica de prefusión bivalente para uso durante el embarazo, fue aprobada en varios países a mediados de 2023. Una vacuna basada en ARNm (ARNm-1345) se encuentra en fase 2 de desarrollo.
| Prevención dirigida |
Idealmente, la prevención del VSR se dirigirá a todos los lactantes, pero como mínimo, se dirigirá a los niños con alto riesgo de enfermedad potencialmente mortal.
⮕ Factores de riesgo relacionados con el paciente
Las afecciones médicas subyacentes para la enfermedad grave por VSR incluyen:
- Prematuridad.
- Enfermedad neurológica.
- Síndrome de Down.
- Enfermedad pulmonar crónica.
- Inmunodeficiencia.
- Cardiopatía congénita.
⮕ Factores de riesgo relacionados con la exposición
Los factores virales asociados, como la cepa del VSR y la codetección de otros patógenos (excepto Haemophilus spp) no se asociaron con una mayor gravedad de la enfermedad. Otro aspecto importante es la relación entre la estacionalidad del VSR y la edad temprana durante la temporada del VSR, donde los bebés menores de 6 meses durante el período de circulación viral tienen mayor riesgo y peores resultados clínicos La exposición a otros niños potencialmente portadores del VSR, como hermanos o asistencia a guarderías, son factores de riesgo conocidos.
⮕ Factores de riesgo socioeconómicos
Más del 70 % de las muertes atribuibles al VSR ocurren fuera del hospital, donde la atención médica es inadecuada, especialmente en condiciones de pobreza estructural. Estos niños suelen vivir en entornos socioeconómicamente vulnerables, como viviendas superpobladas en barrios marginales y densamente poblados con escaso acceso al transporte público y a centros de atención primaria.
Otras características de las muertes infantiles en la comunidad asociadas al VSR, en comparación con las muertes hospitalarias, son la menor duración de la enfermedad y la menor gravedad histopatológica. Para que la prevención del VSR tenga el mayor impacto contra el VSR potencialmente mortal, se necesita acceso urgente a intervenciones preventivas en poblaciones vulnerables donde el acceso a nuevas terapias probablemente se retrasará o no estará disponible en absoluto.
⮕ Secuelas respiratorias a largo plazo
Aunque varios estudios observacionales muestran una asociación entre la infección temprana por VSR y las sibilancias recurrentes y el asma en la infancia, existen pocos ensayos clínicos que puedan establecer una relación causal.
Los lactantes con IVRI por VSR más graves mostraron un mayor riesgo de desarrollar sibilancias recurrentes durante el primer año de vida. Sin embargo, pocos ensayos clínicos aleatorizados han explorado la eficacia de la inmunización preventiva con palivizumab en lactantes prematuros para prevenir las sibilancias recurrentes y el asma en la infancia. Estos ensayos clínicos no demostraron una prevención eficaz de la aparición del asma a los 5 años en comparación con placebo.
| Conclusiones |
Hemos entrado en una nueva era de la pediatría, en la que el VSR se ha convertido en una enfermedad prevenible mediante vacunación en todos los niños. Si bien la inmunización universal debería ser el objetivo, se podría priorizar a los grupos de alto riesgo en el proceso de implementación de la vacuna, incluidas las poblaciones que presentan la mayor carga de VSR potencialmente mortal.
El tratamiento del VSR es poco prometedor y los cuidados de apoyo son la base del manejo. La aparición y la implementación generalizada de la CNAF no cuentan con una base empírica coherente, por lo que esta terapia debería eliminarse de la práctica habitual.
La implementación de la vacuna tendrá un impacto real, incluyendo su eficacia contra las IVR por todas las causas y su impacto en el microbioma respiratorio.
| Comentario: El presente estudio destaca que la enfermedad severa por VSR tiene diferentes formas de presentación, pero no puede distinguirse de otras enfermedades respiratorias sin un test viral. Aunque una alta proporción de niños con infección severa tiene comorbilidades, la mayoría de los lactantes afectados nacieron a término y eran previamente sanos. Debido a que el tratamiento y el manejo hospitalario de la infección por VSR es de sostén, se enfatiza la necesidad de priorizar estrategias de prevención enfocadas a la vacunación de personas gestantes y a lactantes menores de 6 meses o hasta los 2 años si tienen factores de riesgo de enfermedad severa. |