| Introducción |
El accidente cerebrovascular (ACV) fue la segunda causa principal de muerte y la tercera de muerte y discapacidad combinadas en 2019. Se cree que el ACV isquémico es el subtipo más común, con el 62,4 % de los ACV, mientras que la hemorragia intracerebral (HIC) constituye el 27,9 % y la hemorragia subaracnoidea (HSA) el 9,7 %.
Las lesiones isquémicas de patogénesis de vasos pequeños suelen encontrarse en la HIC aguda y la HIC primaria comparte factores de riesgo y patología vascular similar a la oclusión de vasos pequeños. La HIC está relacionada con un control deficiente de la presión arterial (PA) y una anomalía vascular que resulta en la ruptura de pequeñas arterias penetrantes.
En comparación con el ACV isquémico, la HIC tiene mortalidad más alta y discapacidad más grave. Con mejor control de la PA, la frecuencia de la HIC se redujo, pero sigue teniendo una carga crítica.
| Epidemiología |
Los países de ingresos bajos y medios tienen una mayor incidencia de HIC que los países de ingresos altos. La tasa de incidencia de HIC en EE. UU., Reino Unido y Australia se estima entre el 8 y el 15 %, mientras que en Japón, Taiwán y Corea es del 18 al 24 %.
En EE. UU., la incidencia de HIC entre los negros es casi 1,6 veces mayor que entre los blancos y 1,6 veces mayor entre los mexicanos americanos que entre los blancos no hispanos. En China, la incidencia y prevalencia de ACV fueron del 69,6 % y el 77,8 % en ACV isquémicos, del 23,8 % y el 15,8 % en HIC, del 4,4 % y el 4,4 % en HSA y del 2,1 % y el 2,0 % en tipo indeterminado.
Los mexicanos, latinoamericanos, afroamericanos, japoneses y chinos tienen mayor incidencia de HIC en comparación con los estadounidenses blancos.
| Fisiopatología |
En la etapa inicial de la lesión, la ruptura de los vasos sanguíneos puede provocar la formación de un hematoma que causa una lesión mecánica con compresión del parénquima cerebral por efecto de masa que resulta en una alteración física de la arquitectura parenquimatosa. La lesión secundaria produce la activación de la microglía que libera sustancias perjudiciales que causan disfunción de la barrera hematoencefálica, edema vasogénico y apoptosis en neuronas y glía.
La presión intracraneal (PI) aumentará, debido a la expansión del hematoma que puede afectar el flujo sanguíneo y causar deformación mecánica. Hay oligoemia, liberación de neurotransmisores, disfunción mitocondrial y despolarización de la membrana.
La HIC primaria puede deberse a hipertensión, angiopatía amiloide cerebral (AAC) y HSA. La hipertensión es el principal factor de riesgo atribuible al 65 % de las HIC.
La HIC secundaria es causada por tumores cerebrales, aneurismas, malformaciones arteriovenosas y cavernosas cerebrales y coagulopatía. La mayoría de las hemorragias en las HIC relacionadas con la hipertensión se producen en o cerca de la bifurcación de pequeñas arterias penetrantes que se originan en las arterias basilares o cerebrales anterior, media o posterior. Las lesiones se caracterizan por rotura de la lámina elástica, atrofia y fragmentación del músculo liso, disecciones y degeneración celular granular o vesicular.
La AAC es una causa común de HIC sintomática e implica el depósito de péptidos β-amiloide en la media de vasos leptomeníngeos y corticales pequeños y mediano que rodean las células del músculo liso vascular. Estas arterias debilitadas pueden romperse y provocar microhemorragias cerebrales o HIC lobar. La HIC en pacientes más jóvenes se asocia con mayor probabilidad a malformaciones vasculares, pero en pacientes mayores es más probable que sea resultado de angiopatía amiloide. La HIC profunda en el tálamo o los ganglios basales es más probable que se deba a hemorragias hipertensivas, independientemente de la edad.
Con respecto a la HIC asociada a anticoagulantes, un metanálisis de ensayos aleatorizados de fase 3 incluyó datos de los cuatro nuevos anticoagulantes orales en pacientes con fibrilación auricular. Este metanálisis demostró un perfil de riesgo-beneficio favorable y reveló que los nuevos anticoagulantes orales podrían reducir los eventos de ACV o embolia sistémica en un 19 %, en comparación con la warfarina, con una reducción principalmente en el ACV hemorrágico.
Los nuevos anticoagulantes podrían reducir significativamente la mortalidad por todas las causas y la HIC, pero aumentar la frecuencia de sangrado gastrointestinal.
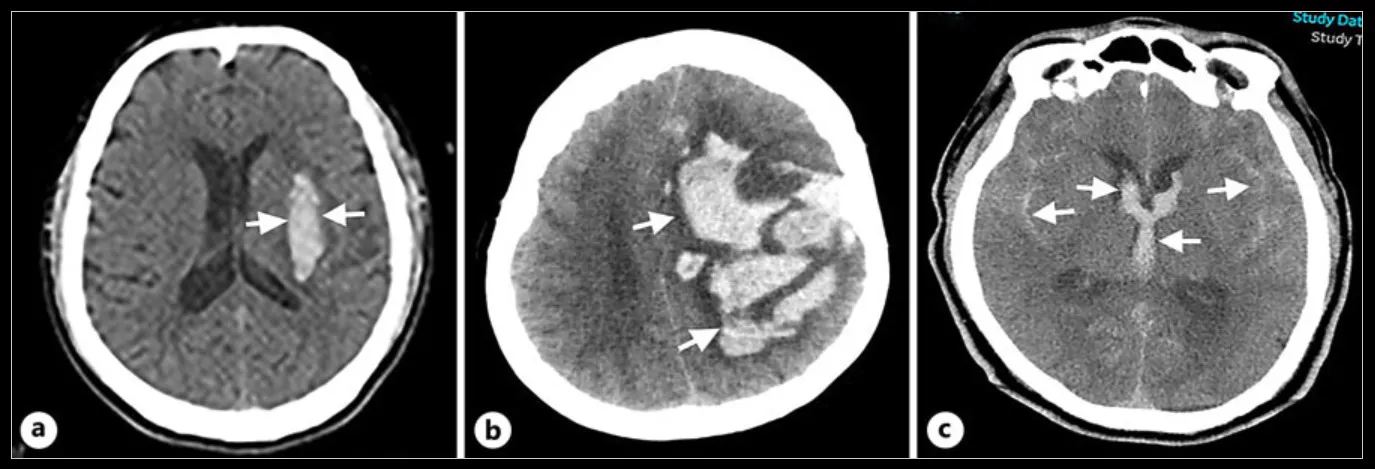
Hallazgos tomográficos computarizados cerebrales de las localizaciones en diferentes subtipos de hemorragia intracraneal. a Indica hemorragia intramuscular hipertensiva en la zona putaminada izquierda. b Indica hemorragia lobular en el lóbulo frontal izquierdo. c Indica hemorragia subaracnoidea con sangre en el espacio subaracnoideo y en las áreas intraventriculares.
| Factores de riesgo |
Diferencias de sexo
Una revisión de la literatura encontró que la epidemiología, los factores de riesgo y el manejo de la HIC espontánea podrían ser diferentes según el sexo. Los hombres pueden experimentar HIC espontánea con mayor frecuencia a edades más tempranas. Los factores de riesgo como el consumo de cocaína, consumo excesivo de alcohol y de tabaco son más comunes en los hombres.
Las mujeres experimentan HIC lobar con mayor frecuencia, mientras que ambos sexos tienen una distribución uniforme de HIC profunda. Las mujeres reciben un manejo menos agresivo que los hombres que probablemente afecte la supervivencia.
Las mujeres eran mayores al inicio y tenían mayor gravedad clínica con una puntuación más alta en la Escala de Ictus de los Institutos Nacionales de Salud (NIHSS) que los hombres. En cuanto a la tasa de letalidad en un año, las mujeres tuvieron una tasa más alta que los hombres (48,5 % frente a 40,1 %), que probablemente estuvo relacionada con una edad más avanzada al inicio de la HIC y una puntuación más alta en la NIHSS en mujeres.
Edad
La incidencia de HIC espontánea aumenta exponencialmente con la edad. En mayores de 80 años representa una proporción creciente de causa de ingreso en unidades de ictus.
Entre los pacientes jóvenes y de mediana edad, las mujeres están relacionadas con una tasa de mortalidad hospitalaria por HIC más baja que los hombres, y los varones mayores tienen un mayor riesgo de complicaciones que pueden contribuir a una mayor mortalidad hospitalaria. Los pacientes mayores pueden tener mayor proporción de angiopatía amiloide y mayor uso de fármacos antitrombóticos que resultan en hemorragia lobar y causan mayor riesgo de agrandamiento del hematoma. La edad avanzada, especialmente después de los 80 años, es un predictor importante de mortalidad por HIC independientemente de las características relacionadas con la gravedad de la HIC.
Los factores de riesgo modificables incluyen:
- PA alta.
- Tabaquismo actual.
- Consumo excesivo de alcohol.
- Colesterol de baja densidad bajo.
- Triglicéridos bajos.
- Uso de anticoagulantes y antiplaquetarios y simpaticomiméticos, como cocaína, heroína, anfetamina, fenilpropanolamina y efedrina, que usan con mayor frecuencia en pacientes jóvenes.
Se sugiere que la fenilpropanolamina es un factor de riesgo independiente para la HIC, especialmente en mujeres.
Los factores de riesgo no modificables son:
- la vejez,
- el sexo masculino,
- la etnia asiática,
- el aneurisma aórtico coronario,
- las microhemorragias cerebrales,
- la función renal deficiente.
Otras condiciones que podrían relacionarse con el riesgo de HIC pueden incluir multiparidad, malas condiciones laborales y duración prolongada del sueño.
El genotipo APOE ε2 o ε4 tiene una fuerte asociación con HIC lobular. La hipertensión es el factor de riesgo más importante para HIC espontánea y está más relacionada con HIC profunda que con HIC lobular. La hipertensión en HIC de posición profunda es dos veces más común que en HIC lobular.
El nivel alto de colesterol o el consumo moderado de alcohol (<=2 bebidas por día) son menos frecuentes en HIC profunda. Podría observarse una asociación protectora entre el nivel alto de colesterol y la HIC profunda, pero no se puede observar tal asociación en la HIC lobular.
La warfarina puede aumentar el riesgo de HIC de 2 a 5 veces si el RIN >3,0 y es probable que contribuya a un exceso de mortalidad. En la población general, la aspirina no se asociaba con el riesgo de HIC y el uso crónico en dosis bajas puede asociarse con un efecto protector sobre la HSA.
Diabetes mellitus
Un artículo de revisión encontró que puede haber asociaciones modestas entre la diabetes y la aparición y el resultado de la HIC, y un estudio de cohorte reveló que la HIC en pacientes diabéticos suele presentar características clínicas diferentes y la diabetes podría ser un determinante independiente de muerte después de la HIC.
Enfermedad renal crónica
La disminución de la tasa de filtración glomerular es un fuerte factor de riesgo para el ACV hemorrágico, pero no para el ACV isquémico. La enfermedad renal crónica se asocia con mayor presencia y número de microhemorragias cerebrales, particularmente en personas negras. La disfunción plaquetaria en pacientes con enfermedad renal crónica también podría explicar el mayor riesgo de HIC.
Microhemorragias cerebrales
Pueden aumentar el riesgo de HIC espontánea, que es mayor que el riesgo de ACV isquémico recurrente. Las microhemorragias cerebrales también pueden aumentar el riesgo de HIC asociada a warfarina o antiplaquetarios. Aunque un estudio de cohorte de pacientes con ACV isquémico mostró que las microhemorragias cerebrales tenían mayor riesgo de ACV isquémico futuro, pero no de HIC, un estudio prospectivo mostró que las microhemorragias cerebrales estaban más fuertemente asociadas con HIC que con ACV isquémico.
| Tratamiento de la hemorragia intracerebral |
Tratamiento quirúrgico
El estudio ENRICH (Extracción temprana mínimamente invasiva de la hemorragia intracerebral) sugiere que la cirugía parafascicular transulcal mínimamente invasiva puede recomendarse para la HIC lobular de 30 a 80 ml dentro de las 24 h del inicio para reducir el volumen del hematoma a <15 ml en pacientes de 18 a 80 años sin discapacidad significativa.
El estudio SWITCH es un ensayo clínico aleatorizado de craneotomía descompresiva en comparación con el tratamiento médico en pacientes con hemorragia intracerebral profunda grave dentro de las 72 h del inicio del ACV. El estudio SWITCH sugirió que la craneotomía descompresiva sin evacuación del coágulo podría beneficiar a pacientes con hemorragia intracerebral de 18 a 75 años con 30 a 100 ml en los ganglios basales o el tálamo.
Las pautas de la American Stroke Association sugieren que en los pacientes con HIC con hidrocefalia que contribuye al aumento de la PIC, si hay una disminución del nivel de conciencia, se debe realizar un drenaje ventricular para reducir la mortalidad. En pacientes con HIC con un nivel de conciencia reducido, se podría considerar la monitorización y el tratamiento de la PIC para reducir la mortalidad y mejorar los resultados.
Tratamiento médico de la HIC
La reducción de la PA en la fase aguda de la HIC es beneficiosa para mejorar los resultados funcionales. La presión arterial debe ajustarse cuidadosamente para asegurar un control continuo, uniforme y sostenido y evitar picos y gran variabilidad en la PA sistólica. La reducción de la PA en la HIC aguda debe iniciarse lo antes posible dentro de las 2 h del inicio de la HIC, y el objetivo de PA debe alcanzarse dentro de la hora para reducir el riesgo de expansión del hematoma y mejorar el resultado funcional.
En pacientes con gravedad leve a moderada de HIC aguda, si la PA sistólica es de 150-220 mmHg, el objetivo de PA debe reducirse por debajo de 140 mmHg y mantenerse en 130-150 mmHg para mejorar los resultados funcionales. Un informe reciente sugiere que la reducción aguda a un objetivo de PA sistólica de 110-139 mmHg en la HIC aguda puede ser mejor para mejorar el resultado funcional que una reducción a un objetivo de presión arterial sistólica de 140-179 mmHg. En pacientes con HIC moderada a grave, el objetivo de la reducción aguda de la PA no está bien establecido. Sin embargo, la reducción intensiva de la PA sistólica puede reducir la frecuencia de expansión del hematoma, pero no reduce la tasa de muerte o discapacidad.
El cambio absoluto medio de la PA sistólica se asocia con el crecimiento del hematoma, y un control sostenido de la PA con una reducción de la variabilidad de la PA sistólica es importante para aumentar el efecto beneficioso del tratamiento antihipertensivo intensivo. Para mantener el control de la PA y minimizar la variabilidad de la PA sistólica, los fármacos antihipertensivos que tienen un inicio de acción rápido, una duración de acción corta y una titulación fácil son los más sugeridos.
El uso ultra agudo de vasodilatadores venosos puede ser perjudicial en pacientes con HIC aguda. El momento para iniciar el tratamiento de la hipertensión y la clase de medicación para lograr un buen control de la PA aún son inciertos.
Se puede considerar la terapia hiperosmolar en bolo, pero no los corticosteroides, para reducir la PIC. La eficacia de la terapia hiperosmolar profiláctica temprana para mejorar los resultados no está bien establecida.
Neuroprotección
Se sugirió que las estatinas respaldan la neuroprotección potencial y mejoran la recuperación en la HIC aguda. Los mecanismos propuestos incluyen promoción de la angiogénesis, aumento de la neurogénesis, inhibición de la apoptosis neuronal, aceleración de la resolución del hematoma, disminución de la inflamación en la zona límite de la HIC y disminución del edema perihematomal. Sin embargo, los estudios sobre la relación de las estatinas con los resultados posteriores a la HIC son limitados, lo que impide una evaluación objetiva de los posibles beneficios terapéuticos de las estatinas en pacientes con HIC.
Se informa que el tratamiento con albúmina sérica humana proporciona neuroprotección y mejora la recuperación al mejorar la función neurológica a corto y largo plazo, mantiene la integridad de la barrera hematoencefálica y reduce el estrés oxidativo neuronal y la apoptosis. Se sugiere que la albuminemia baja al ingreso es un factor pronóstico de malos resultados en pacientes con HIC. Sin embargo, el ensayo se dio por terminado por la baja inscripción y sus posibles efectos adversos.
Se sugiere que la hipotermia terapéutica reduce los mecanismos de muerte celular iniciados por la HIC. Sin embargo, los datos actuales sobre la hipotermia terapéutica en la HIC siguen siendo cuestionables a pesar de las indicaciones prometedoras en estudios con animales. Aun se requieren estudios controlados para responder a esta pregunta terapéutica.
Resultado
La HIC es un subtipo de ACV que se asocia con una alta mortalidad y suele presentar deterioros neurológicos si se sobrevive. Hasta ahora, no se ha realizado ningún ensayo clínico de fase III exitoso que haya demostrado mejorar el resultado de la HIC.
Aunque la HIC constituye un porcentaje pequeño de la prevalencia general de ACV (cerca del 10-15 %), la morbilidad y la mortalidad asociadas son desproporcionadamente altas. Las tasas de mortalidad intrahospitalaria varían del 27,1 al 37,5 %, y la mortalidad a los 2 años puede llegar al 49,5 %.
Solo el 14,5 % de los pacientes que presentan HIC sintomática pueden ser dados de alta a su domicilio de forma independiente, pero más del 34% con HIC sintomática fueron dados de alta a un centro de cuidados a largo plazo. En la HIC, la expansión del hematoma y las complicaciones son las principales causas de muerte en la etapa temprana.
Los factores de mal pronóstico de la HIC pueden incluir una puntuación baja en la escala de Glasgow al inicio, un volumen de la HIC ≥30 cm3, localización infratentoria, ≥80 años, lesiones avanzadas de la sustancia blanca en la imagen cerebral, bajo peso corporal e hiperglucemia al ingreso y una función renal deficiente con una tasa de filtración glomerular estimada <60 mL/min/m2.
| Hallazgos radiológicos |
La expansión del hematoma es un indicador para predecir un mal pronóstico y ocurre en hasta un tercio de los pacientes con HIC. Los estudios sugieren que la expansión del hematoma se puede prevenir utilizando marcadores de imagen.
Hay algunos marcadores específicos en la tomografía y la angiografía por TAC en la fase aguda de la HIC que se sugieren para identificar la expansión del hematoma de manera temprana. Estos marcadores de imagen incluyen los signos:
- del agujero negro,
- de la mezcla,
- del yodo,
- de la isla,
- de fuga,
- del satélite,
- de la mancha,
- de la cola de la mancha,
- del remolino,
- las hipodensidades.
| Sistema de puntuación pronóstica de la HIC |
En la población china se descubrió que el uso del sistema de puntuación de la HIC y el sistema de puntuación de la escala de calificación de la HIC predice con precisión el resultado funcional favorable a corto y largo plazo en pacientes con HIC. El sistema de puntuación de la HIC también puede tener un buen valor predictivo en la evaluación pronóstica de la mortalidad a los 30 días para pacientes que toman anticoagulantes orales, especialmente el uso de anticoagulantes orales sin vitamina K.
La puntuación pronóstica de Osaka (OPS) y la puntuación pronóstica de Nápoles (NPS) se establecen en función del estado inflamatorio y nutricional. Un estudio de cohorte mostró que si había niveles más altos de OPS y NPS al ingreso, había un peor resultado a los 6 meses después de la HIC, lo que sugiere el papel potencial de estos sistemas de puntuación para actuar como marcadores pronósticos para predecir el resultado de la HIC.
| Causa de muerte |
Las muertes dentro de la primera semana suelen deberse a la consecuencia directa de la lesión hemorrágica, mientras que las muertes en las semanas siguientes están relacionadas principalmente con complicaciones médicas. La comparación de la causa de muerte en HIC entre diferentes países mostró que en Asia, el ACV y el cáncer son las causas más comunes de muerte, mientras que en los no asiáticos, el ACV y la enfermedad cardíaca son las causas más comunes de muerte.
| Riesgo de recurrencia |
El riesgo de HIC recurrente varía de 1,2 a 3 % por año en todos los pacientes con HIC, y el primer año después del incidente de HIC tiene la tasa de recurrencia más alta. En pacientes con una HIC primaria, la tasa de recurrencia, muerte vascular o eventos vasculares se estima en 2,1 % a 5,9 % anualmente.
En pacientes con HIC de ≥65 años, el riesgo de recurrencia, evento vascular o muerte se duplica. Los pacientes asiáticos y negros con HIC tienen un mayor riesgo de evento recurrente que los blancos, y los pacientes con seguro privado tienen un riesgo reducido en comparación con aquellos con Medicare.
En pacientes con HIC, menos de la mitad pueden sobrevivir 1 año y menos de un tercio 5 años. Después de una HIC, el riesgo de HIC recurrente o ACV isquémico recurrente parece similar.
| Prevención secundaria |
Es recomendable considerar los factores de riesgo para prevenir la recurrencia:
- Ubicación lobar de la HIC inicial.
- Edad avanzada.
- Presencia, número y ubicación lobar de microhemorragias en la RM.
- Siderosis superficial cortical diseminada en la RM.
- Hipertensión mal controlada.
- Raza asiática o negra.
- Presencia de alelos ε2 o ε4 de la apolipoproteína E.
| Conclusión |
La incidencia, los factores de riesgo y la causa de muerte en pacientes con HIC difieren entre las etnias y los géneros. El tratamiento médico requiere un control intensivo de la PA y se puede considerar la cirugía mínimamente invasiva para la HIC lobar dentro de las 24 horas posteriores a su aparición.
La HIC conlleva una alta mortalidad y, si se sobrevive, se producen importantes deterioros neurológicos. La HIC es una enfermedad crítica y se necesitan más estudios para mejorar los resultados de los pacientes.