Diseñar estudios clínicos en tumores poco frecuentes representa un desafío significativo, debido a la baja incidencia de estos cánceres, lo que limita la disponibilidad de pacientes elegibles y retrasa la recolección de datos.
Para superar estas barreras, es fundamental adoptar enfoques metodológicos flexibles, como los estudios basket, umbrella o plataformas adaptativas, que permiten evaluar múltiples tratamientos o biomarcadores en paralelo. También es clave fomentar la colaboración entre múltiples centros, incluyendo redes internacionales, para maximizar la inclusión de pacientes.
Además, pueden emplearse criterios de inclusión más amplios y el uso de endpoints alternativos, como los biomarcadores de respuesta, para agilizar la obtención de resultados clínicamente significativos.
Otro aspecto esencial es la integración de datos del mundo real y registros observacionales para complementar la evidencia generada en ensayos prospectivos. Las nuevas tecnologías, como la inteligencia artificial y los análisis genómicos, permiten identificar subgrupos moleculares dentro de tumores raros que podrían beneficiarse de terapias dirigidas, facilitando el diseño de estudios más personalizados.
Finalmente, es necesario establecer estrategias regulatorias diferenciadas, que reconozcan las particularidades de estas patologías y permitan una aprobación acelerada de tratamientos en contextos de alta necesidad médica no cubierta.
El ensayo aleatorizado BEVANEC presenta el diseño de un ensayo clínico controlado externamente para pacientes con carcinomas neuroendocrinos gastroenteropancreáticos (GEP-NEC).
Los autores proponen el uso de datos del mundo real (RWD) para crear un brazo de control externo (ECA) que permita comparar la eficacia de FOLFIRI con bevacizumab frente a FOLFIRI solo.
Este enfoque es especialmente relevante para cánceres raros, donde los ensayos clínicos aleatorizados tradicionales son difíciles de realizar, debido al bajo número de pacientes. Los resultados muestran que el ECA, generado a partir de datos retrospectivos y prospectivos, logró un equilibrio en las características basales de los pacientes y resultados similares a los del ensayo BEVANEC original, validando la viabilidad de este diseño.
El estudio utilizó métodos estadísticos avanzados, como la ponderación por el inverso de la puntuación de propensión (IPW-PS), para equilibrar las características de los pacientes entre el brazo experimental y el ECA. Aunque algunos datos clave, como el estado funcional (ECOG) y los niveles de LDH estaban ausentes en el RWD, el análisis demostró que el ECA era adecuado para su uso.
Las tasas de supervivencia global a 6 y 12 meses fueron similares entre el ECA y el brazo de control aleatorizado del ensayo BEVANEC, lo que respalda la validez de los resultados obtenidos con el diseño controlado externamente.
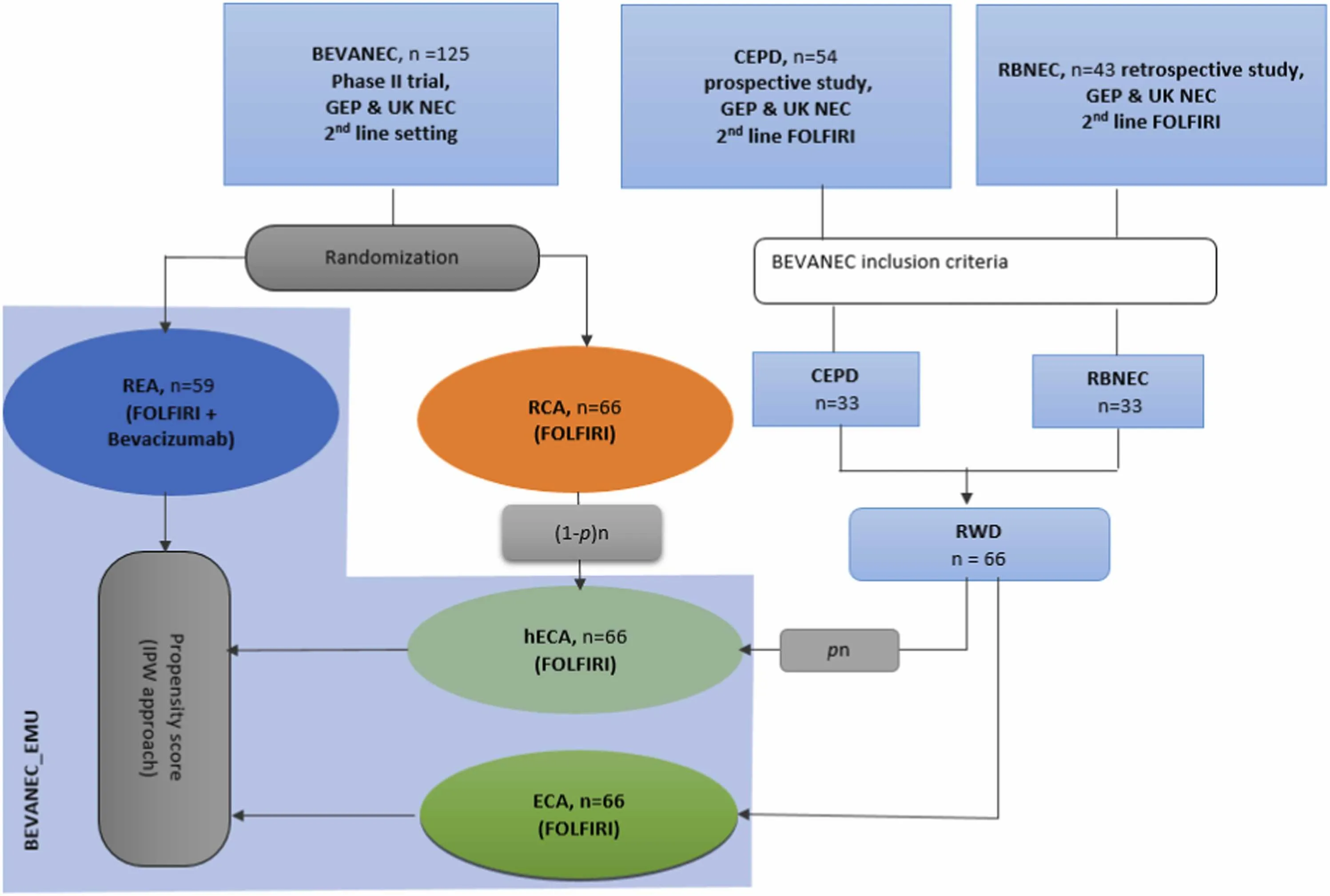
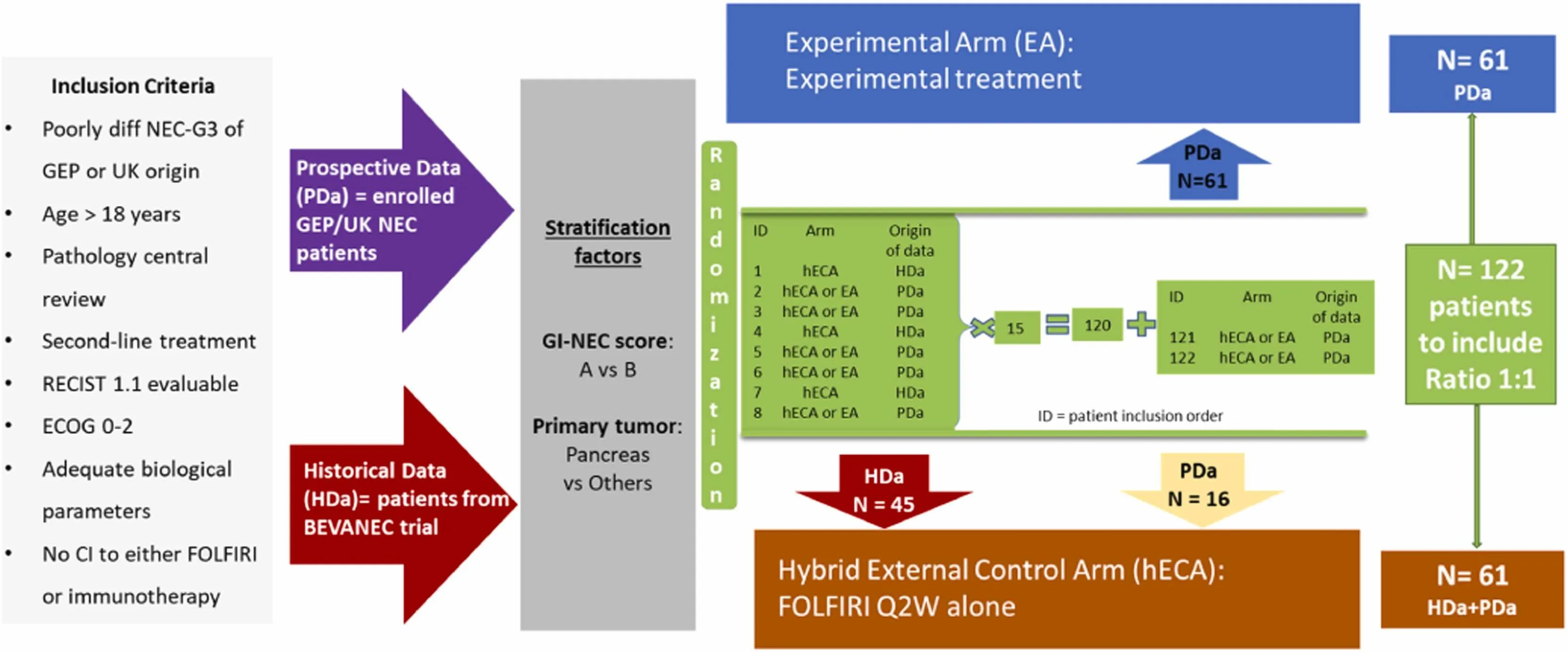
Además, los autores exploraron el uso de un ECA híbrido (hECA), que combina datos prospectivos y RWD, para mejorar la comparabilidad y reducir el número de pacientes necesarios en futuros ensayos.
Este enfoque permitió mantener el equilibrio en las características basales y replicar los hallazgos del ensayo original. Basándose en estos resultados, se diseñó el ensayo REVENEC-01, un estudio prospectivo que evaluará una combinación de inmunoterapia con FOLFIRI en GEP-NEC, utilizando un hECA con un 75 % de datos históricos y un algoritmo de aleatorización adaptativo.
Así se destaca el potencial de los ensayos controlados externamente para acelerar la investigación en cánceres raros y agresivos, donde los ensayos tradicionales son costosos y lentos.
Sin embargo, se señalan desafíos como la falta de datos de seguridad en el RWD y la necesidad de estrategias rigurosas para manejar información faltante. Los autores concluyen que este enfoque, respaldado por redes académicas y datos de alta calidad, puede ser una herramienta valiosa para evaluar nuevas terapias y obtener evidencia aceptable para las agencias reguladoras.