| Introducción |
La resección hepática es el tratamiento curativo principal de los tumores del hígado [1,2], estando recomendada la hepatectomía anatómica para el tratamiento del carcinoma hepatocelular y de algunos cánceres metastásicos en el hígado [3].
Dado que los cirujanos no pueden ver completamente la estructura intraparenquimatosa, sólo las venas hepáticas están disponibles como hitos para realizar la disección parenquimatosa del hígado en muchos casos.
Recientemente, se ha desarrollado una técnica de imágenes basada en verde de indocianina (VIC) fluorescente para brindar una visión anatómica segura del parénquima hepático en la cirugía hepatobiliar [4]. Sin embargo, esta técnica requiere que el cirujano utilice una cámara de mano para capturar las imágenes, estando afectada la calidad de la imagen por el movimiento de la mano y el temblor fisiológico.
La técnica requiere también oscurecimiento de la luz dentro del campo operatorio para prevenir la contaminación con luz blanca de las imágenes. Asimismo, las imágenes fluorescentes son mostradas en un monitor, lo que requiere que los cirujanos cambien su campo de visión desde y hacia las imágenes y que los órganos reales queden bajo un campo quirúrgico oscurecido. Hacer incisiones bajo esas condiciones es altamente estresante.
Para abordar esos problemas, los autores de este trabajo presentan un nuevo dispositivo de imágenes, el sistema de proyección de imágenes médicas (MIPS [Medical Imaging Projection System]), que usa la señal de emisión de VIC y el mapeo de proyección activa.
El MIPS permite a los cirujanos determinar un plano seguro de corte y la dirección apropiada para la disección durante la hepatectomía anatómica, brindando – en consecuencia – una opción para la navegación en tiempo real para la cirugía del hígado.
| Métodos |
> Pacientes
Entre septiembre de 2014 y septiembre de 2015, 52 pacientes fueron sometidos a hepatectomía anatómica en el Hospital Universitario de Kyoto. Se obtuvo el consentimiento informado de todos los pacientes para emplear el MIPS, independientemente del tipo de cáncer y del procedimiento quirúrgico, siempre que el dispositivo estuviera disponible.
Finalmente, se realizaron 23 procedimientos de hepatectomía anatómica bajo guía del MIPS y 29 casos sin la misma. Los autores llevaron a cabo un análisis retrospectivo de los registros médicos para comparar los resultados entre los pacientes sometidos a hepatectomía con y sin MIPS.
El protocolo del estudio fue aprobado por el comité de ética de la Escuela de Medicina de Postgrado de la Universidad de Kyoto (códigos de aprobación: C857 y R955). El estudio fue registrado en la University Hospital Medical Information Network (número único de ensayo: UMIN000014998).
> Evaluación preoperatoria de los procedimientos quirúrgicos
Las imágenes en tres dimensiones (3D) del hígado fueron creadas utilizando el programa SYNAPS VINCENT (Fujifilm Medical Co Ltd, Tokio, Japón), basadas en imágenes preoperatorias tomografía computada (TC). La proporción del volumen del remanente parenquimatoso después de la remoción de los segmentos portadores de cáncer, se estimó de las imágenes reconstruidas en 3D.
Se procedió con la hepatectomía anatómica para el tratamiento de los tumores del hígado cuando la proporción del volumen del remanente hepático con el volumen total del hígado cumplía con el criterio para la resección.
Ese criterio es determinado usando el índice preoperatorio Krem del VIC (VICK-rem) calculado multiplicando la tasa de desaparición del VIC por la relación entre el volumen remanente del hígado y el volumen total del hígado [5]. El procedimiento quirúrgico fue determinado basado en las Guías de Resección Hepática de la International Hepato-Pancreato-Biliary Association [6].
> Administración del verde de indocianina
Para brindar una fuente de fluorescencia, se inyectaron 0,25 mg de VIC (2,5 mg/mL Diagnogreen: Daiichi Sankyo Co, Tokio, Japón), ya sea intravenosamente, después de pinzar las vainas glissonianas que fluyen hacia los segmentos hepáticos portadores de cáncer, o directamente en las ramas portales que suministran sangre a los segmentos portadores de cáncer, después de punzar en esos segmentos bajo guía ecográfica.
El VIC se administró justo antes de la disección parenquimatosa, pero después de la movilización del hígado y de la colocación necesaria de cintas en la envoltura glissoniana.
> Sistema de imágenes fluorescentes
El MIPS fue desarrollado en colaboración con Panasonic AVC Networks Company (Osaka, Japón) e incluye un cabezal de proyección y una barra (Fig. 1A). El cabezal de proyección utiliza un medio espejo para que coincida con el eje óptico de la cámara y el proyector, y se usa durante el procedimiento para obtener la localización del colorante y ajustar la proyección de la imagen para la guía en tiempo real, independientemente de los cambios y la deformación del órgano.
La diferencia entre la ubicación del órgano real y la imagen proyectada está dentro de 1 mm, estando el desfasaje entre la emisión del VIC fluorescente en el hígado y la imagen proyectada dentro de los 100 ms. El cabezal de proyección está diseñado para ser colocado aproximadamente a 100 cm por encima del campo operatorio y no ser sostenido por el cirujano (Fig. 1B).
Los umbrales de detección para el MIPS pueden ser seleccionados basado en el modo de intensidad de fluorescencia de varios pasos (mapas de calor), o pueden ser seleccionados manualmente. Asimismo, el diseño óptico, combinando un medio espejo y un filtro óptico, detecta selectivamente la emisión de VIC, removiendo el MIPS la interferencia de luz blanca de las imágenes proyectadas.
El algoritmo convierte subsecuentemente la fluorescencia emitida y los tejidos no emisores, en colores específicos y en blanco, respectivamente, diferenciando – por lo tanto – áreas proyectadas y no proyectadas de la región seleccionada. Esa diferenciación permite un campo quirúrgico bien iluminado sin requerir el uso de una lámpara sin sombras (Fig. 1C).
El sistema es también personalizable, permitiendo a los cirujanos seleccionar un color preferido para identificar el tejido orgánico real. La configuración de los MIPS dentro del campo operatorio requiere sólo unos minutos. Se ha obtenido una patente para este sistema por parte de la Japan Patent Office (número único: PCT/JP2015/004946). Este dispositivo no ha sido aprobado aún por la FDA y está todavía en investigación.
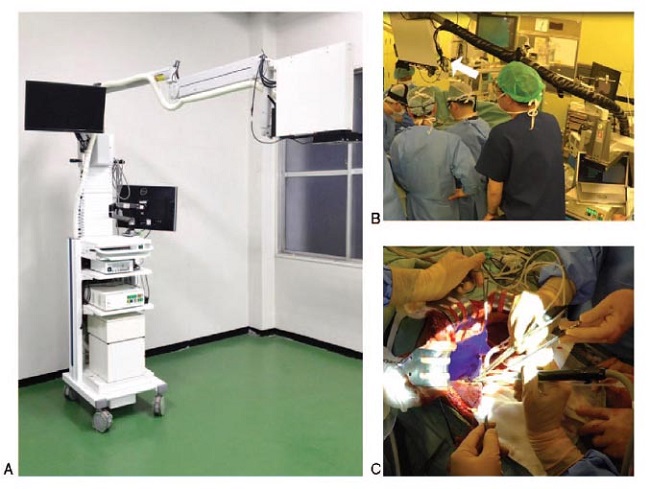 FIGURA 1: El MIPS: un nuevo dispositivo de imágenes fluorescentes utilizando mapeo de proyección. (A) una visión del MIPS, mostrando el cabezal de proyección y los componentes de la barra. (B) visión intraoperatoria utilizando el MIPS. El cabezal de proyección (flecha blanca) está localizado a aproximadamente 100 cm por encima del campo quirúrgico. (C) El campo operatorio está bien iluminado sin necesidad de emplear una lámpara sin sombras.
FIGURA 1: El MIPS: un nuevo dispositivo de imágenes fluorescentes utilizando mapeo de proyección. (A) una visión del MIPS, mostrando el cabezal de proyección y los componentes de la barra. (B) visión intraoperatoria utilizando el MIPS. El cabezal de proyección (flecha blanca) está localizado a aproximadamente 100 cm por encima del campo quirúrgico. (C) El campo operatorio está bien iluminado sin necesidad de emplear una lámpara sin sombras.
> Análisis clínico
Se evaluó la factibilidad y seguridad del uso del MIPS realizando un análisis retrospectivo de las características perioperatorias y de los resultados operatorios y postoperatorios de los pacientes sometidos a hepatectomía anatómica, con y sin el uso del sistema MIPS (grupo MIPS y grupo no-MIPS, respectivamente). Para el análisis, las líneas de demarcación claramente proyectadas en imágenes MIPS correspondieron, morfológicamente, a las líneas observables en las imágenes 3D preoperatorias.
> Análisis estadístico
Todos los análisis estadísticos fueron realizados utilizando el programa SAS (JMP 12.0.1; SAS Institute Inc, Cary, NC). Las variables continuas fueron expresadas como valores medios ± desvío estándar, y comparadas utilizando la prueba t de Student entre los grupos MIPS y no-MIPS.
Las diferencias entre grupos en las variables categóricas fueron evaluadas usando la prueba de c2 o la exacta de Fisher, según correspondiera para el conjunto de datos. Las tasas de sobrevida fueron calculadas utilizando el método de Kaplan-Meier y la prueba de log-rank. Los valores de P menores a 0,05 fueron considerados como significativos.
| Resultados |
No hubo diferencias significativas en las características preoperatorias entre los grupos, excepto para el tipo y estadio de la progresión del cáncer. El tiempo operatorio y el volumen de la pérdida de sangre fueron comparables entre los grupos.
Las líneas de demarcación fueron claramente proyectadas por el MIPS en 21 pacientes, pero no fueron detectables en 2 pacientes. Aunque la sección parenquimatosa fue realizada siguiendo la imagen proyectada por el MIPS en sólo 5 casos, la correspondencia entre las líneas de límite detectadas por el MIPS del parénquima hepático profundo, con aquellas identificadas en las imágenes preoperatorias, fue confirmada en todos los casos.
Postoperatoriamente, la tasa de morbilidad fue comparable entre los 2 grupos. La tasa de sobrevida libre de enfermedad a 1 año, sin embargo, fue más alta entre los pacientes del grupo MIPS que en los pacientes del grupo no-MIPS, aunque esa diferencia no fue estadísticamente significativa.
Se presentan a manera de ejemplo 3 casos con características específicas de los pacientes.
> Paciente 1
El tumor más grande fue identificado en el segmento hepático IV en la TC preoperatoria (Fig. 2A). Basado en las imágenes de reconstrucción 3D preoperatorias (Fig. 2B) se planificó una hepatectomía izquierda extendida y una resección parcial del segmento VIII. Intraoperatoriamente, la rama de la vaina glissoniana izquierda fue encintada y el flujo sanguíneo bloqueado pinzando la vaina. La línea de demarcación de la región isquémica fue identificada mediante visión directa (Fig. 2C).
Se inyectó el VIC intravenosamente y se obtuvieron las imágenes fluorescentes, utilizando el sistema convencional (Fig. 2D), proyectándoselas sobre la superficie del hígado mediante el MIPS (Fig. 2E). La línea de disección para asegurar el margen del tumor en el segmento IV fue determinada basado en la imagen preoperatoria y la ecografía intraoperatoria. La línea de corte cruzó el área coloreada y las 2 superficies de corte fueron coloreadas debido a la hepatectomía izquierda extendida y la resección parcial del segmento VIII requerida (Fig. 2F).
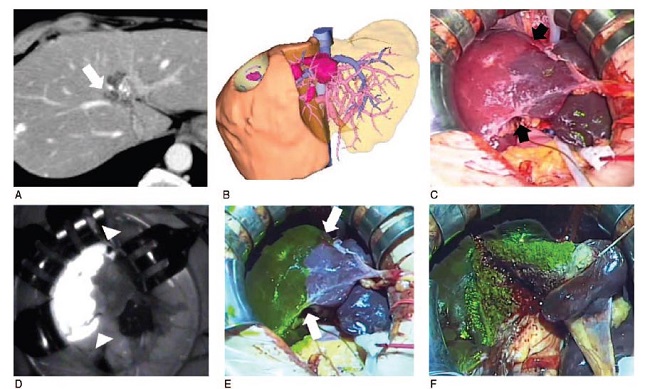 FIGURA 2: Hepatectomía izquierda extendida realizada por metástasis hepáticas múltiples en un paciente con cáncer de colon, utilizando el sistema MIPS. (A) la TC preoperatoria reveló que el tumor más grande (4 mm de diámetro) estaba localizado en el segmento IV del hígado (flecha blanca). (B) imagen preoperatoria en 3D basada en la imagen de la TC. Se efectuó una hepatectomía izquierda extendida y una resección parcial del segmento VIII. (C) la línea de demarcación fue identificada por visualización directa de la región isquémica después de pinzar la rama de la vaina glissoniana izquierda (entre las 2 flechas negras). (D) la línea de demarcación fue identificada sobre el monitor con el sistema convencional después de la inyección intravenosa del VIC (entre las 2 flechas blancas). La línea de demarcación es la misma observada en (C). (E) la línea de demarcación fue proyectada sobre la superficie del hígado con el sistema MIPS después de la inyección intravenosa de VIC (entre las 2 flechas blancas). La línea de demarcación es la misma observada en (C) y (D). (F) Imágenes proyectadas por el MIPS durante la disección parenquimatosa de una hepatectomía izquierda extendida, con la línea de corte cruzando el área coloreada para asegurar el margen del tumor en el segmento IV. Ambas superficie de corte fueron coloreadas.
FIGURA 2: Hepatectomía izquierda extendida realizada por metástasis hepáticas múltiples en un paciente con cáncer de colon, utilizando el sistema MIPS. (A) la TC preoperatoria reveló que el tumor más grande (4 mm de diámetro) estaba localizado en el segmento IV del hígado (flecha blanca). (B) imagen preoperatoria en 3D basada en la imagen de la TC. Se efectuó una hepatectomía izquierda extendida y una resección parcial del segmento VIII. (C) la línea de demarcación fue identificada por visualización directa de la región isquémica después de pinzar la rama de la vaina glissoniana izquierda (entre las 2 flechas negras). (D) la línea de demarcación fue identificada sobre el monitor con el sistema convencional después de la inyección intravenosa del VIC (entre las 2 flechas blancas). La línea de demarcación es la misma observada en (C). (E) la línea de demarcación fue proyectada sobre la superficie del hígado con el sistema MIPS después de la inyección intravenosa de VIC (entre las 2 flechas blancas). La línea de demarcación es la misma observada en (C) y (D). (F) Imágenes proyectadas por el MIPS durante la disección parenquimatosa de una hepatectomía izquierda extendida, con la línea de corte cruzando el área coloreada para asegurar el margen del tumor en el segmento IV. Ambas superficie de corte fueron coloreadas.
> Paciente 2
La TC preoperatoria localizó el tumor en el segmento V del hígado (Fig. 3A). Basado en las imágenes en 3D preoperatorias (Fig. 3B) se planificó una segmentectomía anterior derecha anatómica. Intraoperatoriamente, el tumor fue expuesto sobre la superficie del segmento V y el área ocupada por el tumor fue proyectada utilizando el sistema MIPS (Fig. 3C).
No se requirió inyección de VIC debido a la persistencia del VIC alrededor del tumor, proveniente de la prueba preoperatoria. Una de las ramas anteriores de la vena porta fue identificada con ecografía y la vaina fue punzada utilizando una aguja 23-G para la inyección intraportal del VIC. Se obtuvieron las imágenes fluorescentes usando el sistema convencional (Fig. 3D) y se proyectaron sobre la superficie del hígado mediante el MIPS (Fig. 3E).
Las imágenes fluorescentes incluyeron el área expuesta del tumor y el área comprometida identificada por la señal del VIC. La línea de disección fue determinada con base en las imágenes de referencia del segmento VIII, correspondiendo el límite entre el área coloreada y la no coloreada a la línea de sección en las imágenes 3D preoperatorias (Fig. 3F). Para el tratamiento, se realizó una segmentectomía anterior derecha.
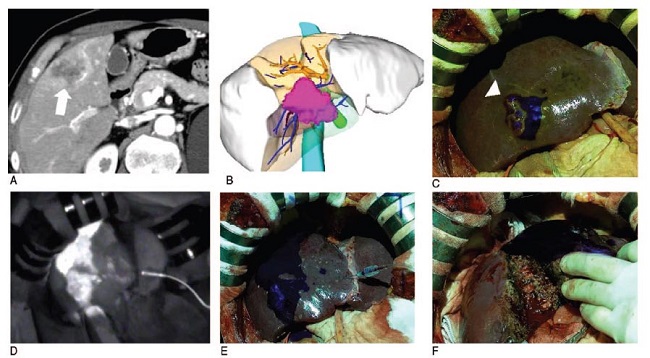 FIGURA 3: Segmentectomía anterior derecha para el tratamiento de un carcinoma hepatocelular utilizando el sistema MIPS. (A) la TC reveló que el tumor (30 mm de diámetro) estaba localizado en el segmento V del hígado (flecha blanca). (B) imagen preoperatoria en 3D basada en la imagen de la TC. Se realizó una segmentectomía anterior derecha. (C) Imagen proyectada usando el MIPS antes de la inyección del VIC, mostrando excreción biliar desordenada del VIC en el tumor, a causa del VIC usado preoperatoriamente (punta de flecha blanca). (D) la línea de demarcación fue identificada sobre el monitor con el sistema convencional después de punzar la rama seleccionada de la vena porta y la inyección intraportal del VIC. (E) la línea de demarcación fue proyectada sobre la superficie del hígado utilizando el MIPS después de la punción de la rama seleccionada de la vena porta y la administración intraportal, mediante inyección, del VIC. (F) imagen proyectada por el MIPS durante la disección parenquimatosa del segmento para una segmentectomía anterior derecha
FIGURA 3: Segmentectomía anterior derecha para el tratamiento de un carcinoma hepatocelular utilizando el sistema MIPS. (A) la TC reveló que el tumor (30 mm de diámetro) estaba localizado en el segmento V del hígado (flecha blanca). (B) imagen preoperatoria en 3D basada en la imagen de la TC. Se realizó una segmentectomía anterior derecha. (C) Imagen proyectada usando el MIPS antes de la inyección del VIC, mostrando excreción biliar desordenada del VIC en el tumor, a causa del VIC usado preoperatoriamente (punta de flecha blanca). (D) la línea de demarcación fue identificada sobre el monitor con el sistema convencional después de punzar la rama seleccionada de la vena porta y la inyección intraportal del VIC. (E) la línea de demarcación fue proyectada sobre la superficie del hígado utilizando el MIPS después de la punción de la rama seleccionada de la vena porta y la administración intraportal, mediante inyección, del VIC. (F) imagen proyectada por el MIPS durante la disección parenquimatosa del segmento para una segmentectomía anterior derecha
> Paciente 3
La imagen en la TC preoperatoria identificó un tumor localizado en el segmento VII del hígado (Fig. 4A). Basado en las imágenes en 3D preoperatorias (Fig. 4B) se planificó una segmentectomía posterior derecha anatómica. Intraoperatoriamente, la rama de la vaina glissoniana posterior derecha fue encintada y el flujo sanguíneo se bloqueó mediante el pinzamiento de la vaina.
La línea de demarcación sobre la superficie del hígado fue reconocible visualmente (Fig. 4C), particularmente sobre el lecho vesicular (Fig. 4D). Se inyectó intravenosamente el VIC y se obtuvieron imágenes fluorescentes usando el sistema convencional (Fig. 4E), que se proyectaron sobre la superficie del hígado con el MIPS. La imagen proyectada siguió suavemente el movimiento y la deformación del hígado y se realizó una segmentectomía posterior derecha siguiendo la imagen proyectada por el MIPS durante la disección parenquimatosa.
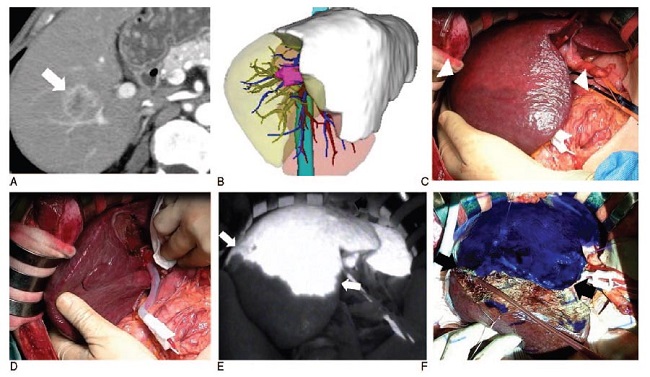 FIGURA 4: Segmentectomía posterior derecha anatómica para el tratamiento de un paciente con un carcinoma hepatocelular usando el sistema MIPS. (A) la TC preoperatoria reveló que el tumor (30 mm de diámetro) estaba localizado en el segmento VII del hígado (flecha blanca). (B) imágenes en 3D preoperatorias basadas en la TC. Se realizó una segmentectomía posterior derecha anatómica. (C) la línea de demarcación no fue identificada claramente con la visión directa para la región isquémica después de pinzar la rama derecha posterior de la vaina glissoniana (entre las 2 puntas de flecha blancas). (D) la línea de demarcación del lecho vesicular no fue identificada por la visión directa de la región isquémica después del pinzamiento. (E) la línea de demarcación fue identificada sobre el monitor con el sistema convencional después de la inyección intravenosa del VIC (entre las 2 flechas blancas). (F) resultados de la disección parenquimatosa durante una segmentectomía posterior derecha anatómica usando el sistema MIPS. El área proyectada del hígado resecado durante la disección parenquimatosa debería haberse preservado. Se pensó que la línea de disección era el límite entre el área coloreada y no coloreada (entre 2 flechas negras)
FIGURA 4: Segmentectomía posterior derecha anatómica para el tratamiento de un paciente con un carcinoma hepatocelular usando el sistema MIPS. (A) la TC preoperatoria reveló que el tumor (30 mm de diámetro) estaba localizado en el segmento VII del hígado (flecha blanca). (B) imágenes en 3D preoperatorias basadas en la TC. Se realizó una segmentectomía posterior derecha anatómica. (C) la línea de demarcación no fue identificada claramente con la visión directa para la región isquémica después de pinzar la rama derecha posterior de la vaina glissoniana (entre las 2 puntas de flecha blancas). (D) la línea de demarcación del lecho vesicular no fue identificada por la visión directa de la región isquémica después del pinzamiento. (E) la línea de demarcación fue identificada sobre el monitor con el sistema convencional después de la inyección intravenosa del VIC (entre las 2 flechas blancas). (F) resultados de la disección parenquimatosa durante una segmentectomía posterior derecha anatómica usando el sistema MIPS. El área proyectada del hígado resecado durante la disección parenquimatosa debería haberse preservado. Se pensó que la línea de disección era el límite entre el área coloreada y no coloreada (entre 2 flechas negras)
| Discusión |
La resección hepática ofrece el mayor potencial para el tratamiento curativo de los pacientes con cáncer de hígado, brindando el trasplante hepático y la ablación por radiofrecuencia opciones adicionales, dependiendo del tamaño y localización del tumor y del estadio de progresión de la enfermedad [1,7].
No obstante, aun cirujanos experimentados deben manejar dificultades técnicas significativas durante la hepatectomía, donde un ligero error que conlleva el riesgo de complicaciones graves, incluyendo hemorragia masiva y falla hepática. El sistema de base de datos clínicos nacionales de Japón reportó un riesgo de mortalidad relacionada con la hepatectomía del 4% [8].
La resección anatómica de los territorios portales portadores de cáncer es un procedimiento razonable para el tratamiento del carcinoma hepatocelular y para algunos pacientes con cáncer metastásico en el hígado [3,9]. Este procedimiento requiere identificación precisa del plano intersegmentario, que no siempre es neto. [10]
Se usan generalmente dos abordajes para identificar la línea de demarcación del área tumoral. El primer abordaje involucra la punción quirúrgica de las ramas portales que irrigan los segmentos hepáticos portadores de cáncer, bajo guía ecográfica intraoperatoria, confirmando la superficie hepática mediante la inyección de colorante (carmín de índigo o azul de metileno) [11,12].
Aunque el carmín de índigo aumenta la detección de los segmentos hepáticos, como un punto de referencia para la disección parenquimatosa, su efectividad en general es limitada [13].
En el segundo abordaje, los cirujanos aíslan y encintan las vainas glissonianas que fluyen a los segmentos hepáticos portadores de cáncer, seguido por el pinzamiento de las mismas para bloquear el flujo de sangre, con la subsiguiente determinación de la línea de demarcación de las regiones isquémicas sobre la superficie del hígado [3,14].
Los cirujanos pueden entonces determinar la línea de corte basados en la línea de demarcación y la localización de las venas hepáticas principales. No obstante, la línea de demarcación no es identificable bajo visión directa en casos de cirrosis o adherencias severas [13,15].
Aunque la imagen del hígado simulada en 3D, basada en las imágenes preoperatorias de TC, ha progresado con los años [16-18], el hígado se puede mover libremente y cambiar su forma durante la cirugía, haciendo difícil la identificación precisa de la anatomía interna de los sitios con tumor o de los vasos, basado en imágenes estáticas.
Más recientemente, la impresión 3D se ha utilizado para crear un modelo transparente del hígado, que puede ser usado como referencia dentro del campo operatorio [19,20]. Ese abordaje estático, sin embargo, todavía no tiene en cuenta el movimiento intraoperatorio o la deformación del hígado.
La navegación quirúrgica molecular, empleando marcadores con fluorescencia para identificar el tejido tumoral usando seudocolores contrastantes, ha sido desarrollada [21]. En particular, la imagen fluorescente utilizando VIC y un sistema de cámara cercana al infrarrojo, han sido adoptados mundialmente, con investigación de apoyo [4].
Como el espectro de excitación y la longitud de onda máxima de la señal de emisión del VIC se encuentran dentro del rango de absorbancia de hemoglobina y agua [22,23], la imagen con VIC puede detectar tumores pequeños del hígado y de los conductos biliares [24,25].
Por otro lado, la imagen fluorescente obtenida mediante la inyección de VIC en la rama portal o en la vena periférica, puede ser usada para la identificación intraoperatoria de los segmentos hepáticos [26,27]. El MIPS extiende la técnica del VIC, combinando la imagen emitida por el VIC con un mapeo de proyección activa, sin el requisito de uso de gafas especiales o pantallas de computadora.
El MIPS es superior a los sistemas por imágenes convencionales por las siguientes razones: los cirujanos pueden concentrarse sobre el campo quirúrgico, sin tener que cambiar su visión hacia otros componentes, para visualizar el área de interés.
La calidad de la imagen no está influenciada por la contaminación generada por el movimiento de los dispositivos sostenidos con la mano; el oscurecimiento el campo operatorio para evitar la contaminación por la luz blanca es eliminado; y es posible una proyección precisa en tiempo real que permite seguir el movimiento y la deformación del hígado para mantener la precisión
En el paciente 1, el VIC se distribuyó en el área de preservación y la línea de demarcación fue claramente proyectada (Fig. 2E), y se identificó el límite correspondiente bajo visualización directa después de pinzar la vaina glissoniana (Fig. 2C).
En el paciente 2, el VIC se distribuyó más difusamente dentro del área seleccionada para resección, con dificultad para punzar eficazmente las ramas más pequeñas de la vena porta, identificadas en las imágenes preoperatorias en 3D como brindando la irrigación principal al segmento hepático V. En ese caso, se identificó la línea de demarcación utilizando tanto la imagen de MIPS proyectada sobre el hígado, como las imágenes de referencia preoperatorias en 3D del segmento V.
En el paciente 3, el límite proyectado por el MIPS fue más claramente visible que la línea de demarcación identificada por visualización directa, particularmente sobre el lecho vesicular, realizándose la segmentectomía derecha posterior anatómica, rastreando la imagen fluorescente proyectada que diferenciaba los segmentos hepáticos (Fig. 4E).
Dado que la imagen del MIPS se proyecta directamente sobre la superficie de corte, la línea de disección – correspondiente al límite entre las áreas coloreadas y no coloreadas – correspondía al plano intersegmentario y fue concordante incluso en las regiones profundas del hígado.
Aunque el MIPS se usó sólo en pocos casos para la sección parenquimatosa en la parte profunda del hígado, se halló que la imagen del MIPS era muy útil en esos casos. El plano coloreado puede ser usado también para identificar errores, como extender la línea de corte en los tejidos no isquémicos.
La sección del parénquima hepático a lo largo de todo el límite mostrado por el MIPS, permitiría a los cirujanos realizar la hepatectomía anatómica, ya que la línea de corte se identifica utilizando el momento adecuado y la ruta de inyección del VIC fluorescente, después de la ligadura venosa portal.
La línea de demarcación no pudo ser identificada usando el MIPS en 2 casos. En un caso, se debió al error en la identificación de la vaina glissoniana portadora de cáncer bajo guía ecográfica intraoperatoria, que requiere experiencia.
En el otro caso, la línea de demarcación no pudo ser detectada porque el procedimiento involucró la ligadura de la vaina glissoniana originada en la rama de la vaina glissoniana izquierda. Los pacientes en los que el cirujano puede aislar el flujo de las vainas glissonianas a los segmentos hepáticos portadores de cáncer, son más adecuados para el uso del MIPS.
De la experiencia de los autores surge que el modo de establecer el umbral de la imagen fue eficaz para corregir los efectos de un tiempo de tinción más corto y una menor concentración del VIC, para la inyección del mismo por vía intravenosa en lugar de intraportal [27]. La configuración de una alta sensibilidad de detección permitió el descubrimiento de la línea de demarcación en pacientes con cirrosis hepática, en los cuales la línea no era clara bajo la luz blanca.
De hecho, la línea de demarcación del MIPS fue claramente proyectada en el paciente 1, con un puntaje B de Child-Pugh para cirrosis hepática. Los niveles de los índices VICR15 (tasa de retención del VIC a los 15 minutos) y VICK-rem estuvieron dentro de límites normales en los 2 casos en los que el MIPS no proyectó una línea clara de demarcación, por lo que se requiere más investigación para clarificar los efectos del puntaje Child-Pugh sobre la visibilidad anatómica brindada por el MIPS.
El principal beneficio clínico del MIPS es la proyección continua que brinda para guiar la sección en la parte profunda del parénquima hepático, que no es posible con la técnica convencional por imágenes, debido al cambio de enfoque visual, imagen borrosa a causa del temblor de las manos, y baja visibilidad por el oscurecimiento requerido para el campo operatorio. Asimismo, la navegación del MIPS en tiempo real corrige los movimientos y deformación del órgano durante la cirugía, para asegurar una precisión consistente de la imagen proyectada.
Es importante el desarrollo de sistemas de navegación en tiempo real confiables y precisos, tales como el MIPS, particularmente en vista del reciente aumento en el uso de la laparoscopía para la resección hepática. Los nuevos dispositivos con integración de las imágenes VIC con el sistema laparoscópico [28,29], tienen un gran potencial para ser ampliamente aceptados en un futuro temprano.
Basado en su experiencia, los autores de este trabajo proponen que el MIPS debería ser utilizado aun cuando estuvieran disponibles otras técnicas, incluyendo imágenes de simulación 3D del hígado basadas en TC preoperatorias y ecografía intraoperatoria.
La no aclaración del VIC inyectado preoperatoriamente para evaluar la función del hígado alrededor del tumor, puede causar confusión de la línea de proyección correcta, como en el paciente 2 de la serie de casos de los autores. También se requiere atención en los casos en los que el tumor se ubica cercano a la línea de corte, requiriendo el uso de simulación 3D basada en las imágenes de TC preoperatorias y ecografía intraoperatoria.
El ácido 5-aminolevulínico, un material fluorescente usado recientemente para la detección de tumores hepáticos [30] y el VIC, utilizados en una técnica de doble trazador, podría mejorar aún más el límite entre el tumor y la línea de corte.
En conclusión, el MIPS brinda una identificación confiable de los puntos de referencia para la disección parenquimatosa, mediante la combinación de un mapeo de proyección activa, con imágenes guiadas por fluorescencia.
Se necesita mayor investigación para determinar completamente si el plano de resección proyectado por el MIPS es lo suficientemente preciso para una navegación en tiempo real. Un ensayo clínico comparando la precisión de la sección parenquimatosa entre la hepatectomía guiada por MIPS y la hepatectomía convencional está siendo llevado a cabo en la actualidad.
Comentario y resumen objetivo: Dr. Rodolfo D. Altrudi