|
Resumen La insuficiencia cardíaca es una enfermedad compleja, manifestación de diversas patologías cardíacas y no cardíacas. Los enfoques terapéuticos son los mismos desde hace décadas. Las tasas de rehospitalización siguen siendo altas y el pronóstico es malo. La creación e implementación de mejores algoritmos para evaluar y tratar a los pacientes con insuficiencia cardíaca durante la hospitalización continúan siendo necesarias. En este artículo se propone un algoritmo ampliado para el monitoreo y el tratamiento de los pacientes hospitalizados por insuficiencia cardíaca aguda descompensada a fin de mejorar los resultados pos alta y disminuir las tasas de rehospitalizaciones. |
| INTRODUCCIÓN |
La insuficiencia cardíaca (IC) no es una sola enfermedad, sino un síndrome heterogéneo que es la manifestación de diversas patologías cardíacas y no cardíacas. Se la observa por lo general en personas de 65 años o mayores y tiene altas tasas de morbimortalidad. La mortalidad y la tasa de reingreso de los pacientes hospitalizados por IC con reducción de la fracción de eyección (ICFEr) son de hasta el 15% y el 30%, respectivamente, a 60–90 días pos alta.
Estos valores no cambiaron en la última década a pesar de los nuevos tratamientos y modalidades de monitoreo. La hospitalización y las rehospitalizaciones son fuertes factores pronósticos de evolución negativa, como por ejemplo la mortalidad en los pacientes con IC. En este contexto, la creación e implementación de mejores algoritmos para evaluar y tratar a los pacientes con IC durante su hospitalización sigue siendo una necesidad no cubierta.
En este artículo los autores proponen y brindan fundamentos para el empleo del siguiente enfoque sistemático durante las tres fases de la hospitalización (evaluación inicial, hospitalización y pos alta):
(1) adoptar un marco reglamentado para evaluar y tratar la IC descompensada aguda,
(2) tratar más allá de la congestión clínica,
(3) ampliar el uso de tratamientos subempleados que mejoran los resultados,
(4) identificar y tratar las enfermedades simultáneas no cardíacas y
(5) hacer hincapié en la importancia de las visitas de seguimiento después del alta. El propósito es utilizar herramientas y estrategias para mejorar los resultados posteriores al alta y disminuir las tasas de rehospitalización.
| 1. ADOPTE UN ENFOQUE REGLAMENTADO PARA EVALUAR Y TRATAR LA IC DESCOMPENSADA AGUDA |
El enfoque terapéutico para la IC descompensada aguda (ICDA) en pacientes hospitalizados no cambió significativamente en las últimas décadas. El algoritmo terapéutico actual para la ICDA se centra en tratar los signos y síntomas de congestión con diuréticos y vasodilatadores. Además, hay otros numerosos factores a tener en cuenta durante las tres diferentes fases de la hospitalización.
Durante la fase inicial en el servicio de urgencias es razonable emplear un modelo de evaluación de seis ejes descrito por Gheorghiade et al. que determina si la IC es nueva o crónica, su gravedad, los factores precipitantes, la frecuencia y el ritmo cardíacos, la presión arterial y las enfermedades concomitantes. Esto puede orientar el triage y la iniciación de los tratamientos inmediatos necesarios que se efectuarán en el servicio de urgencias antes de la hospitalización.
Una vez hospitalizados los pacientes, los autores proponen una evaluación más exhaustiva con un nuevo modelo de ocho ejes que se muestra en la figura. Una vez hospitalizado el paciente, además de tratar la congestión, hay ocho entidades importantes, cardíacas y no cardíacas que contribuyen a la aparición y el empeoramiento de la ICFEr:
(1) enfermedad coronaria,
(2) hipertensión,
(3) miocardiopatía,
(4) enfermedad pericárdica,
(5) alteraciones eléctricas,
(6) valvulopatía,
(7) incumplimiento terapéutico,
(8) coexistencia de otras enfermedades (nefropatía, ferropenia, enfermedad pulmonar, diabetes).
Estas entidades son igualmente importantes en el tratamiento de las exacerbaciones de la ICFEr, como se indica en la figura. La determinación de la fracción de eyección (FE) es esencial durante la segunda fase de la hospitalización a fin de orientar la evaluación y los tratamientos, siendo ampliamente aceptadas las tres clases siguientes (1) ICFEr = 40%, (2) FE intermedia del 41 - 49%, (3) ICFEr = 50%.
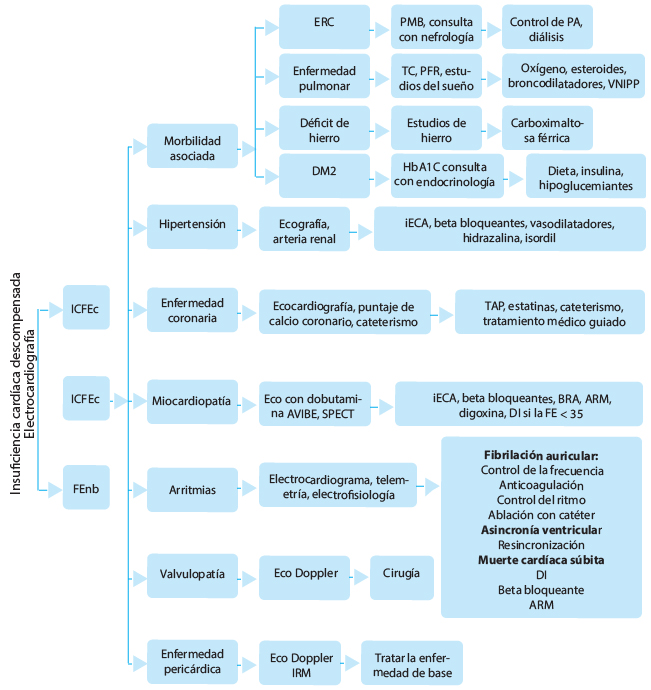
Figura. Algoritmo del enfoque terapéutico de la insuficiencia cardíaca.
ICFEc: insuficiencia cardíaca con fracción de eyección conservada; ICFEr: insuficiencia cardíaca con fracción de eyección reducida; FE: fracción de eyección; ERC: enfermedad renal crónica; PMB: panel metabólico básico; PA: presión arterial; TC: tomografía computada; PFR: pruebas de función respiratoria; VNIPP: ventilación no invasiva de presión positiva; iECA: inhibidor de la enzima convertidora de angiotensina; TAPD: tratamiento antiplaquetario dual; AVIBE: análisis de vector de impedancia bioeléctrico; BRA: bloqueantes de receptores de angiotensina; ARM: antagonista de los receptores mineralocorticoides; DI: desfibrilador implantable; ECG: electrocardiograma; MCS: muerte cardíaca súbita; IRM: imagen de resonancia magnética. Elaborado sobre el contenido del artículo de Njoroge et al.
Es necesario evaluar todos los posibles componentes para crear planes terapéuticos personalizados con múltiples blancos terapéuticos que puedan revertir la disfunción cardíaca
Una evaluación cardiovascular completa se puede lograr con otras modalidades de estudios por imágenes, entre ellas la ecocardiografía para determinar la función sistólica y diastólica y las valvulopatías, la resonancia magnética cardíaca para evaluar si hay enfermedad pericárdica (para los que no tienen un desfibrilador cardioversor implantable o un marcapasos permanente), tomografía computarizada por emisión de fotón único (SPECT por las siglas del inglés) para evaluar si hay miocardio viable y la ecografía de estrés con dobutamina para determinar la reserva contráctil.
En pacientes con ICFEr y miocardio disfuncional, pero viable, un sólido conjunto de evidencias avala la posibilidad de mejorar la función sistólica con la optimización del tratamiento orientado por las guías. Esto se demostró, por ejemplo en el estudio CHRISTMAS, donde los pacientes con ICFEr y miocardio viable determinado por SPECT aumentaron la FE cuando se los trataba con carvedilol. Hay asimismo relación entre el grado de viabilidad miocárdica y el porcentaje de mejoría en la FE.
Cada paciente con IC tiene grados variables de los trastornos mencionados, que contribuyen a su proceso patológico específico. Es necesario evaluar todos los posibles componentes para crear planes terapéuticos personalizados con múltiples blancos terapéuticos que puedan revertir la disfunción cardíaca.
| 2.TRATE MÁS ALLÁ DE LA CONGESTIÓN |
La congestión en la IC abarca los signos y síntomas conocidos de IC: disnea, ortopnea, rales y edema periférico. Mucho menos reconocida es la congestión hemodinámica, definida como el aumento de la presión diastólica del ventrículo izquierdo a pesar de evidencia mínima o ausente de IC clínica. El desarrollo de la congestión clínica y hemodinámica abarca un espectro de distinta gravedad; a medida que la congestión hemodinámica continúa progresando, los síntomas de congestión clínica comienzan a aparecer hasta varias semanas después.
Varios pacientes en este continuum refieren disnea, pero no tienen signos sistémicos. En un estudio de 50 pacientes, estos signos estuvieron ausentes en el 42% de los pacientes con congestión con aumento demostrado de la presión capilar pulmonar (PCP).
Muchos pacientes son dados de alta con mejoría de los síntomas, pero con alta presión de llenado del ventrículo izquierdo, ortopnea provocada y escasa capacidad de ejercicio. A continuación se mencionan otras herramientas y técnicas para aumentar la sensibilidad de la evaluación de la congestión persistente.
La fisiopatología detrás del desarrollo y el empeoramiento de la insuficiencia cardíaca es multifacética y, como tal se la debe evaluar más minuciosamente
> Escalas de medición de la disnea y la ortopnea
La disnea y la ortopnea son síntomas iniciales frecuentes que actúan como marcador subjetivo de la congestión en el paciente con ICDA.
En el hospital, la disnea evaluada por el médico y la referida por el paciente no se asociaron independientemente con la calidad de vida posterior al alta, la supervivencia o las rehospitalizaciones. Aunque el alivio de la disnea continúa siendo un objetivo terapéutico para los pacientes hospitalizados con ICFEr, esta medición quizás no sea un sustituto fiable para los resultados a largo plazo con el enfoque actual de evaluación.
La escala de Likert y el puntaje análogo visual son herramientas que reducen al mínimo la subjetividad cuando evalúan el grado de ortopnea o disnea. El empleo conjunto de ambas escalas aumenta la sensibilidad de la evaluación al medir múltiples aspectos específicos de la disnea. Estas herramientas objetivas comparan la congestión desde el ingreso hasta el alta para asegurar la mejoría
> Signos vitales ortostáticos
En personas con función cardíaca y volumen intravascular normales, la respuesta refleja a los cambios de posición desde la sedestación a la bipedestación incluye la disminución leve de la presión arterial y el aumento de la frecuencia cardíaca. En pacientes descompensados con congestión intravascular, estos cambios de posición pueden tener efectos paradójicos.
Los sarcómeros en los pacientes con IC congestiva inicialmente se estiran por demás, pero después se encogen dentro de límites ideales con disminución del retorno venoso y precarga resultante disminuida, mejorando la contractilidad.
Por lo tanto, la ortostasis puede producir aumento del gasto cardíaco y mejora de la presión arterial, que podrían indicar congestión intravascular que exige más diuresis. Esta herramienta es de utilidad limitada entre pacientes con miocardiopatía hipertrófica, estenosis aórtica o fibrilación auricular.
> Maniobra de Valsalva
En la persona con volumen intravascular normal, la respuesta a la maniobra de Valsalva sostenida es multifásica. Inmediatamente después de iniciar la maniobra, el aumento de la presión intratorácica causa un breve pico de la presión arterial, seguido por disminución del retorno venoso y aumento de la resistencia vascular sistémica, lo que provoca caída de la presión arterial por debajo de lo habitual.
Cuando el esfuerzo cesa, la disminución de la presión intratorácica causa otra caída tensional seguida por aumento del retorno venoso y disminución de la resistencia vascular (y por lo tanto, disminución de la poscarga) lo que permite el aumento rebote de la presión.
A la inversa, en los pacientes con congestión, el cese del esfuerzo produce el aumento persistente de la presión arterial debido al aumento de la presión diastólica del ventrículo izquierdo y el aumento persistente de las presiones centrales.
Esta maniobra tiene gran relación con las presiones de llenado ventricular medidas de manera invasiva y demuestra su utilidad para monitorear el estado del volumen intravascular.
La prueba de caminata de seis minutos es una herramienta sencilla para provocar síntomas de congestión que quizás no se hallen en reposo. Es estudio ESCAPE halló que esta prueba era uno de los factores pronósticos más fiables de mortalidad tras la hospitalización por empeoramiento de la IC junto con las mediciones de PCP. La prueba de caminata de seis minutos se puede emplear antes del alta y para el monitoreo continuado durante la tercera fase del seguimiento ambulatorio.
> Medición del péptido natriurético
La comparación entre los valores en sangre del NT-proBNP (por las siglas del inglés) al ingreso y antes del alta puede asegurar la correcta trayectoria terapéutica. El NT-proBNP es escindido del BNP, tiene más estabilidad in vivo, y mayor sensibilidad y especificidad que los valores circulantes de BNP. Se halló que los pacientes con NTproBNP persistentemente alto antes del alta tienen riesgo significativamente mayor de rehospitalización o muerte.
El monitoreo serial de los valores de NT-proBNP no es tan útil en el paciente hospitalizado debido a la demora en los cambios de los valores en relación con la progresión de la congestión intravascular. Sin embargo, la reducción de los valores de NT-proBNP en por lo menos el 30% desde el ingreso se asocia con mejores resultados posteriores al alta.
El monitoreo hemodinámico no invasor se puede emplear a través de las tres fases de la hospitalización por IC. La compresibilidad o la distensión de la vena cava inferior se puede evaluar fácilmente para distinguir entre la congestión sistémica y la redistribución de los líquidos.
Goonewardena et al. determinaron que la ecografía de Ia cava inferior a la cabecera del paciente identificaba a los pacientes con ICDA que serían rehospitalizados por empeoramientos de la IC basados sobre venas cavas inferiores pletóricas con índices menores de colapsibilidad.
El empleo de la impedancia bioeléctrica transtorácica como marcador de la acumulación de líquido aún está ganando terreno, pero se demostró que es fiable para medir el gasto cardíaco y el índice cardíaco cuando se la comparó con los métodos invasivos.
| 3.AUMENTE EL EMPLEO DE TRATAMIENTOS POCO UTILIZADOS, QUE SE HA DEMOSTRADO QUE DISMINUYEN LAS REHOSPITALIZACIONES |
A pesar del conjunto importante de datos que apoyan las recomendaciones de diversas instituciones, como el American College of Cardiology (ACC), la American Heart Association (AHA) y la European Society of Cardiology (ESC) para la ICFEr, persisten vacíos significativos en la provisión de tratamientos recomendados a pacientes con indicaciones para ellos.
Esto quizás se origine por pensar solo en la posible desestabilización clínica a corto plazo en lugar de considerar los posibles beneficios alejados del tratamiento. Por ejemplo, evidencia sólida sugiere que el empeoramiento de la función renal al aumentar el tratamiento descongestivo o iniciar el bloqueo del sistema renina–angiotensina–aldosterona no perjudica el pronóstico, sino que representa un beneficio neto para el paciente.
No obstante, con frecuencia se suspenden los inhibidores de la enzima convertidora de angiotensina iECA y los bloqueantes del receptor de angiotensina (BRA) sin reiniciarlos antes del alta. A continuación se verán ejemplos de tratamientos en pacientes con ICFEr que se deben tener en cuenta para iniciarlos antes del alta o durante el seguimiento a fin de promover la reversibilidad de la disfunción cardíaca.
La digoxina tiene beneficios hemodinámicos comprobados y se asocia con menores tasas de reingreso. Es respaldada por las recomendaciones para su empleo en pacientes apropiados con síntomas persistentes y rehospitalizaciones por ICFEr. Sin embargo, su prescripción disminuyó durante la última década.
El estudio DIG demostró que la digoxina, agregada a los diuréticos y los iECA en pacientes con ICFEr crónica, con ritmo sinusal, disminuyó las hospitalizaciones sin afectar la mortalidad. Este efecto neutral sobre la mortalidad en un gran estudio aleatorizado es notable en medio de preocupaciones persistentes sobre la seguridad de la digoxina.
Este efecto de la digoxina se observó a pesar que el protocolo del estudio invitaba a su administración intensiva a fin de lograr concentraciones en sangre superiores a las de las recomendaciones actuales. La evidencia sugiere que las dosis según lo aconsejado por ACC/AHA mejoran más aún el índice riesgo-beneficio del tratamiento con digoxina.
> Antagonistas del receptor de mineralocorticoides
Menos del 33% de los pacientes idóneos hospitalizados por IC reciben antagonistas del receptor de mineralocorticoides (ARMC) antes del alta a pesar de datos que indican que reducen significativamente la tasa de hospitalización temprana.
Además de bloquear el efecto de la aldosterona sobre los ARMC pueden prevenir que la aldosterona favorezca la fibrosis de los cardiomiocitos, la lesión oxidativa y el remodelado cardíaco. En dosis mayores, los ARMC también pueden proporcionar beneficios natriuréticos y se los empleó para este fin durante años en pacientes cirróticos.
> Torsemida
Los tres diuréticos del asa más empleados son furosemida, bumetanida y torsemida. Aunque aún no hay datos definitivos sobre los resultados clínicos, evidencia convincente apoya a la torsemida debido a sus claras ventajas sobre los otros diuréticos del asa.
La torsemida tiene una biodisponibilidad significativamente mejor, independiente de la presencia de edema intestinal o disfunción renal. En relación con la biodisponibilidad variable de la furosemida, del 10 - 90% según el estado de la enfermedad, la biodisponibilidad de la torsemida es del 80%. Otra ventaja es su mayor duración de acción (12–18 hs) en relación con la furosemida y la bumetanida (6 - 8 hs) y su menor tendencia a la hipopotasiemia.
> Diuréticos tiacídicos
Los pacientes que necesitan el empleo crónico de diuréticos pueden desarrollar con frecuencia tolerancia a los diuréticos del asa debido a hipertrofia del segmento distal del nefrón y aumento de la reabsorción de sodio proximal al lugar de acción del diurético.
Los diuréticos tiacídicos pueden ser importantes para potenciar los efectos de la excreción de sodio de los diuréticos del asa en estos pacientes. Al actuar sobre los túbulos distales, las tiacidas proporcionan un efecto sinérgico al combinarse con los diuréticos del asa y prevenir la reabsorción de sodio y agua en la rama ascendente del asa de Henle y los túbulos contorneados distales.
> La ivabradina es un agente cronotrópico que disminuye la frecuencia cardíaca y por lo tanto el trabajo cardíaco. Se mostró su utilidad en una cohorte específica de pacientes con IC crónica con FE < 35% y frecuencia cardíaca > 70 por minuto, donde disminuyó la tasa de hospitalizaciones y la muerte debidas a IC. Se debe considerar su iniciación en la fase posterior al alta entre pacientes con ICFEr que ya reciben dosis óptimas del tratamiento médico orientado por las guías. En el paciente estable con IC que ingresó por descompensación aguda se la debe comenzar antes del alta.
> Los inhibidores del receptor de angiotensina y la neprilisina (IRAN) mejoran la vasodilatación y la natriuresis al inhibir la endotelina, la vasopresina, la actividad simpática y el sistema renina angiotensina aldosterona.
El estudio PARADIGM-HF demostró mejores resultados en la ICFEr con el tratamiento con IRAN que con iECA. El análisis post hoc de este estudio sugiere que estos beneficios se extienden y mejoran los resultados clínicos tras la hospitalización por IC y se debe considerar iniciar su administración durante las visitas como paciente ambulatorio.
> Ultrafiltración
Se conoce bien la interdependencia de las funciones renales y cardíacas, donde la disfunción de un órgano con frecuencia afecta al otro. El equilibrio entre la descongestión cardíaca y la función renal es una lucha que los médicos enfrentan a menudo cuando tratan pacientes con IC aguda descompensada. La ultrafiltración ofrece una opción para una mayor descongestión de los pacientes con IC y disfunción renal, si bien los datos actuales sobre el riesgo-beneficio no son concluyentes.
Otro estudio (Cardiorenal Rescue Study in Acute Decompensated Heart Failure, CARRESS-HF) examinó los efectos de la ultrafiltración para la eliminación continua de líquido en presencia de insuficiencia que empeora, pero demostró aumento de la asociación con más episodios adversos, empeoramiento de la función renal y ninguna diferencia significativa en los resultados.
Por su parte, en el estudio AVOID-HF (Aquapheresis Versus Intravenous Diuretics and Hospitalizations for Heart Failure) no se observó diferencia en los efectos adversos entre los grupos tratados con ultrafiltración y los que recibieron diuréticos del asa.
También es importante que hubiera mayor duración entre el episodio inicial de IC y los episodios siguientes dentro de los 90 días en el grupo con ultrafiltración que en el que recibió diuréticos. Este estudio se finalizó precozmente por motivos de financiación, pero es un incentivo para continuar evaluando su validez como parte de una estrategia empírica para la congestión resistente al tratamiento farmacológico intensivo.
| 4. IDENTIFIQUE Y TRATE LAS ENFERMEDADES SIMULTÁNEAS NO CARDÍACAS |
La hiperglucemia de por sí no es un blanco terapéutico en la IC, y múltiples tratamientos de descenso de la glucemia aumentan el riesgo de episodios de IC a pesar del control de la glucemia
Los empeoramientos de la IC se suelen producir por el interjuego entre el sustrato cardíaco subyacente y las enfermedades simultáneas como la diabetes mellitus, la insuficiencia renal y la EPOC. Numerosos pacientes con IC experimentan rehospitalizaciones o muerte secundaria a enfermedades simultáneas más que a la cardiopatía en sí.
La significación pronóstica de las enfermedades simultáneas no cardíacas es igualmente importante en pacientes con IC con FE conservada, media y reducida. En la IC con fracción de eyección conservada (ICFEc), con la posible excepción de la espironolactona, estudios aleatorizados controlados de diversos tratamientos no pudieron demostrar hasta ahora mejoría de los resultados.
Algunas enfermedades simultáneas específicas merecen ser mencionadas. La diabetes mellitus y la cardiopatía simultáneas tienen mala evolución La diabetes simultánea se puede hallar en hasta el 44% de los pacientes con ICFEr y el 32–45% de los pacientes con ICEFc. Entre los pacientes con diabetes, la complicación más frecuente se debe a enfermedad cardiovascular, especialmente IC.
Sin embargo, datos acumulados de estudios previos sugieren que la hiperglucemia de por sí no es un blanco terapéutico en la IC, y múltiples tratamientos de descenso de la glucemia aumentan el riesgo de episodios de IC a pesar del control de la glucemia.
En el estudio reciente EMPA-REG OUTCOME (Empagliflozin, Cardiovascular Outcomes, and Mortality in Type 2 Diabetes) la empagliflozina, un inhibidor del cotransportador 2 de sodio–glucosa, tuvo efecto positivo sobre el riesgo cardiovascular. Específicamente, hubo una disminución de la mortalidad cardiovascular así como menor riesgo de hospitalización debida a IC en relación con el placebo. Datos similares se observaron con canagliflozin, otro inhibidor del cotransportador 2 de sodio–glucosa.
La ferropenia es otra comorbilidad frecuente en la IC crónica y es un indicador de enfermedad más avanzada, así como de disminución de la capacidad funcional y la calidad de vida.
Se halló ferropenia en el 33% de los pacientes con anemia o sin ella y se asoció con disminución de la supervivencia sin complicaciones a 36 meses. Un estudio no mostró utilidad del tratamiento con inyecciones de darbepoetina en pacientes con anemia ferropénica y otro no demostró utilidad de la administración de hierro oral, pero otros mostraron mejores resultados con el hierro intravenoso.
| 5.HAGA HINCAPIÉ EN LAS VISITAS DE SEGUIMIENTO DESPUÉS DEL ALTA |
Los 2–3 meses después del alta se conocen como la fase vulnerable, cuando la morbimortalidad aumenta más que en cualquier otro momento desde el ingreso. Esto generalmente se debe al empeoramiento a corto plazo de la hemodinamia cuando el tratamiento es subóptimo, no se cumple con la medicación y la dieta, y otros factores. Se debe controlar estrechamente a los pacientes al inicio de este período para prevenir que la congestión, la función renal y las inadaptaciones neurohormonales empeoren.
A fin de determinar quién tiene más alto riesgo durante esta fase vulnerable, se puede estratificar a los pacientes según el riesgo, sobre la base de ciertos indicadores pronósticos. La hipotensión, la disincronía ventricular, la anemia, el aumento persistente del BNP, y la hiponatremia tienen pronóstico negativo en pacientes con IC aguda. Otra herramienta para la estratificación del riesgo en este período es el Kansas City Cardiomyopathy
Questionnaire (KCCQ), un cuestionario respondido por el paciente sobre su calidad de vida para evaluar el estado funcional. Green et al. determinaron que los pacientes con IC crónica estable tenían siempre puntajes más altos del KCCQ y los pacientes con IC descompensada tenían puntajes más bajos.
Es de destacar que el puntaje KCCQ mayor antes del alta se asoció con mayor tasa de reingresos a 30-días por IC. Los síntomas evaluados por el KCCQ tienden a ser el motivo de consulta al reingreso al hospital entre los pacientes con IC. Por lo tanto, el KCCQ, así como los signos mencionados, son de utilidad significativa en un modelo pronóstico para reducir al mínimo las rehospitalizaciones cuando no hay signos de congestión.
La ACC y la AHA indican que el objetivo de la primera consulta posterior al alta es revaluar el estado del volumen vascular y la función renal y asegurar que la medicación que el paciente recibe corresponde al tratamiento orientado por las recomendaciones. Para propósitos pronósticos se puede considerar repetir el análisis de los biomarcadores. Además, investigaciones recientes demostraron que tiene fundamento pronóstico monitorear los valores de troponina I y que el valor aumentado a 1 mes pronostica el aumento de problemas clínicos a 12 meses.
Los controles siguientes deben optimizar el tratamiento, evaluar nuevos blancos para la intervención y tratar las enfermedades concomitantes a fin de prevenir nuevos factores precipitantes y empeoramientos. Asimismo, se debe optimizar el estado de los macronutrientes y micronutrientes. Instruir al paciente es igualmente esencial para asegurar el seguimiento continuado y el cumplimiento terapéutico y alimentario.
La rehabilitación cardíaca es un programa de tres ejes que se centra en mejorar la salud cardiovascular, prevenir el deterioro y reducir al mínimo las rehospitalizaciones aconsejando a los pacientes sobre hábitos de vida saludables, ejercicio y reducción del estrés.
En el estudio HF-ACTION se halló que la rehabilitación cardíaca mejoraba la calidad de vida relacionada con la salud. A pesar de esto, solo el 10% de los pacientes idóneos son derivados en el momento del alta. Con los nuevos accesos a la consejería y la rehabilitación a través de internet y los teléfonos celulares resulta más fácil incorporar estas medidas en la vida cotidiana.
El monitoreo hemodinámico invasivo ambulatorio es una intervención nueva para la evaluación continua del paciente ambulatorio. El CardioMEMS es un dispositivo implantable que mide la PECP para advertir precozmente la presencia de congestión antes de que esta progrese y sea necesario hospitalizar al paciente. Aunque tiene ciertos riesgos inherentes a su implantación, además de su costo, este dispositivo puede ser útil en determinados pacientes.
Por último, los pacientes con IC grave en etapa D o clase III-IV de la NYHA se deben evaluar para el empleo de dispositivos invasivos como los desfibriladores cardíacos invasivos y los dispositivos de asistencia ventricular cuando estén indicados, ya sea en el hospital o como pacientes ambulatorios. Las recomendaciones actuales de la ESC y la ACC/AHA aclaran cuando están indicados y la identificación temprana de los candidatos es esencial para evitar el deterioro continuo de la función cardíaca.
| Conclusión |
La fisiopatología detrás del desarrollo y el empeoramiento de la insuficiencia cardíaca es multifacética y, como tal se la debe evaluar más minuciosamente. Los autores de este artículo presentan un algoritmo utilizando una evaluación multimodal delos factores precipitantes y agravantes y una guía para un mejor tratamiento de la insuficiencia cardíaca aguda descompensada.
El artículo destaca la importancia de la evaluación exhaustiva, planes terapéuticos personalizados más allá de la congestión clínica, con tratamientos subutilizados, inclusión de las comorbidlidades no cardíacas y continuación del tratamiento después de la hospitalización.
El propósito es proporcionar orientación para mejorar la función cardíaca y por lo tanto, reducir al mínimo la rehospitalización entre los pacientes con insuficiencia cardíaca.
Resumen y comentario objetivo: Dr. Ricardo Ferreira