| Introducción |
La endocarditis infecciosa (EI) es una enfermedad antigua que puede ser difícil de diagnosticar y tratar, lo que lleva a una morbilidad y mortalidad sustanciales incluso en la era moderna. La literatura sobre el manejo de la EI presenta pocos ensayos clínicos aleatorizados de alta calidad. Esta segunda declaración de consenso de WikiGuidelines aborda el manejo basado en evidencia de la EI.
WikiGuidelines proporciona recomendaciones claras cuando se dispone de datos reproducibles de alta calidad y/o evidencia que confirma hipótesis y, de lo contrario, proporciona revisiones clínicas integrales que resumen diferentes enfoques clínicos.
Los usuarios finales a los que se dirige son médicos que brindan atención a pacientes en diversos entornos (académicos, comunitarios) y niveles socioeconómicos (países de ingresos bajos, medios o altos), con experiencia variada (médicos generales o especialistas). Incorporamos los principios de atención de alto valor (es decir, atención correcta, lugar correcto, costo correcto) y calidad de la atención médica (es decir, oportuna, segura, efectiva, eficiente, equitativa y centrada en el paciente).
| Métodos |
Esta guía se elaboró de acuerdo con la carta de WikiGuidelines y sigue la guía de informes Standards for Quality Improvement Reporting Excellence (SQUIRE 2.0). El sistema GRADE (Grading of Recommendations, Assessment, Development, and Evaluations) para evaluar la solidez de la evidencia fue reemplazado por un enfoque dicotómico de proporcionar recomendaciones claras o revisiones clínicas, debido a las preocupaciones publicadas con GRADE, incluido el riesgo de sesgo, la baja confiabilidad entre evaluadores y la disociación entre la solidez de la recomendación y la calidad de la evidencia.
Los datos de alta calidad que confirman hipótesis permiten una recomendación clara y se basan en al menos un ensayo controlado aleatorizado (ECA) adecuadamente realizado y con potencia adecuada y al menos otro estudio clínico controlado prospectivo concordante. En ausencia de tales datos, para proporcionar una guía que sea permisiva en lugar de proscriptiva, WikiGuidelines proporciona revisiones clínicas que analizan los enfoques clínicos, comparando los riesgos y los beneficios. Reconociendo el principio ético y clínico central de no hacer daño, se permite el consenso sobre evitar de manera rutinaria la atención no fundamentada incluso en ausencia de una recomendación clara.
| Resultados |
Las tablas y los recuadros incluidos aquí no tienen como objetivo servir como recomendaciones en el sentido tradicional de las directrices. La información se basa a menudo en datos limitados, extrapolaciones o ambos. Parte del contenido representa el intento de los autores de presentar opciones clínicas razonables basadas en sus interpretaciones de la literatura publicada imperfecta.
| Parte 1: Establecer el diagnóstico de EI |
Pregunta 1: ¿Qué criterios se deben utilizar para establecer el diagnóstico de EI? (Revisión clínica)
El estándar de referencia para el diagnóstico de EI es la confirmación anatomopatológica. Sin embargo, dicha información prácticamente nunca está disponible en el momento en que se deben tomar decisiones terapéuticas empíricas y, a menos que el paciente se someta a un reemplazo quirúrgico de una válvula, sigue sin estar disponible para confirmar el diagnóstico. A lo largo de los años se han desarrollado varios esquemas para guiar a los médicos en el diagnóstico de EI.
Cinco de los siete esquemas se basan en los criterios originales de Duke. Dichos esquemas suelen incluir criterios clínicos, microbiológicos y de imágenes. Esquemas como los criterios de Duke modificados (actualizados en 2023 a los criterios Duke-ISCVID) se utilizan ampliamente y son convenientes para los médicos, ya que facilitan la toma de decisiones diagnósticas y terapéuticas en tiempo real.
No existen estudios de alta calidad que determinen definitivamente qué esquema de diagnóstico es más preciso, ni tampoco estudios cara a cara que comparen los resultados clínicos entre esquemas. Dado que la mayoría de los estudios de investigación aplican los criterios de Duke modificados, es probable que estos criterios concuerden con lo que utilizan la mayoría de los médicos.
Pregunta 2: ¿Cómo se deben utilizar los parámetros del hemocultivo para fundamentar la sospecha de endocarditis infecciosa? (Revisión clínica)
¿El tiempo hasta la positividad de los hemocultivos predice la endocarditis infecciosa? Los datos observacionales sugieren que el tiempo hasta la positividad (TTP) de los hemocultivos de menos de 12 horas está asociado con la endocarditis infecciosa por Staphylococcus aureus y predice de forma independiente la mortalidad hospitalaria. Un estudio similar encontró que un TTP más corto estaba asociado con la endocarditis infecciosa en la bacteriemia monomicrobiana por Enterococcus faecalis.
¿Cuánto tiempo deben incubarse los hemocultivos en casos sospechosos de EI? Los datos de observación sugieren que, con las técnicas de cultivo modernas, una incubación estándar de 5 días para hemocultivos es adecuada para casi todas las causas de EI.
¿El número de conjuntos de hemocultivos se relaciona con el diagnóstico de EI? Dos grandes estudios observacionales sugieren que el rendimiento máximo para recuperar un patógeno de los hemocultivos se logra con 3 (96% 17 -98%) a 4 juegos (99,8%) durante 24 horas, cada uno de los cuales comprende 2 frascos llenos de 10 ml. Siempre que sea posible, estos deben tomarse antes de los antibióticos, ya que el rendimiento de los hemocultivos disminuye después de recibirlos.
Preguntas 3 y 4: ¿Cómo se pueden establecer los diagnósticos de endocarditis infecciosa por Bartonella y Coxiella burnetii (fiebre Q)? (Revisión clínica)
Existen datos limitados que informan sobre la precisión de las pruebas de diagnóstico para la endocarditis infecciosa por Bartonella y C. burnetii. Si bien puede ser razonable utilizar un valor de corte de título de Ig G de al menos 1:800 como evidencia diagnóstica de la endocarditis por Bartonella, debe tenerse en cuenta que el conjunto de datos que respalda este valor de corte es limitado; los pacientes que no tienen EI pueden tener títulos tan altos como 1:800 o más, y los pacientes pueden tener títulos más bajos, pero aún tener a Bartonella como etiología de EI.
El valor de corte serológico ampliamente utilizado para diagnosticar la endocarditis infecciosa por fiebre Q es un título de anticuerpos IgG de 1:800. Sin embargo, ningún estudio publicado de alta calidad ha establecido su precisión.
Pregunta 5: ¿Cuál es el papel de las pruebas de diagnóstico rápido molecular en el diagnóstico de la endocarditis infecciosa? (Revisión clínica)
Cuando está disponible, algunos profesionales utilizan pruebas de ARN de tejido valvular en casos no resueltos de endocarditis con cultivo negativo, con una amplia variabilidad en la sensibilidad reportada. Las pruebas de diagnóstico molecular requieren más estudios antes de que puedan recomendarse de manera rutinaria, pueden ser útiles en casos selectos.
Pregunta 6: ¿Cuál es el papel del ecocardiograma en el diagnóstico de la endocarditis infecciosa? (Revisión clínica)
En la mayoría de los casos sospechosos, la realización de un ecocardiograma es habitual. No obstante, se debe solicitar cuando sirva para orientar las decisiones de tratamiento. Tanto la probabilidad pretest de EI como la calidad del estudio afectan en gran medida el impacto de la ecocardiografía transtorácica (ETT) en el tratamiento del paciente. Una ETT negativa puede ser adecuada para descartar endocarditis de válvula nativa (EVN) si la probabilidad pretest es baja (p. ej., <10 %), o con un estudio de alta calidad, incluso si la probabilidad pretest es moderada (p. ej., <25 %).
La ecocardiografía transesofágica (ETE) es más sensible que la ETT para el diagnóstico de EI. La ETE es más útil en escenarios específicos: (1) para reducir la posibilidad de EVN cuando sigue habiendo una probabilidad inaceptablemente alta después de una ETT negativa (p. ej., 5%-10%) y cuando la eliminación del diagnóstico cambiará el tratamiento del paciente; (2) en la evaluación de EVP cuando la ETT tiene una sensibilidad menor; y/o (3) para facilitar la planificación quirúrgica o para evaluar complicaciones específicas (p. ej., absceso perivalvular).
Pregunta 7: ¿Cuál es el papel de los sistemas de puntuación en la identificación de pacientes que pueden requerir una ecografía transesofágica para el diagnóstico de endocarditis infecciosa? (Revisión clínica)
Se han desarrollado numerosos sistemas de puntuación clínica para identificar mejor a los pacientes que pueden beneficiarse de la ETE. Solo se han evaluado en estudios retrospectivos. Por lo tanto, los datos son insuficientes para hacer una recomendación clara.
Pregunta 8: ¿Cuál es el papel de la ecografía transtorácica seriada para evaluar el progreso de la endocarditis infecciosa o aumentar la sensibilidad diagnóstica? (Revisión clínica)
No existen datos de alta calidad que respalden la realización de ecocardiogramas repetidos o seriados en pacientes con un estudio inicial negativo. Si el resultado cambiará la conducta, un ecocardiograma repetido puede ser de utilidad. De lo contrario, no parece proporcionar un beneficio a los pacientes.
Pregunta 9: ¿Cuál es el papel de la PET con fluorodesoxiglucosa (18F-FDG) en el diagnóstico y el tratamiento de la endocarditis infecciosa? (Revisión clínica)
Numerosos estudios observacionales han evaluado la precisión de la PET/TC con 18F-FDG para el diagnóstico de EVN, EVP y EI relacionada con dispositivos cardíacos (EICD). Los metanálisis han informado que la sensibilidad para EVN es baja, especialmente en comparación con EVP y EICD; sin embargo, la especificidad sigue siendo alta. La PET/CT con 18F-FDG requiere muchos recursos, no está disponible en todos los centros y expone a los pacientes a radiación ionizante; aún se desconoce si su uso mejora los resultados.
| Parte 2: Equipos multidisciplinarios de EI |
Pregunta 1: ¿Un equipo multidisciplinario de EI mejora los resultados de los pacientes? (Revisión clínica)
Los equipos multidisciplinarios de EI pueden estar compuestos por expertos en infectología, farmacia, cardiología, cirugía cardíaca y, según la disponibilidad, especialistas en radiología, neurología, stroke, cirugía general o vascular, adicciones y servicio social. Los estudios observacionales sugieren que la participación de un equipo multidisciplinario de EI puede mejorar los resultados del paciente, incluido el tiempo hasta la intervención quirúrgica y la mortalidad. Sin embargo, no hay ensayos clínicos aleatorizados.
| Parte 3: Profilaxis |
Pregunta 1: ¿En qué pacientes es adecuado prescribir profilaxis antibiótica para prevenir la endocarditis infecciosa? (Revisión clínica)
La profilaxis corre el riesgo de tener efectos adversos y favorece la resistencia a los antibióticos, lo que provoca daños a nivel social. En consecuencia, los autores de WikiGuidelines prefieren limitar la profilaxis a los pacientes que se perciben como de mayor riesgo de EI (p. ej., válvulas cardíacas protésicas o personas con antecedentes de EI) y que se someten a procedimientos odontológicos en los que es probable que exista un mayor riesgo de bacteriemia (p. ej., manipulación del tejido gingival o la región periapical, o perforación de la mucosa oral). Si se utiliza, los riesgos de la profilaxis antimicrobiana pueden mitigarse parcialmente utilizando una dosis única en lugar de ciclos más prolongados.
Pregunta 2: ¿Qué antibióticos son apropiados para la profilaxis antibiótica para prevenir la endocarditis infecciosa? (Revisión clínica)
No existen datos de alta calidad que informen sobre la eficacia relativa de los distintos regímenes de profilaxis para prevenir la endocarditis infecciosa. Sin embargo, es racional seleccionar antibióticos profilácticos que sean activos contra los estreptococos del grupo viridans (VGS). Se prefiere la administración oral, y las penicilinas y cefalosporinas se asocian con una tasa menor de infección por Clostridioides difficile en comparación con la clindamicina. La amoxicilina parece ser la más utilizada y conlleva el menor riesgo de eventos adversos en general.
| Parte 4: Tratamiento |
Pregunta 1: ¿Qué terapia empírica se debe considerar para la EI? (Revisión clínica)
Hay poca evidencia de alta calidad disponible para guiar la selección de terapia empírica para EI conocida o sospechada. En general, una combinación de vancomicina o daptomicina (para cubrir MRSA, Enterococcus spp, y en el caso de válvula protésica, estafilococos coagulasa-negativos) y un β-lactámico como ceftriaxona (si se sospecha un foco odontogénico o gastrointestinal) o cefazolina (si se sospecha S. aureus sensible a la meticilina [MSSA]) puede ser razonable, aunque también son posibles regímenes alternativos y casi no hay evidencia comparativa directa. A falta de estudios comparativos de resultados, algunos autores prefieren una dosis de daptomicina de 8 a 10 mg/kg si se sospecha S. aureus y de 10 a 12 mg/kg si se trata de enterococos. Para minimizar el daño, es mejor reservar los aminoglucósidos y la rifampicina para la terapia definitiva, si es que se utilizan.
Tabla 1. Posibles antibióticos de dosis única para la profilaxis de la endocarditis infecciosa en función de la cobertura antimicrobiana
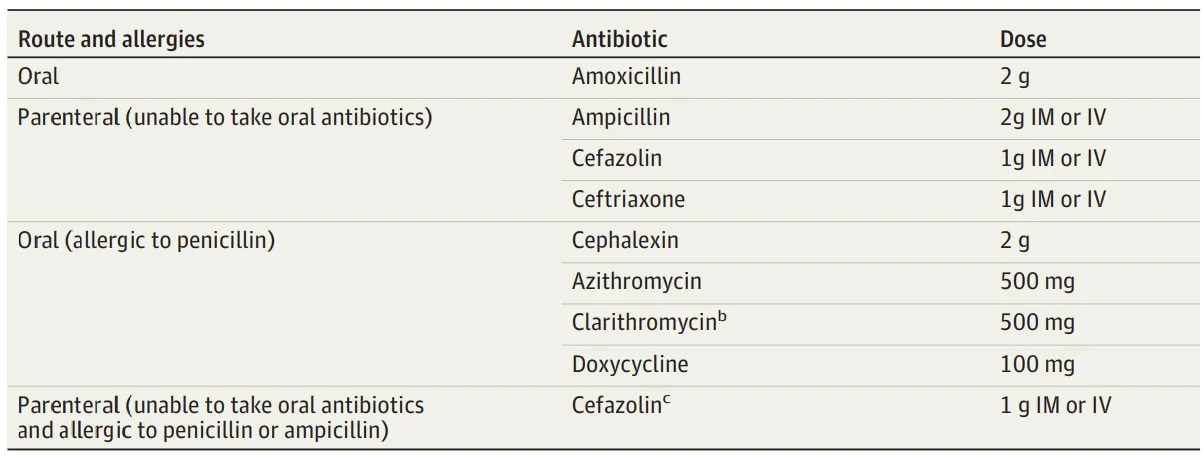
Pregunta 2: ¿Cuáles son las posibles opciones definitivas de tratamiento intravenoso para la endocarditis infecciosa? (Revisión clínica)
La terapia antibiótica definitiva recomendada para la EI depende del organismo etiológico, su susceptibilidad, factores del paciente (p. ej., comorbilidad, alergia) y si la infección es de una válvula nativa o protésica. En general, la adición de agentes adyuvantes (p. ej., β-lactámicos, aminoglucósidos, rifampicina) requiere una consideración cuidadosa de los riesgos y beneficios y un reconocimiento de las limitaciones de la evidencia. La mayoría de los autores de WikiGuidelines sugieren no usar de manera rutinaria aminoglucósidos adyuvantes debido a la falta de evidencia de beneficio con un riesgo demostrable de daño.
Tabla 2. Opciones para regímenes de terapia intravenosa definitiva suponiendo que el organismo es susceptible
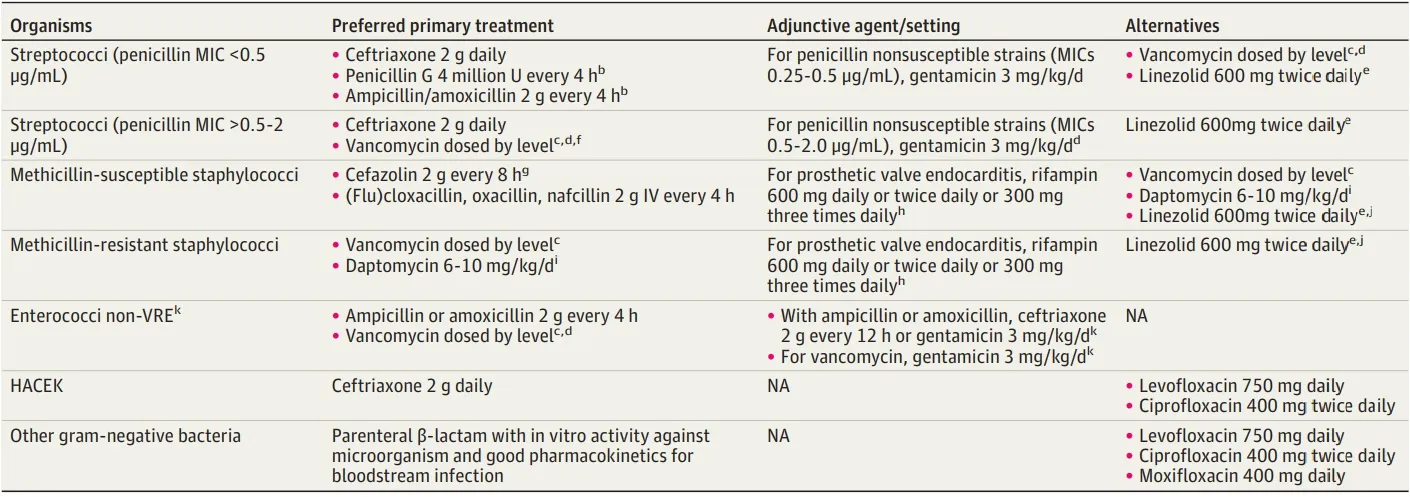
Pregunta 3: ¿Se puede utilizar la terapia antimicrobiana oral para tratar la endocarditis infecciosa? (Recomendación clara)
Es posible proporcionar una recomendación clara para esta pregunta. Tres ensayos clínicos aleatorizados han establecido que la transición de la terapia intravenosa inicial a la terapia oral es al menos tan efectiva como la terapia intravenosa sola para el tratamiento de la EI. Es importante destacar que la terapia intravenosa sola nunca se ha establecido como superior a la terapia antimicrobiana oral en ningún ensayo clínico o estudio observacional de pacientes con EI. Por lo tanto, la transición a la terapia oral desde la terapia intravenosa inicial es una opción razonable para tratar a los pacientes con EI.
Tabla 3. Resumen de los antibióticos de transición orales utilizados en estudios clínicos publicados
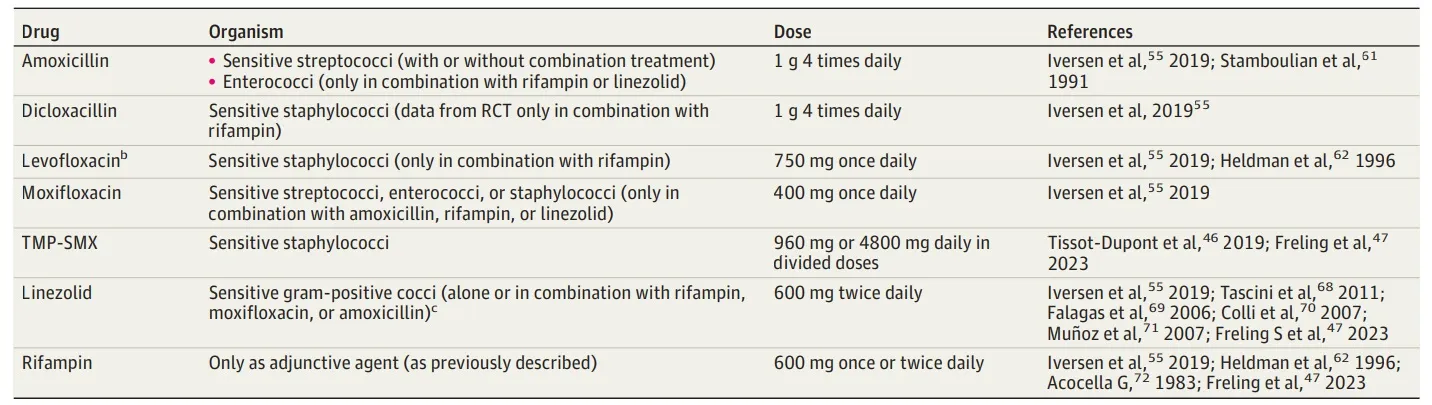
Pregunta 4: Si se utiliza terapia antimicrobiana oral en el tratamiento de la endocarditis infecciosa, ¿existen agentes preferidos?, ¿es necesaria una duración específica de la terapia intravenosa inicial y cuáles son los criterios clínicos razonables para la selección de pacientes? (Revisión clínica)
No todos los agentes antimicrobianos orales son candidatos probables para el tratamiento de la EI. La experiencia histórica sugiere que las sulfonamidas, tetraciclinas y macrólidos más antiguos pueden conducir a malos resultados quizás relacionados con las bajas concentraciones en sangre alcanzables en relación con las CIM objetivo. TMS fue inferior como una opción de inicio para el tratamiento de la EI estafilocócica en 2 ECA. Si se utiliza terapia oral, es racional seleccionar antibióticos que hayan demostrado tener eficacia en estudios publicados.
No está claro en qué medida se necesita una terapia intravenosa de introducción antes de la transición a la terapia oral, ya que los estudios han utilizado una amplia gama de terapias intravenosas de introducción antes de la terapia oral. Los criterios razonables de selección de pacientes para la terapia oral pueden incluir (1) estabilidad clínica sin indicación inmediata para control de la fuente mediante procedimiento o cirugía cardíaca; y (2) la bacteriemia ha desaparecido o está desapareciendo sin necesidad de control de la fuente; y (3) hay disponible un régimen antibiótico oral al cual el organismo etiológico es susceptible in vitro y que está respaldado por datos clínicos publicados; y (4) es probable una buena absorción del antibiótico desde el tracto gastrointestinal; y (5) no hay determinantes socioeconómicos que hagan de la terapia intravenosa la vía de elección.
Pregunta 5: ¿Cuál es la duración recomendada del tratamiento antimicrobiano para la endocarditis infecciosa? (Revisión clínica)
EI izquierda
La evidencia que respalda la duración del tratamiento para la endocarditis infecciosa es casi completamente observacional y la mayoría de las duraciones se basan en la práctica histórica. Un ECA estableció que la endocarditis estreptocócica sensible a la penicilina tratada con 2 semanas de terapia combinada con ceftriaxona y gentamicina tuvo resultados similares a 4 semanas de monoterapia con ceftriaxona.
En el caso de otros patógenos, y en ausencia de datos, la práctica histórica ha sido tratar la endocarditis izquierda por estafilococos y enterococos durante 6 semanas y la endocarditis por HACEK durante 4 semanas. Las recomendaciones para tratar la EVP durante 6 semanas también se basan en opiniones más que en datos de alta calidad.
EI derecha
En el caso de la endocarditis infecciosa derecha no complicada causada por MSSA (definida como la ausencia de complicaciones intracardiacas o sistémicas de la infección), los estudios observacionales prospectivos y un ensayo clínico aleatorizado sugieren que 2 semanas de terapia antibiótica combinada podrían dar como resultado tasas de curación similares a las de los tratamientos más prolongados.
Se desconocen las duraciones óptimas de la terapia para la endocarditis infecciosa derecha no complicada fuera de la población de personas que se inyectan drogas y/o causada por otros patógenos. Los autores de WikiGuidelines creen que puede ser razonable en casos cuidadosamente seleccionados utilizar una duración de terapia similar para otros patógenos que para MSSA. En el caso de los pacientes con endocarditis infecciosa del lado derecho complicada, no hay datos disponibles que orienten la duración del tratamiento y a menudo se utilizan tratamientos más prolongados sin ninguna evidencia que los respalde.
| Discusión |
La EI se asocia a una alta morbilidad y mortalidad. A pesar de la extensa literatura que analiza el tratamiento de la endocarditis infecciosa, los autores han descubierto que la mayoría de los aspectos del diagnóstico y el tratamiento se basan en la práctica histórica y en estudios observacionales pequeños y obsoletos.
Los estudios de alta calidad solo pueden informar una recomendación clara: antibióticos orales de transición para el tratamiento de la endocarditis infecciosa. Esta escasez de evidencia de alta calidad cambiará con la llegada de los resultados de varios ensayos controlados aleatorizados en curso muy necesarios.
| Conclusiones |
Esta declaración de consenso destaca la falta de evidencia de alta calidad que respalde la mayoría de las prácticas modernas en el diagnóstico y el tratamiento de la endocarditis infecciosa bacteriana en adultos.
Como se indicó anteriormente, ningún ensayo clínico o síntesis de conocimientos puede extrapolarse a todos los posibles escenarios de atención al paciente; por lo tanto, esta guía no pretende establecer estándares médico-legales de atención ni reemplazar el criterio del médico para pacientes individuales.