| Introducción |
El embarazo ectópico tubárico (EET) es la implantación de un óvulo fecundado en la trompa de Falopio y es una afección temporal que puede provocar una rotura tubárica y hemorragia potencialmente mortal. Representa aproximadamente el 2 % de todos los embarazos en Europa y Norteamérica y el 2,7 % de las muertes relacionadas con el embarazo en EE.UU.
El riesgo de hemorragia en un EE tratado es ≥50 %. Sin embargo, muchos EET ahora se detectan con la suficiente antelación como para ser tratados en el ámbito ambulatorio.
Las afecciones que provocan inflamación y cicatrización tubárica, como un EE previo, enfermedad inflamatoria pélvica y cirugía tubárica previa, aumentan el riesgo de EE. Las pacientes con un EE previo tienen un riesgo del 8 al 15 % de tener otro. El tabaquismo, que puede afectar la motilidad de las trompas de Falopio o la renovación de las células epiteliales tubáricas, es otro factor de riesgo.
| Evaluación |
Si bien el manchado vaginal y el dolor abdominal bajo son comunes durante el embarazo, también son síntomas típicos de presentación de un EET y constituyen indicaciones para la ecografía en personas con una prueba sérica positiva para ß-hCG.
La visualización ecográfica de un saco gestacional que contiene un saco vitelino, un embrión o ambos fuera del útero es diagnóstica. Sin embargo, muchos EE no progresan a una etapa visible o carecen de estructuras de desarrollo normales. En estos casos, la ecografía puede mostrar una masa no anexial homogénea o una estructura extrauterina en forma de saco.
Aunque la utilidad diagnóstica de la ecografía es mayor cuando la evaluación es realizada por expertos, con equipo especializado, estos hallazgos ecográficos en una paciente con una prueba de embarazo positiva y sin embarazo intrauterino sugieren un EE. Un embarazo normal debería observarse en la ecografía transvaginal aproximadamente 5 o 6 semanas después de la última menstruación, pero podría no observarse hasta que el nivel sérico de ß-hCG alcance aproximadamente 2500 mUI/ml. Si el nivel de ß-hCG es >3500 mUI/ml, no se visualiza un embarazo intrauterino en la ecografía transvaginal y la historia clínica no sugiere un aborto espontáneo reciente (es decir, sangrado vaginal abundante), también es muy probable que se trate de un EE. Si no se observa un embarazo intrauterino en la ecografía y se visualiza líquido libre en la cavidad peritoneal se debe sospechar un EE roto con hemoperitoneo.
Cuando una paciente con dolor, sangrado o ambos presenta una prueba de embarazo positiva, pero en la ecografía transvaginal no se visualiza embarazo, se aplica el término "embarazo de localización desconocida".
El diagnóstico diferencial incluye un embarazo intrauterino normal temprano, una pérdida prematura del embarazo intrauterino y un EE. En tales casos, si el embarazo no es deseado, el diagnóstico puede acelerarse vaciando el útero mediante procedimientos o medicamentos.
Si el embarazo es deseado, los médicos deben realizar un seguimiento estrecho de las pacientes con pruebas seriadas de ß-hCG cada 2 días, evaluación frecuente de síntomas y repetición de imágenes para reevaluar la ubicación del embarazo.
El EE se sugiere por la falta de duplicación de los niveles de ß-hCG en 48 horas o por el empeoramiento del dolor o inestabilidad hemodinámica. En pacientes con estabilidad clínica y embarazos deseados, antes de cualquier intervención presuntiva se requiere una evaluación cuidadosa de la viabilidad y la ubicación del embarazo.
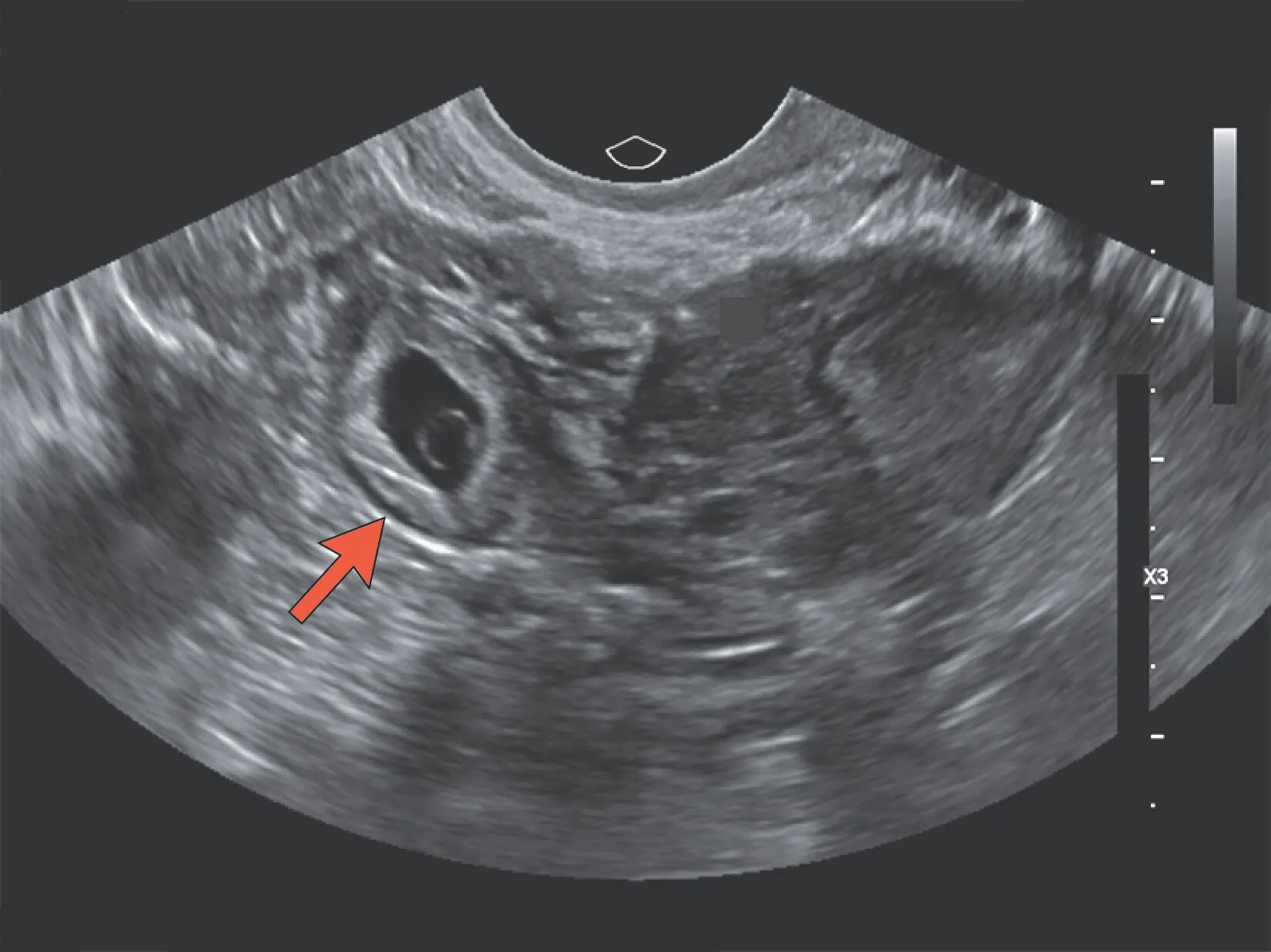
Ecografía transvaginal de embarazo ectópico tubárico definitivo. Un saco gestacional y un saco vitelino (flecha) son visibles.
| Manejo quirúrgico |
La cirugía está indicada para pacientes que están hemodinámicamente inestables y aquellas que prefieren un tratamiento acelerado o desean evitar el metotrexato. La laparotomía para el EET ocasionalmente está justificada en casos de hemorragia intrabdominal masiva o si la enfermedad adhesiva impide el abordaje laparoscópico.
El procedimiento generalmente implica una salpingectomía laparoscópica o una salpingostomía (extirpación del embarazo a través de una incisión tubárica, preservando la trompa, a veces denominada salpingotomía); ambas pueden realizarse de forma ambulatoria. La recuperación es relativamente rápida con un abordaje mínimamente invasivo y las pacientes suelen retomar sus actividades habituales en unas 2 semanas.
Aunque la salpingectomía se considera el procedimiento estándar y se prefiere en caso de rotura de la trompa, ciertos factores, como el grado en que la trompa de Falopio contralateral y los planos de fertilidad futura están dañados, pueden favorecer la salpingostomía. Las pacientes que se someten a salpingostomía tienen un riesgo pequeño de retención de tejido trofoblástico, por lo que este procedimiento generalmente requiere la verificación de que los niveles de ß-hCG vuelvan a cero después de la operación y el tratamiento con metotrexato si hay evidencia de persistencia del trofoblasto.
El ensayo aleatorizado European Surgery in Ectopic Pregnancy sobre cirugía en el EE comparó la salpingostomía con la salpingectomía. Entre las 446 participantes, la incidencia acumulada de embarazos posteriores en un plazo de 36 meses no difirió significativamente entre ambos grupos (61 % y 56 %, respectivamente). De las 215 pacientes asignados a salpingostomía, el 20 % (n=43) se sometieron a salpingectomía debido a sangrado tubárico persistente, el 1 % (n=2) se sometió a una nueva laparoscopia debido a sangrado postoperatorio y 5 (2 %) se sometieron a una nueva laparoscopia para tratar la persistencia del trofoblasto.
Los eventos adversos incluyeron conversión a laparotomía (1 % en cada grupo), transfusión sanguínea (7 % en el grupo de salpingostomía y 3 % en el grupo de salpingectomía) y reingreso (5 % y 1 %, respectivamente). Estos hallazgos respaldan la salpingectomía como el tratamiento quirúrgico de elección para pacientes con EE y una trompa contralateral sana.
Una revisión sistemática y un metaanálisis que incluyeron ensayos aleatorizados y estudios observacionales confirmaron las ventajas de la salpingectomía sobre la salpingostomía. Sin embargo, el ensayo aleatorizado más grande incluyó solo a participantes con una trompa contralateral normal. Tras excluir este ensayo del análisis, el análisis de subgrupos incluyendo a pacientes con factores de riesgo de infertilidad sometidas a salpingectomía (en comparación con salpingostomía) mostró menor probabilidad de embarazo intrauterino posterior y mayor probabilidad de EE repetido. Estas observaciones sugieren que se puede preferir la salpingostomía para pacientes con alto riesgo de enfermedad tubárica en la trompa contralateral, que desean permanecer fértiles en el futuro. La salpingectomía bilateral es una opción para pacientes que desean anticoncepción permanente después del tratamiento de un EE.
El metotrexato (administrado por vía intramuscular) es el tratamiento estándar para el manejo médico del EET. El metotrexato inactiva la dihidrofolato reductasa, lo que causa la depleción del tetrahidrofolato, un cofactor esencial para la síntesis de ADN y ARN; las células de división rápida como las células trofoblásticas son susceptibles a su acción.
No se debe usar metotrexato si se desea el embarazo antes de que el EE sea confirmado definitivamente. Para ser elegible para el manejo médico, que se proporciona de forma ambulatoria, se requiere estabilidad hemodinámica, ausencia de evidencia de rotura tubárica y capacidad para el seguimiento, incluyendo la ausencia de dificultades con el transporte.
Las pacientes con un nivel sérico de ß-hCG <5000 mUI/ml, ausencia de actividad cardíaca embrionaria y un EE de menos de 4 cm son elegibles para recibir metotrexato como alternativa al tratamiento quirúrgico. Sin embargo, el lapso hasta la resolución del embarazo puede prolongarse. En un estudio retrospectivo reciente, la mediana de tiempo hasta la resolución del embarazo fue de 22 días en los casos en que el tratamiento médico fue exitoso.
El metotrexato puede administrarse en protocolos de dosis única, 2 dosis o multidosis. El más utilizado es el régimen de dosis única y, aunque la mayoría de las pacientes lograrán la resolución del embarazo con una sola dosis, se les debe informar acerca de la posibilidad de administrar dosis adicionales.
Para cada protocolo, se miden los niveles séricos de ß-hCG al inicio, durante el tratamiento y semanalmente durante el seguimiento posterior al mismo. El éxito del tratamiento se define, de forma más conservadora, como la resolución del nivel de ß-hCG a <5 mUI/ml. Se pueden administrar dosis adicionales o menores a las inicialmente planificadas, dependiendo principalmente de la progresión de los niveles de ß-hCG durante el tratamiento.
La efectividad relativa del protocolo de 2 dosis parece ser mayor que la del protocolo de dosis única en pacientes con niveles de ß-hCG >3000 mUI/ml y en aquellas con masas anexiales mayores (>2 cm). Se notificaron eventos adversos, con mayor frecuencia estomatitis y conjuntivitis, en el 31 % de las pacientes que recibieron el protocolo de 2 dosis y en el 23 % de las que recibieron el protocolo de dosis única.
En última instancia, las pacientes que optan por la terapia con metotrexato pueden esperar una mediana de tiempo hasta la resolución del embarazo de 28 días. Para aquellas que desean concebir de nuevo, los resultados de fertilidad de 207 participantes asignadas aleatoriamente a salpingostomía más metotrexato o salpingectomía sola, y de 199 participantes asignadas aleatoriamente a salpingostomía más metotrexato o metotrexato solo, no mostraron diferencias significativas entre los grupos en la incidencia de embarazo durante los 2 años posteriores.
Aunque los datos son limitados, una población seleccionada de pacientes podría ser elegible para el manejo expectante del EET. Un metanálisis que incluyó 2 ensayos aleatorizados (con 153 participantes) comparó la administración intramuscular de dosis única de metotrexato con el manejo expectante del EET.
Según los datos individuales de las participantes, el tratamiento tuvo éxito en el 79 % de las participantes del grupo de metotrexato y en el 69 % del grupo de manejo expectante, mientras que se recurrió a la intervención quirúrgica en el 10 % y el 19 %, respectivamente.
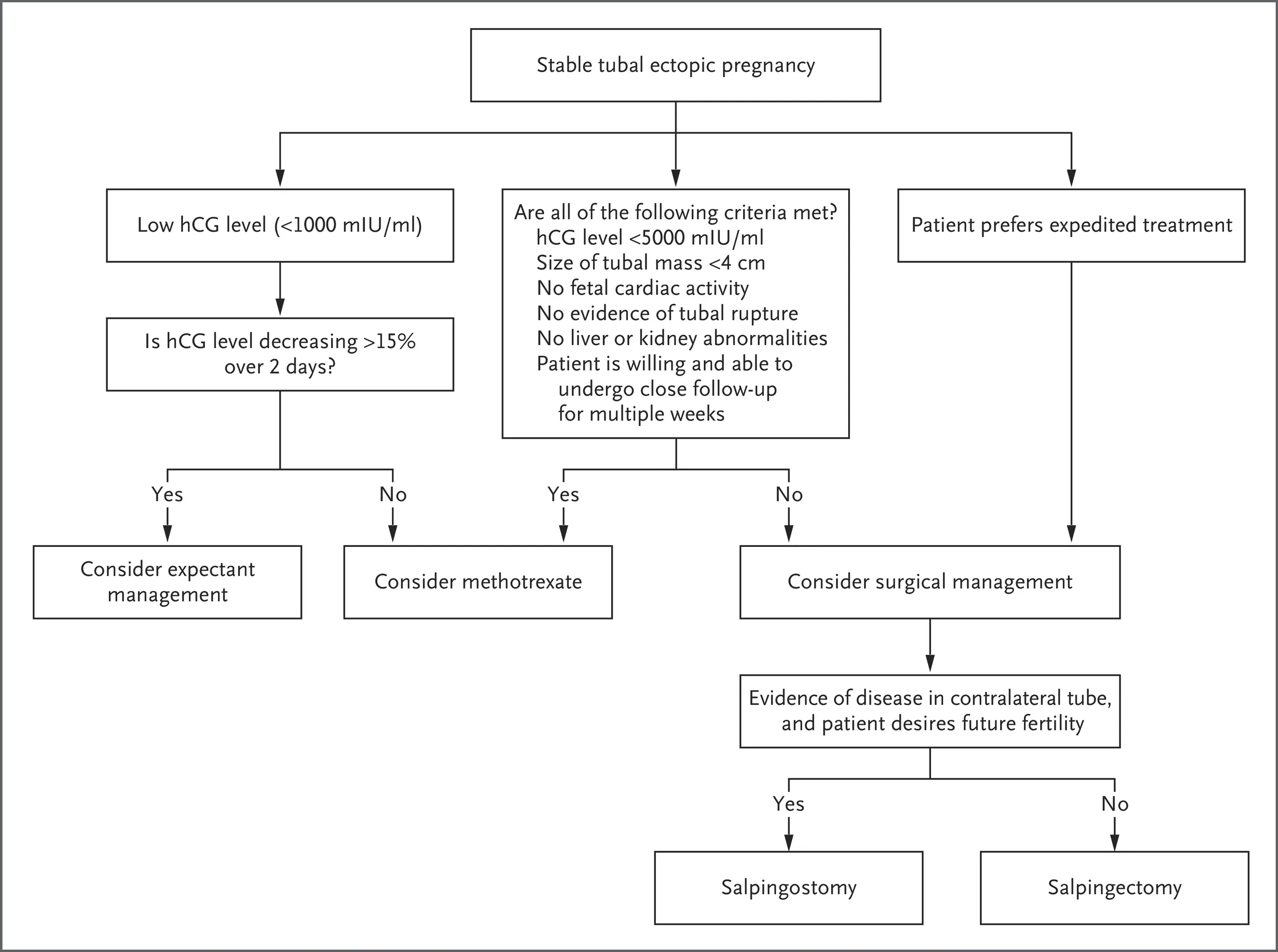
| Seguimiento y asesoramiento postratamiento |
Se carece de datos que permitan formular recomendaciones sobre el momento óptimo para concebir un nuevo embarazo tras la resolución de un EET, con cirugía o metotrexato. En futuros embarazos se recomienda el seguimiento tan pronto como una prueba de embarazo sea positiva para proporcionar un diagnóstico y tratamiento tempranos, en caso de recurrencia del EE.
Las pacientes que no planean concebir deben recibir asesoramiento anticonceptivo centrado en ellas. En un estudio de cohorte prospectivo con mujeres que habían sufrido pérdida de embarazo y que incluyó 116 EE, la quinta parte de las pacientes con EE presentó estrés postraumático y ansiedad, y una décima parte presentó depresión moderada o grave que persistió 9 meses después del tratamiento.
| Áreas de incertidumbre |
El gefitinib, un inhibidor del receptor del factor de crecimiento epidérmico (EGER), podría alterar el lugar de implantación del EE debido a la elevada expresión de EGFR en el tejido placentario. Una serie de casos y un ensayos abiertos mostraron una alta probabilidad de resolución exitosa del EET con un ciclo de gefitinib además del metotrexato. Sin embargo, un ensayo aleatorizado que comparó un ciclo de 7 días de gefitinib oral con placebo, combinado con una dosis única de metotrexato, mostró poca diferencia en el porcentaje de pacientes que se sometieron a intervención quirúrgica (30 % y 29 %, respectivamente).
Un ensayo abierto mostró que la mifepristona junto con metotrexato puede ser más efectiva que el metotrexato solo, pero se necesitan ensayos más amplios para informar mejor su eficacia.
Se carece de datos contemporáneos y de consenso social para orientar el uso de la profilaxis con inmunoglobulina anti-D tras el tratamiento del EE.