| Introducción |
En la anastomosis por compresión magnética (ACM), se colocan 2 imanes de tierra rara en la luz del órgano que se anastomosa, lo que induce necrosis en el sitio de compresión, permitiendo su adsorción§ . Esta técnica puede inducir espontáneamente una anastomosis similar a la creada mediante cirugía, pero con menor invasividad [1].
En términos de su aplicación clínica, se espera que el procedimiento sea una alternativa a la cirugía en pacientes con serias comorbilidades, antecedentes de cirugía abdominal complicada, o complicaciones postoperatorias.
En la región esofágica, la atresia esofágica en los niños ha sido tratada exitosamente con la ACM [2,3]. En la región hepatobiliar, se ha efectuado exitosamente una ACM para la estenosis biliar severa y la obstrucción biliar completa, que son difíciles de manejar usando intervenciones no quirúrgicas convencionales [4-6]. No obstante, su aplicación en la región gastrointestinal todavía se está desarrollando.
Se han presentado anastomosis gastrointestinales exitosas en animales usando ACM, y su no inferioridad en relación con la anastomosis convencional con sutura o grampas ha sido reportada, basado en la tolerancia detallada a la presión anastomótica y los exámenes histológicos [7-13].
Sin embargo, hay sólo unos pocos reportes de anastomosis gastrointestinales en seres humanos [14-18], y no hay disponibles series de casos con muestras de gran tamaño. Por lo tanto, la validez y factibilidad de la ACM para la anastomosis gastrointestinal no son claras.
Graves y col. [14], reportaron que podía crearse una anastomosis gastrointestinal efectiva usando ACM durante una cirugía abierta bajo anestesia general, comparable con una anastomosis intestinal convencional usando engrampadora o suturas. Los autores de este trabajo hipotetizaron que la ACM puede ser una alternativa valiosa y menos invasiva a la cirugía, si se puede realizar seguramente sin utilizar anestesia general.
Este estudio retrospectivo apuntó a evaluar la seguridad, eficacia, y factibilidad de la ACM para la obstrucción gastrointestinal, sin requerir anestesia general.
| Métodos |
En esta serie retrospectiva de casos, 14 pacientes que fueron sometidos a una anastomosis gastrointestinal o una derivación gastrointestinal con ACM, en el Department of Surgery of the International University of Health and Welfare Hospital, desde enero de 2013 hasta octubre de 2019, fueron enrolados.
Fueron elegibles para la inclusión los pacientes adultos con obstrucción o estenosis gastrointestinales que requerían alguna anastomosis intestinal, pequeña o grande, para restaurar la continuidad intestinal, con severas comorbilidades, antecedentes de cirugía abdominal complicada, o complicaciones postoperatorias, y que no eran capaces de tolerar una cirugía.
Los pacientes en los que se consideró imposible la colocación adecuada de imanes y aquellos con órganos interpuestos identificados durante la evaluación previa al tratamiento, fueron excluidos porque tenían un riesgo alto de lesión de otros órganos.
El procedimiento de ACM fue aprobado por el Institutional Review Board del International University of Health and Welfare Hospital (aprobación n° 13-B-90). Se obtuvo un consentimiento informado de todos los pacientes. El objetivo final primario fue el éxito técnico de la ACM. Los objetivos finales secundarios fueron el tiempo del procedimiento, duración de la formación de la anastomosis, complicaciones, duración de la estadía hospitalaria, y cantidad de días hasta el comienza de la ingesta oral.
> Evaluación pretratamiento
Los pacientes fueron sometidos a seriadas gastrointestinales y tomografía computada mejorada (TCm), para confirmar la ausencia de interposición de otros órganos entre los sitios anastomóticos, y para calcular la longitud de la estenosis y la distancia entre los imanes.
> Imanes utilizados
Se usaron imanes de cobalto-samario. Los imanes colocados en los lados oral y anal del tracto intestinal se denominaron "imanes hijos" e " imanes padres", respectivamente. Esos imanes tenían un diámetro de 10 a 25 mm y 5 mm de grosor. Eran imanes en forma de disco de 1.800 a 3.500 gauss. Los imanes fueron elegidos dependiendo de los diámetros del intestino y de la estenosis (Fig. 1A). Siempre se emplearon imanes menores a 17,5 mm de tamaño para el intestino delgado, y mayores de 22,5 mm para el colon.

- FIGURA 1: Imanes y dispositivos utilizados en la ACM. (A) Imanes de cobalto-samario. Desde la izquierda: 12,5 mm, 15 mm, 17,5 mm, 22,5 mm x 5 mm. (B) El imán es transportado por un catéter en canastilla de litotricia (flecha).
> Técnica quirúrgica
Con el paciente en posición supina, el procedimiento fue realizado bajo guía constante fluoroscópica, con la administración endovenosa de 0,4 mg de flunitrazepam, por un equipo de 2 cirujanos y 1 radiólogo. Para alojar el imán padre, la estenosis – si estaba presente – fue dilatada temporalmente con un catéter balón con guía de alambre (CRE Ballon Catheter, Boston Scientific), permitiendo el paso de un endoscopio o tubo de íleo.
Luego se insertó un alambre guía de 0,045 a 0,049 pulgadas (Pathwinder, Created Medic Co, Ltd), a través del cual se pasó el imán (Fig. 1B). Un catéter con canastilla de litotricia (CCL) (Lithotripsy Basket Catheter; Zeon Medical), generalmente usado para litotricia biliar, se usó para llevar los imanes a los órganos elegidos.
El CCL se usó directamente a través del alambre guía o bajo guía endoscópica. Para el tracto intestinal distal, que no podía ser alcanzado con el CCL, se usó un imán externo poderoso para ubicar el imán interno. Si el tracto intestinal estaba completamente obstruido, se insertó un tubo de íleo o un endoscopio desde el ano o desde una gastrostomía o enterostomía preexistente.
Seguidamente, se abordó el tracto intestinal accesible más cercano al lado oral con un alambre guía, sobre el que se colocó el imán usando el CCL. La guía se dobló aproximadamente a 30 grados, a 10 cm de la punta, para que el imán no se saliera espontáneamente por peristalsis, lo que podría ocurrir si el imán se moviera hacia la punta del alambre guía. Después de confirmar que los imanes se habían adsorbido en la posición elegida, el endoscopio y el alambre guía fueron removidos, finalizando el procedimiento.
> Manejo postoperatorio
La posición del imán fue controlada diariamente con radiografías simples de abdomen. La completitud de la anastomosis fue identificada por el cambio en la posición de los imanes. Los imanes pasaron espontáneamente a través del ano; si la excreción de los imanes era lenta, los mismos fueron recuperados endoscópicamente.
Luego que los imanes fueron recuperados, la anastomosis fue observada unos días después usando un endoscopio. Si era esperable una re-estenosis y era considerado necesario prevenirla, se colocó un tubo de íleo para mantener permeable la anastomosis, o se efectuó una dilatación con balón regularmente. La cantidad requerida de dilataciones dependió del diámetro de la anastomosis.
> Seguimiento
Si no se presentaron síntomas después de completar las dilataciones, no se requirieron exámenes regulares distintos a los de la enfermedad subyacente.
> Presentación de casos
Yeyunocolostomía (Caso 1) (Fig. 1e)
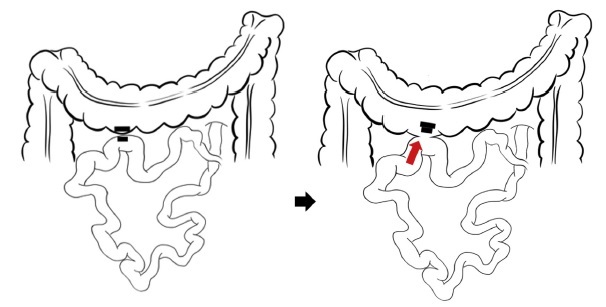
- Figura 1e: esquema de la paciente 1 (yeyunocolostomía con ACM)
La paciente tenía cáncer cervical con recidiva en los ganglios linfáticos para-aórticos y múltiples metástasis pulmonares (después de una histerectomía radical y anexectomía bilateral, con linfadenectomía pelviana bilateral). Un nódulo diseminado causó un íleo refractario.
Dado que la cirugía no estaba indicada debido al severo estado funcional, se prefirió una derivación usando ACM (Fig. 2A). El tubo de íleo insertado preoperatoriamente fue reemplazado con un alambre guía, y se usó el CCL para llevar un imán hijo de 17,5 mm al yeyuno, a 150 cm del ligamento de Treitz. Un imán padre de 22,5 mm fue llevado al colon transverso usando un colonoscopio, y se confirmó la adsorción de ambos imanes (Figs. 2B y 2C).
Se colocó un tubo de íleo en el yeyuno para su descompresión, finalizándose el procedimiento. La anastomosis fue creada 11 días después (Fig. 2D). Se efectuaron dilataciones con balón a intervalos de 7 días para prevenir la re-estenosis.
Después de 8 dilataciones se produjo una perforación anastomótica y se realizó cirugía de emergencia (drenaje abierto e ileostomía). Los hallazgos intraoperatorios revelaron la presencia de la perforación anastomótica. El curso postoperatorio fue sin incidentes, y la paciente egresó a los 120 días de la ACM.
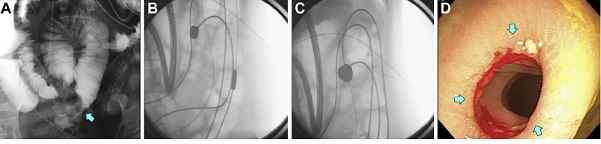
- FIGURA 2: Anastomosis intestinal grande vía intestino delgado. (A) Estenosis (flecha) debida a diseminación de nódulos en el íleon terminal antes de la ACM. (B) El endoscopio y CCL se combinaron para transportar los imanes desde el lado oral al yeyuno, y desde el lado anal al colon transverso. (C) Ambos imanes fueron adsorbidos. (D) Vista endoscópica de la anastomosis completada (flecha) (20 días después de la ACM).
Colorectostomía (Caso 5) (Fig. 2e)
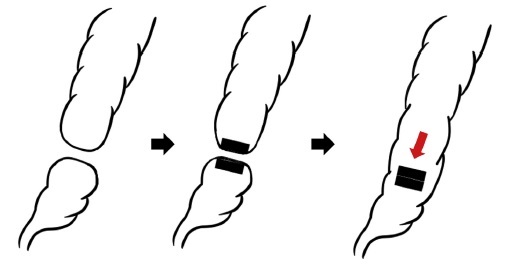
- Figura 2e: esquema del paciente 5 (colorectostomía con ACM)
Paciente de 59 años. Se realizó drenaje abierto y colostomía transversa en asa por perforación diverticular sigmoidea y peritonitis. Seis meses después se realizó sigmoidectomía (con preservación de la colostomía) y el paciente fue derivado por estenosis completa de la anastomosis en el colon sigmoides (Fig. 3A).
Un imán hijo de 17,5 mm fue colocado en el colon sigmoides desde la colostomía transversa, usando un tubo de íleo. Un imán padre, del mismo tamaño, fue colocado en el recto utilizando un endoscopio a través del ano, y ambos imanes fueron adsorbidos (Figs. 3B y 3C). La anastomosis fue inducida 7 días después. Dado que la misma era lo suficientemente grande, no fue necesario hacer dilataciones.; por lo tanto, el tratamiento quedó completado. Dos meses después, se cerró exitosamente la ostomía.
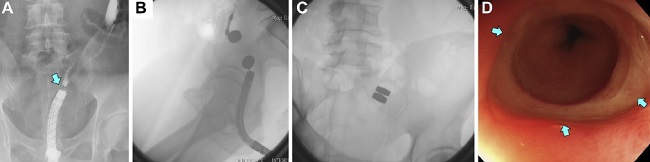
- FIGURA 3: Anastomosis en el intestino grueso vía el intestino grueso. (A) Estenosis completa de la anastomosis en el colon sigmoides (flecha). (B) El imán fue transportado desde la colostomía transversa por un tubo de íleo. Un imán padre fue transportado desde el ano hasta el sitio designado, con un endoscopio gastrointestinal bajo. (C) Ambos imanes fueron adsorbidos. (D) Vista endoscópica de la anastomosis completada (14 días después de la ACM).
Yeyunoyeyunostomia (Caso 10) (Fig. 3e)
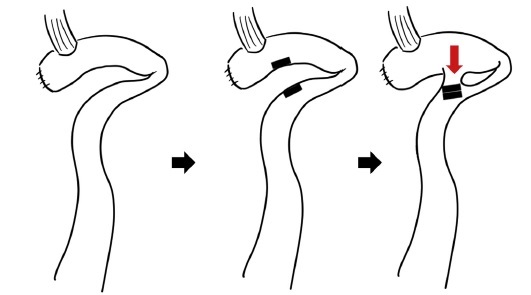
- Figura 3e: esquema del paciente 10 (yeyunoyeyunostomía con ACM)
Paciente de 64 años. Se efectuó una gastrectomía total abierta por cáncer gástrico. Se realizaron dilataciones endoscópicas repetidas con balón para una estenosis no anastomótica del yeyuno proximal, pero no fueron efectivas (Fig. 4A).
Se consideró una reoperación con anastomosis intratorácica como altamente invasiva. El imán padre no pudo pasarse a través de la estenosis; por lo tanto, se usó un catéter con balón para dilatar, a una presión de 4 atm a 16 mm, por 3 minutos.
Un imán padre de 17,5 mm fue transportado desde el lado anal de la estenosis usando un CCL. Seguidamente, un imán hijo de 17,5 mm fue colocado al final del yeyuno proximal y ambos imanes fueron adsorbidos (Figs. 4B y 4C).
La anastomosis se desarrolló 21 días después, lo que fue confirmado por endoscopía alta (Fig. 4D). Se realizaron 3 dilataciones endoscópicas para prevenir la estenosis. El tratamiento fue completado sin reaparición de los síntomas.
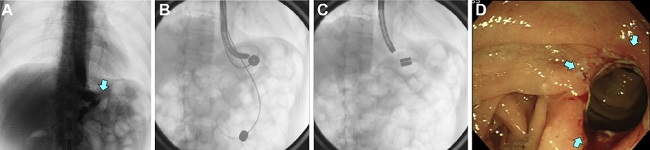
- FIGURA 4: Anastomosis en el intestino delgado vía el intestino delgado. (A) Estenosis no anastomótica del yeyuno elevado (flecha). (B) Antes de la dilatación del segmento estenótico el imán padre fue transportado desde el lado oral al lado anal de la estenosis con un CCL. Se combinó un endoscopio y un CCL para transportar el imán hijo al lado oral de la estenosis. (C) Ambos imanes fueron adsorbidos. (D) Vista endoscópica de la anastomosis completada (flecha), 25 días después de la ACM.
| Resultados |
> Características de los pacientes
Catorce pacientes fueron sometidos a una ACM; 9 fueron hombres y 5 mujeres. La edad promedio fue de 65 años (rango: 39 a 82 años). Tres, 6 y 5 pacientes tenían puntajes de 2, 3 y 4, respectivamente, de la clasificación del estado físico de la American Society of Anesthesiologists (ASA).
La estenosis responsable para la indicación de la ACM se ubicó en el intestino delgado en 9 pacientes, en el intestino grueso en 3, en el duodeno en 1, y en el esófago en 1. Once (73%) y 3 (27%) estenosis fueron benignas y malignas, respectivamente.
Las anastomosis fueron enteroenterostomías en 6 pacientes, colorectostomías en 3, enterocolostomías en 3, gastroenterostomía en 1, y esofagogastrostomía en 1. Diez pacientes tuvieron anastomosis latero-laterales y 4 término-terminales. Los diámetros de los imanes (hijo/padre) fueron 17,5 / 17,5 mm en 11 pacientes, 17,5 / 22,5 mm en 2 pacientes, y 15 / 15 mm en 1 paciente.
> Resultados quirúrgicos
Se logró el éxito técnico en todos los 14 casos (100%). Cada procedimiento consumió un promedio de 44 minutos (rango: 10 a 143 minutos), que fueron medidos desde el momento de la inserción del endoscopio hasta el momento de su remoción. La duración de la creación de la anastomosis, en promedio, fue de 13 días (rango: 5 a 24 días).
El tiempo promedio hasta la iniciación de la ingesta oral fue de 13 días (rango: 1 a 34 días) comenzando desde el día después del procedimiento de ACM si los pacientes tenían una ostomía y, de lo contrario, comenzando desde el día después de la creación de la anastomosis, usando nutrición parenteral total como nutrición suplementaria. La media de la duración de la estadía hospitalaria fue de 36 días (rango: 14 a 120 días).
La re-estenosis anastomótica, una complicación relacionada con la ACM, ocurrió en 2 pacientes (14%), y la perforación anastomótica debida a dilatación con balón para prevenir la re-estenosis, ocurrió en 1 (7%). La dilatación con balón para prevenir la re-estenosis se efectuó en 8 pacientes (57%; hubo superposición con la dilatación por tratamiento). Cuatro pacientes (29%) fallecieron por empeoramiento de la enfermedad subyacente. El promedio del seguimiento alejado fue de 34 meses (rango: 6 a 57 meses).
| Discusión |
Este estudio reveló que el uso de la ACM, sin la necesidad de anestesia general, para crear una anastomosis gastrointestinal, es seguro y factible. El mayor beneficio de la ACM es que permite la creación de una anastomosis gastrointestinal similar a la quirúrgica, con mínima invasividad, y sin requerimiento de anestesia general.
En consecuencia, en la institución en donde se desempeñan los autores, la ACM está indicada para los pacientes en los que se requiere una derivación gastrointestinal, independientemente de la enfermedad primaria subyacente.
El procedimiento es una alternativa al tratamiento inicial en pacientes con severas complicaciones que no pueden tolerar la cirugía, o la reoperación en pacientes con antecedentes de cirugía abdominal complicada, o complicaciones postoperatorias.
Con respecto a la región gastrointestinal, aunque se conocen reportes de ACM exitosas en estudios con animales [7-13], hay pocos reportes disponibles sobre la utilidad y factibilidad de la ACM para la anastomosis gastrointestinal en los seres humanos.
Graves y col. [14], reportaron que la anastomosis intestinal en 5 pacientes, similar a la obtenida mediante cirugía, podía ser realizada con seguridad usando la ACM; no obstante, su estudio estuvo limitado por el tamaño pequeño de la muestra, y los imanes fueron colocados durante una cirugía abierta.
Esos autores concluyeron que la colocación de imanes bajo procedimientos laparoscópicos, endoscópicos o fluoroscópicos, podría ser deseable. Chopita y col. [15], efectuaron una derivación gastroyeyunal usando ACM, con una endoprótesis metálica insertada endoscópicamente en 15 pacientes con obstrucción maligna, y tuvieron resultados favorables, con éxito técnico en 13 pacientes (89%) y complicaciones menores (desviación de la endoprótesis, obstrucción) en 4 (31%).
Van Hooft y col. [16] realizaron un procedimiento similar en 18 pacientes con obstrucción gástrica maligna, y reportaron éxito técnico en 12 pacientes (67%); 1 paciente experimentó una complicación grave (perforación por la endoprótesis), y 3 tuvieron complicaciones menores (migración de la endoprótesis).
Sin embargo, el estudio fue terminado prematuramente. Esos autores reportaron que la ACM era factible, pero la inserción de la endoprótesis metálica podría no estar recomendada [16]. Estos 2 últimos estudios se limitaron a la derivación gastroyeyunal por estenosis maligna del tracto gastrointestinal alto, y requirieron la inserción de una endoprótesis metálica.
Una de las causas de la no popularidad de la ACM como un método para la creación de una anastomosis gastrointestinal, es la dificultad para colocar los imanes en el intestino distal [9].
Para resolver este problema, los autores transportan los imanes usando una combinación de CCL, tubo de íleo, y endoscopios, alcanzando un éxito del 100% en todas las regiones gastrointestinales. Los imanes fueron trasportados suavemente usando el alambre guía y el CCL bajo guía fluoroscópica en los pacientes en los que el transporte no podía hacerse endoscópicamente.
En los pacientes con una ostomía, el uso de la misma como un punto de entrada permite una colocación más fácil de los imanes. En un estudio previo [14], se hizo un agujero en el centro de los imanes adsorbidos durante la laparotomía, obteniéndose una descompresión inmediata. Fue difícil crear un orificio de descompresión durante los procedimientos endoscópicos y fluoroscópicos y, de necesitarse una descompresión, se colocó un tubo de descompresión en el lado oral de los imanes adsorbidos, en el presente estudio.
Los imanes son recuperados generalmente después de la defecación, o endoscópicamente en ausencia prolongada de una excreción. Cuando se realiza una derivación para el íleo, es difícil recuperar los imanes si se dejan caer en el tracto del asa ciega. Para prevenir eso, se coloca un imán más pesado en el lado anal de la anastomosis, y los imanes adsorbidos caen hacia ese lado.
La completitud de la anastomosis se alcanzó entre los 8 y 24 días para los diferentes órganos involucrados. La duración de la anastomosis según el tamaño de los imanes no difirió. Reportes previos habían señalado la recuperación de los imanes después de 2 a 8 semanas [14] para las anastomosis del intestino delgado, y de 7 a 10 días [15] para las anastomosis gastroyeyunales, lo que no tuvo mayores diferencias con los actuales resultados. Once pacientes (79%) con puntaje ASA 3 o mayor, tuvieron resultados favorables en este estudio.
La ACM fue realizada como el tratamiento inicial en 3 pacientes (21%) con estenosis maligna y un puntaje ASA 4, y la ingesta oral fue posible después de una ACM exitosa. Considerando el bajo estatus funcional causado por la progresión de la enfermedad subyacente y la ascitis masiva, la ACM mínimamente invasiva puede ser una alternativa a la cirugía paliativa de derivación gastrointestinal. Otra ventaja sobre la cirugía, es que puede comenzarse la quimioterapia casi inmediatamente después del procedimiento, sin un período de espera.
Las complicaciones encontradas fueron la re-estenosis en 2 pacientes (14%) y la perforación anastomótica en 1 paciente (7%), debida a la dilatación con balón para prevenir la re-estenosis. En 2 casos de re-estenosis, se realizó regularmente dilatación con balón, con mejora de la estenosis; no obstante, un paciente experimentó perforación anastomótica con peritonitis generalizada inmediatamente después de la octava dilatación, requiriendo una cirugía de emergencia.
Pichakron y col. [7], efectuaron un análisis histopatológico de la gastroyeyunostomía con ACM en un modelo experimental con animales, y presentaron un mecanismo para la ACM. La necrosis del material intercalado fue evocada durante la primera semana, la anastomosis se hizo patente en la segunda semana, y la fibrosis alrededor de la anastomosis se volvió prominente. Para la 6º semana, la re-epitelización había ocurrido a través de la fibrosis e inflamación.
En la experiencia de los autores de este trabajo, la re-estenosis en los pacientes que fueron sometidos a ACM, fue causada por una fibrosis y cicatrización excesivas del sitio anastomótico, que pudo no haber quedado cubierto completamente por la mucosa después de la remoción del imán. En el paciente 1, se considera que la perforación fue causada por una dilatación excesiva con el balón, antes de haberse alcanzado la epitelización completa a las 8 semanas después de realizada la anastomosis.
Dada la perforación anastomótica ocasionada por la dilatación con balón, los autores proporcionaron una medida preventiva para la re-estenosis. Si la anastomosis era grande, no se realizó la dilatación preventiva con balón, o se colocaron algunos tubos de íleo según el diámetro de la anastomosis. A partir de eso no hubo más re-estenosis.
Cuando se efectuó dilatación con balón, se limitó a una dilatación a baja presión, por aproximadamente 2 meses después de completada la anastomosis, y la dilatación con balón a alta presión fue realizada después de alcanzarse la epitelización completa.
Otras complicaciones, tales como la filtración anastomótica, lesión de otros órganos, y perforación a causa de la presencia de los imanes por largo tiempo, no fueron observadas. Para la ACM, la comprensión anatómica precisa de la presencia de objetos interpuestos entre órganos, usando la TCm preoperatoria, es particularmente importante para evitar la lesión de otros órganos. En algunos pacientes, el imán puede adsorberse en el lado mesentérico, por lo que es esperable que interfiera con el flujo sanguíneo intestinal. Sin embargo, no se observaron complicaciones.
Dado que el flujo marginal es abundante, los autores piensan que la interposición de vasos pequeños entre los imanes no es problemática. La ACM puede ser efectuada con seguridad incluso en pacientes con una distancia de 5 cm entre los órganos elegidos, determinada por la TCm preoperatoria. La distancia podría acortarse mediante procedimientos endoscópicos o fluoroscópicos y la peristalsis intestinal, durante el procedimiento. Sobre la base de esta experiencia, consideran que la limitación específica de la distancia es de aproximadamente 5 cm.
Como una limitación de este estudio, la ACM debería ser realizada por equipos bien entrenados, porque se requieren técnicas específicas para la colocación de los imanes. El uso generalizado de ACM requiere el desarrollo de un dispositivo dedicado, que requerirá la simplificación y estandarización del procedimiento.
Además, en ausencia de una vía nutricional suplementaria, es un desafío forzar la nutrición parenteral hasta que se complete la anastomosis. Por otra parte, la resonancia magnética nuclear está contraindicada porque hay un imán presente en el cuerpo. Dado que éste fue un estudio retrospectivo unicéntrico con un tamaño de muestra pequeño, se requieren estudios futuros con un mayor número de pacientes
| Conclusiones |
La ACM sin anestesia puede ser una alternativa valiosa de la cirugía para la obstrucción gastrointestinal
Comentario y resumen objetivo: Dr. Rodolfo D. Altrudi
§ Atraer y retener en la superficie de un cuerpo moléculas o iones de otro cuerpo