| Introdução |
> Eixo intestino-pele
A principal interface do organismo com o ambiente ocorre nas superfícies cobertas por células epiteliais, onde a pele e o trato gastrointestinal têm grande relevância. O intestino é considerado o maior órgão imune do ser humano, uma vez que, exposto a incontáveis antígenos, possui uma rede única e complexa de mecanismos imunológicos e não imunológicos, a chamada barreira mucosa gastrointestinal.1
A integridade da barreira intestinal, juntamente com a ação do muco, células imunológicas, imunoglobulina A e peptídeos antimicrobianos produzidos pelos enterócitos, impede a entrada de bactérias na corrente sanguínea, mantendo a homeostase local e em tecidos a distância, incluindo a pele. A lâmina própria do intestino é o maior local de produção de anticorpos do organismo, onde se encontram cerca de 80% de células B ativadas.2
Nesse contexto, o trato intestinal também pode ter impacto significativo na homeostase geral; sabe-se que a população bacteriana que habita o trato gastrointestinal (TGI) é imensa: o corpo humano transporta cerca de 390 trilhões de microrganismos nos seus intestinos (3,9x1013 – 1,3 vez maior do que o número total de células humanas no corpo [3,7x1013]). São mais de 15.000 espécies de 900 gêneros bacterianos diferentes.3,4
Esses microrganismos atuam em equilíbrio dinâmico, exercendo funções que impactam a imunidade local e sistêmica, como:5,6
- Inibição da proliferação e adesão de microrganismos oportunistas ou patógenos;
- Maior síntese de mucinas;
- Estímulo à síntese de IgA;
- Estímulo de células da imunidade inata do intestino (células dendríticas);
- Modulação da resposta inflamatória Th1;
- Inibição da resposta alérgica do tipo Th2;
- Além de atuar na síntese de vitaminas (biotina, vitamina K2), atua também na síntese dos ácidos graxos de cadeia curta (SCFAs) butirato, acetato e propionato, que desempenham papel anti-inflamatório na medida em que promovem a inibição de NF-kB e a proliferação de Treg;
- Influência em microbiomas de outros órgãos: vias respiratórias, cavidade oral, mucosa vaginal e pele, através do tecido linfoide (GALT) e permeabilidade de barreira, impedindo a penetração de toxinas e outras noxas na corrente sanguínea.
A figura 1 sumariza o papel da eubiose intestinal na homeostase sistêmica.7
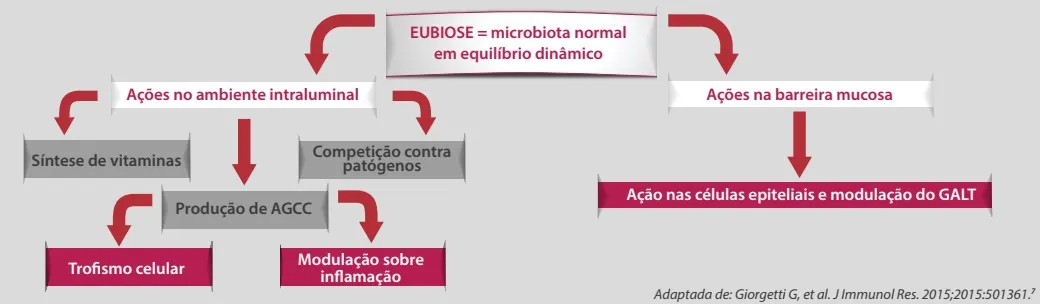
 Figura 1. Eubiose intestinal e sua repercussão.
Figura 1. Eubiose intestinal e sua repercussão.
> Desbiose e dermatoses
A disbiose intestinal é caracterizada por alterações quanti e qualitativas dos microrganismos da sua microbiota, com aumento das bactérias patogênicas. São múltiplos os fatores que podem desencadeá-la: dietéticos, uso de antibióticos e mesmo doenças intestinais.8
Os quadros de disbiose levam a um fenômeno denominado leaky gut (intestino permeável), em que há um prejuízo da função da barreira intestinal, com perda da barreira enterocitária e redução da produção dos AGCC; haverá aumento da penetração sistêmica de bactérias, antígenos e bacteriocinas, e consequente ativação imune e inflamação.9
O impacto da disbiose vem sendo estudado em diversas doenças inflamatórias, degenerativas, alérgicas e autoimunes. Na dermatologia, a doença mais estudada é a dermatite atópica, mas outras dermatoses como a acne, psoríase, rosácea etc. também reúnem evidências de uma influência da disbiose intestinal, sumarizadas no quadro 1. 10-13


Quadro 1. Microbiota intestinal em dermatoses.
> Microbioma intestinal e dermatite atópica
A dermatite atópica é uma doença eczematosa multifatorial, em que fatores genéticos determinam alterações de barreira cutânea (clinicamente caracterizadas por prurido e xerose) e alterações de resposta imunitária humoral e celular. Com um curso crônico, manifesta-se primariamente na infância, no primeiro trimestre de vida, e, em 30% dos casos, está associada a outras doenças: rinite alérgica, asma brônquica e alergia alimentar. Os períodos de manifestação de cada uma delas compõem a marcha atópica, conforme o gráfico 1.14
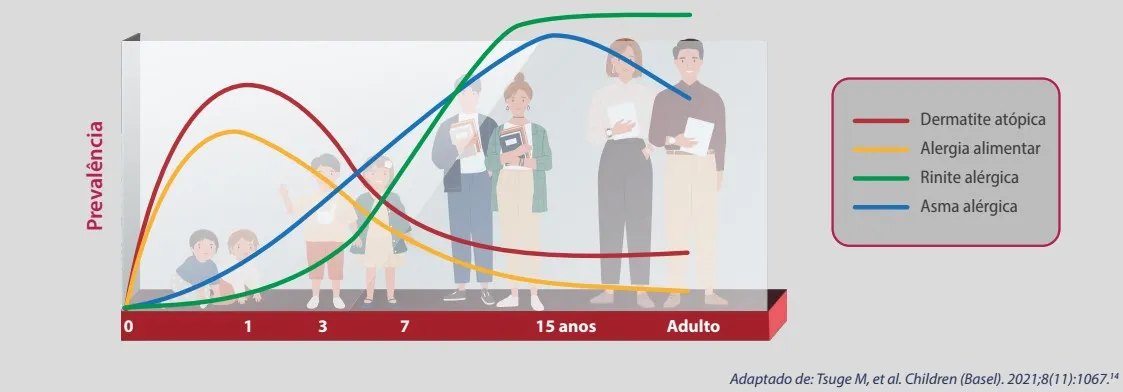
 Gráfico 1. Períodos de manifestação das doenças relacionadas a atopia: a marcha atópica.
Gráfico 1. Períodos de manifestação das doenças relacionadas a atopia: a marcha atópica.
Há evidências de que alterações na microbiota intestinal seriam um dos elementos impeditivos e fundamentais para o desenvolvimento da tolerância imunológica, e a dermatite atópica tem maior comprovação clínica e experimental do impacto da microbiota no desenrolar da doença.15
Pacientes com dermatite atópica possuem menor alfa diversidade de bactérias, quando comparados a indivíduos sem eczema.16 O microbioma intestinal alterado permite a penetração de alimentos mal digeridos, micróbios e toxinas, e está associado à disfunção da barreira epitelial em pacientes com dermatite atópica. O microbioma intestinal alterado desencadeia a inflamação Th2, resultando em maior inflamação e consequente prurido, com piora da ruptura da barreira da pele, tornando-se um círculo vicioso.17
Sabe-se que crianças em aleitamento materno têm maior número de bifidobactérias em seu TGI (efeito bifidogênico); esse gênero de bactérias, assim como os lactobacilos, chega a representar a maioria da microbiota intestinal.18
Por esses motivos, o uso oral de probióticos parece ser uma estratégia adequada para restabelecer a diversidade bacteriana e melhorar a função de barreira intestinal, reduzindo, assim, esse gatilho inflamatório.18
Evidências estão se acumulando para um efeito protetor dos probióticos contra a ocorrência de eczema no início da vida, mas não se sabe se isso é devido a um atraso no início dos sintomas ou à prevenção primária.19,20
Dados publicados sobre o acompanhamento de um estudo randomizado, controlado por placebo, com pacientes em uso diário de probióticos a partir de 35 semanas de gestação até os 2 anos de idade, demonstraram que o Lactobacillus rhamnosus HN001 (HN001) protegeu contra o desenvolvimento de eczema nessa faixa etária, assim como contra a sensibilização atópica aos 6 anos de idade. O grupo controle, com tratamento com Bifidobacterium lactis HN019 (HN019), não demonstrou efeito significativo.20
Essas descobertas para HN001 são comparáveis às dos estudos finlandeses de L. rhamnosus GG, que mostrou proteção notavelmente semelhante aos efeitos nas faixas etárias de 4 e 7 anos.21
Um estudo norueguês que interveio com uma combinação de probióticos nos períodos pré e pós-natal em mães também encontrou proteção persistente contra eczema até aos 6 anos de idade.22
Finalmente, um estudo avaliando a suplementação de L. rhamnosus HN001 na primeira infância foi associado a reduções significativas (p=0,015) na prevalência de eczema em crianças de 12 meses a 11 anos de idade; os resultados também foram significativos para sintomas respiratórios. Para a prevalência ao longo da vida, o HN001 foi associado a uma redução significativa em todo o espectro da doença alérgica, demonstrando, pela primeira vez, uma intervenção probiótica precoce reduzindo, na primeira década de vida, todo o espectro da doença alérgica. O comparador não teve efeito significativo sobre os parâmetros avaliados.23
| Conclusão |
Há várias evidências de que a microbiota intestinal é capaz de causar impacto na saúde de seu hospedeiro, tanto local como sistemicamente. O restabelecimento da eubiose, com o uso de probióticos, tem um potencial de benefícios que vem sendo estudado em vários campos da medicina, e, na dermatologia, a doença mais estudada é a dermatite atópica.
De todos os probióticos que vêm sendo estudados para a prevenção e controle da marcha atópica, o L. rhamnosus HN001 foi o primeiro a demonstrar, em um estudo randomizado duplo-cego comparativo, a capacidade de atuar reduzindo significativamente as manifestações da doença atópica na primeira década de vida.



