La Sociedad Argentina de Vacunología y Epidemiología (SAVE) elaboró un documento con recomendaciones para los equipos de salud para el abordaje de la Fiebre Hemorrágica Argentina (FHA). En concreto, se reportaron 75 casos sospechosos, de los cuales 11 ya fueron confirmados, la mayor cifra de los últimos 10 años. A continuación el documento de la sociedad científica.
La Fiebre Hemorrágica Argentina (FHA) también llamada Mal de los rastrojos es una enfermedad viral grave causada por el virus Junín (V.J.) perteneciente a la familia Arenaviridae.
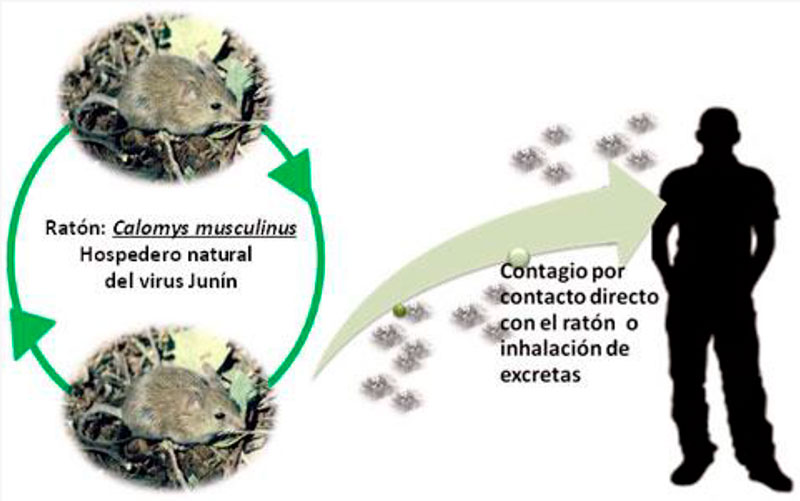
Los arenavirus infectan a un número limitado de especies de pequeños roedores. El ratón de campo Calomys musculinus, conocido también como ratón maicero, laucha manchada, laucha del maíz, ha sido identificado como el reservorio principal del VJ. El roedor pequeño construye sus nidos en campos cultivados, en zona de malezas, alambrados, caminos, aguadas, banquinas, huertas y malezas en los fondos de las casas rurales. Este vector sufre infección crónica asintomática y elimina el virus a través de saliva, orina, sangre. El hombre adquiere la enfermedad por contacto con roedores infectados, a través de la inhalación de aerosoles de las excretas, (la vía más importante) o por contacto de las mismas con pequeñas excoriaciones de piel o mucosas, siendo la transmisión interhumana muy infrecuente.
Epidemiología
El área afectada en ese momento por brotes anuales y estacionales se circunscribía a cuatro partidos de la provincia de Buenos Aires, con una superficie de 16.000 km2 y una población en riesgo estimada en 270.000 habitantes. A través de los años, se han producido sucesivas extensiones del área endémica llegando a ocupar una superficie de 150.000 Km2, con una población en riesgo estimada en 5.000.000 millones de habitantes, área que comprende; Noroeste de la provincia de Buenos Aires, sureste de la provincia de Córdoba, sur de la provincia de Santa Fe y noreste de la provincia de La Pampa.
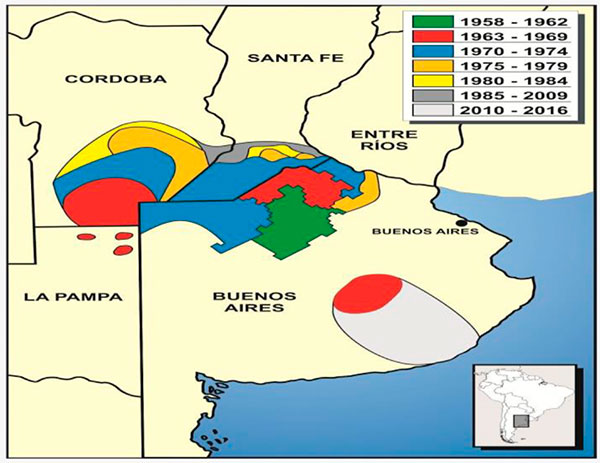
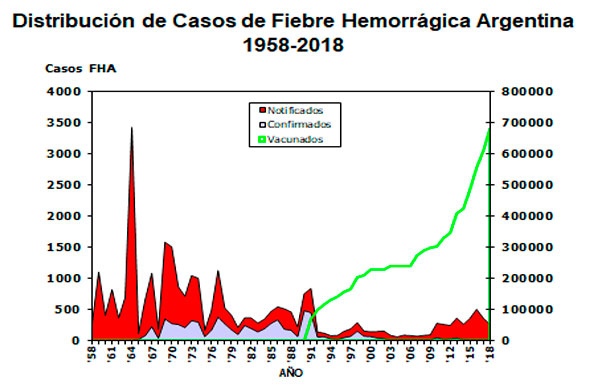
Desde la introducción de la vacuna la incidencia de la enfermedad disminuyó significativamente, pero en los últimos años se han presentado brotes en áreas endémicas.
Situación epidemiológica de la Provincia de Buenos Aires
Entre SE 1 y 22 en la Provincia de Buenos Aires se notificaron 75 casos sospechosos de FHA, de los cuales 11 casos fueron confirmados (15%), 27 descartados y 37 casos permanecen como casos sospechosos con resultados no conclusivos, a la espera de segundas muestras para completar estudios serológicos. Cabe destacar que es el mayor número de casos confirmados registrado en los últimos 10 años.
Los partidos de San Nicolás, Pergamino y Ramallo en donde se han confirmados los casos de FHA, corresponden al área endémica de la enfermedad y donde es esperable la aparición de casos esporádicos. En cuanto el tratamiento, sólo tres de los casos confirmados no recibieron transfusión con plasma inmune de convaleciente y ninguno de los 11 casos tenía antecedentes de vacunación con Candid#1.
Uno de los casos confirmados falleció en SE 15. Se trató de una mujer de 42 años de edad, que tenía como antecedente epidemiológico, haber participado de un evento social en una zona rural del partido de Ramallo. Para el mismo período de 2021 se habían notificado 15 casos sospechosos y un caso confirmado en el municipio de San Nicolás (*)
(*) Vigilancia de Fiebre Hemorrágica Argentina (FHA) Semana del 29/05 al 4/06 -2022 Dirección Provincial de Epidemiología Prevención y Promoción de la Salud.
La FHA afecta especialmente a quienes residen, visitan o trabajan en el medio rural, predominantemente agricultores del sexo masculino, lo que indica que esta actividad es un factor de riesgo determinante de la infección al exponerse a material contaminado con excretas de roedores Es más frecuente en el sexo masculino, en el grupo de 15 y 60 años.
Tiene un comportamiento estacional, con su mayor incidencia principalmente de marzo a octubre.
Entre 2001 y 2010 se han producido cambios relativos en el patrón epidemiológico clásico (género, edad, ocupación y distribución rural -urbanade la FHA) que, en algunos casos, se han atribuido a las intervenciones sanitarias descritas (por ejemplo, aumento de la proporción en mujeres por haber centrado la vacunación en varones), mientras que otros, como la emergencia en localidades no históricas y no endémicas, urbanos y suburbanos.
Actualmente se describen 3 escenarios:
· Escenario clásico: abarca el área endémica y coincide geográficamente con el complejo agroindustrial cerealero de exportación del país (zona núcleo). El lugar de contagio y de residencia de los casos se ubican en este territorio.
· Escenario emergente-reemergente: paisajes donde acontecieron cambios en la organización social de la producción que lo hacen compatible con el escenario clásico.
- Emergente: los casos residen y se contagian fuera del área endémica pero que no viajaron en las tres semanas previas a enfermar. Áreas nuevas de transmisión.
- Reemergente: los casos residen en áreas históricas de transmisión donde no se habían notificado casos en los diez años previos.
· Escenario viajero: los casos transitaron por un escenario clásico o emergente-reemergente, pero no residen en ellos. En este escenario se unen viajeros y trabajadores que migran estacionalmente o transitan eventualmente para emplearse en tareas asociadas al complejo agroindustrial.
Manifestaciones clínicas
Es una enfermedad viral aguda grave- Las manifestaciones clínicas van desde formas leves a graves.
Periodo de Incubación: oscila entre 1 y 2 semanas.
Periodo de Estado: el inicio de la enfermedad es insidioso siendo los síntomas más comunes en el período de invasión: síndrome febril, decaimiento, hiporexia y cefalea. Se agregan mialgias, lumbalgias, dolorretroocular, mareos, epigastralgias, náuseas y vómitos. Pueden presentarse en este período epistaxis y gingivorragias leves. No hay manifestaciones catarrales ni signos de alteraciones broncopulmonares.
Durante la primera semana pueden observarse en el examen físico facie eritematosa, exantema eritematoso que afecta cuello, parte superior de tronco, axila y cara interna del tercio superior de los brazos observándose con frecuencia petequias aisladas o en ramilletes. Enantema bucofaríngeo caracterizado por un aumento en la red vascular del paladar blando y de la faringe, con petequias y microvesículas. Se observa un ribete gingival y las encías suelen sangrar a la presión siendo frecuentes las gingivorragias o epistaxis espontáneas. En las mujeres es casi constante la presencia de metrorragia.
A nivel ocular es común observar inyección conjuntival y edema periorbitario.
Pueden constatarse bradicardia relativa e hipotensión postural.
Los signos neurológicos son frecuentes, especialmente hacia el final de la primera semana: irritabilidad, somnolencia, temblor fino, ataxia moderada, hiperestesia cutánea, hipotonía muscular e hipo o arreflexia osteotendinosa.
No cursa con hepato o esplenomegalia.
Durante la segunda semana de la enfermedad comienza la mejoría en el 70 a 80% de los enfermos.
En el 20-30% restante se presentan manifestaciones hemorrágicas o neurológicas severas, shock o complicaciones bacterianas.
Se distinguen tres formas clínicas: leve, común y grave y dentro de esta última a su vez 3 formas: hemorrágica, neurológica o mixta.
El período de convalecencia es de duración prolongada, de 1 o 2 meses, con astenia, hipoacusia, trastornos de la memoria, irritabilidad y pérdida transitoria del cabello.
Mortalidad
La mortalidad por FHA sin tratamiento es del 20-30% y con tratamiento adecuado (plasma de convaleciente administrado dentro de los 8 días del inicio de los síntomas) disminuye al 1%.
Diagnóstico

Es una enfermedad de denuncia obligatoria, y de notificación inmediata al sistema de vigilancia nacional SNVS-2 ante caso sospechoso. El diagnóstico puede ser directo aislamiento viral y/ó RT-PCR en una muestra y con pruebas serológicas en 2 muestras pareados con 45-60 días de diferencia (ELISA/ la prueba de neutralización por reducción de placas (PRNT).
Agente Inmunizante vacuna Candid # 1
Es una vacuna viral atenuada parenteral con cepa viva atenuada homónima del virus Junín. Para la obtención de la vacuna se utilizan cultivos de células FRhL-2 (pulmón de feto de monos Rhesus) crecidos con medio MEMNEAA, 10% de suero fetal bovino certificado e irradiado, 3 m M de Lglutamina y neomicina (0,05 mg/l).
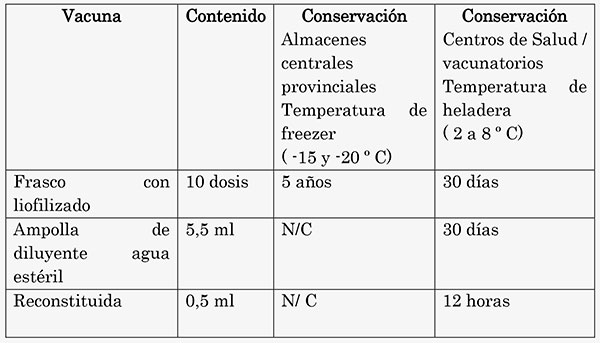
Se presenta en 2 frascos:
-Un producto liofilizado que contiene diez dosis de vacuna
- Una ampolla de diluyente de 5,5 ml de agua estéril
Reconstitución de la vacuna liofilizada
• Los frascos de vacuna serán reconstituidos en el momento de ser utilizados.
• No se debe pasar alcohol u otro desinfectante sobre el tapón de goma de los frascos de vacuna, ya que este procedimiento puede inactivar el virus de la vacuna.
• Utilizando jeringa de 10 ml y aguja 20 Gx1 estériles descartables, agregar lentamente 5,5 ml del agua estéril para inyectables que se entrega con la vacuna, evitando formar espuma. Descartar la jeringa y la aguja utilizadas.
• No agitar ni sacudir el frasco. Rotarlo suavemente y colocarlo en la heladera (NO en el congelador).
• No se utilizará el frasco hasta que el material liofilizado se haya disuelto por completo, cuando el líquido se vea completamente transparente y sin partículas en suspensión.
• Cada frasco contiene 10 dosis de vacuna.
Descarte de los frascos de vacuna utilizada y vencidos
Al finalizar cada jornada de vacunación los frascos vacíos que han sido utilizados deberán ser manipulados, almacenados y transportados hasta su tratamiento y disposición final de acuerdo a las normas vigentes para los residuos patogénicos de cada provincia. Cuando queden frascos de vacuna que hayan superado los plazos de conservación establecidos o no se hayan mantenido con cadena de frío, se procederá al descarte inmediato. Este material debe manejarse con procedimientos idóneos que no importen un riesgo para la salud y que aseguren condiciones de bioseguridad. Se aconseja levantar un acta al momento del descarte de los mismos, para evitar confundir la partida de vacuna a utilizar.
Esquema y vía de administración
Limpiar la piel del sitio de aplicación con solución fisiológica o agua destilada estéril y dejar secar completamente antes de inocular. La vacuna se aplica en una dosis única de 0,5 ml del producto reconstituido, por vía intramuscular, preferentemente en deltoides izquierdo, utilizando agujas 22Gx1 y jeringas descartables de 1 ml.
Incorporación de vacuna Candid #1 al Calendario Nacional
Según Resolución 48/2007 “Incorpórese al Programa Nacional de Inmunizaciones la vacunación contra la Fiebre Hemorrágica Argentina, en el área endémica de la enfermedad de las provincias de Santa Fe, Córdoba, Buenos Aires y La Pampa; e incorpórese la misma al Calendario Nacional de Vacunación”.
Indicaciones y edad
La vacunación está indicada a partir de los 15 años de edad en el área endémica de la enfermedad (un mes antes de actividades de riesgo para seroconversión).
Los estudios de la vacuna se realizaron en la población comprendida entre 15 a 65 años.
Condiciones que deben reunir las personas que deseen vacunarse son:
• Residir, desarrollar actividades o visitar localidades de las cuatro provincias donde se han presentado casos de FHA en los últimos años.
• Hombres y mujeres a partir de 15 años de edad.
• No haber recibido vacuna Candid #1 anteriormente y contar con certificación
• En caso de personas en edad fértil, no estar cursando un embarazo o estar en periodo de lactancia.
• No presentar cuadros agudos o crónicos descompensados.
• No estar recibiendo corticoides sistémicos o presentar cuadros de inmunosupresión.
• No haber recibido otras vacunas y/o gammaglobulinas en el mes previo ni recibirlas en el mes posterior a recibir Candid #1.
Eficacia e Inmunogenicidad
La eficacia de la vacuna Candid #1 para la protección contra la FHA fue del 95,5% (intervalos de confianza del 95%, 82%-99%, p < 0.001)
La inmunogenicidad medida por detección de anticuerpos neutralizantes contra el virus Junín es un marcador subrogante de eficacia para la FHA.
La efectividad estimada en terreno es del 98%.
Los anticuerpos producidos por la Candid # 1 se detectan a partir del decimoquinto día posterior a la vacunación. Para el día 60, más del 90% de los receptores ya habrá desarrollado su respuesta inmune.
Revacunación
No está recomendada.
Aplicación simultaneidad con otras vacunas
A la fecha no se dispone de datos sobre simultaneidad con otras vacunas . Se administra sola, respetando un intervalo mínimo de 30 días antes y después de su inoculación.
Contraindicaciones
· Embarazo: no existen datos en esta población, se contraindica por ser una vacuna viral atenuada
· Lactancia: el virus Junín, como otros arenavirus, se ha aislado de la leche materna en caso de FHA, por este riesgo teórico se contraindicada
· Déficit inmunitario adquirido o congénito
· Enfermedades agudas febriles en curso, afecciones crónicas malignas o descompensadas que puedan afectar la respuesta inmune y terapias inmunodepresoras en el momento de la vacunación.
Efectos adversos
· Generales: dentro de las tres semanas posteriores a la vacunación pueden presentarse cefalea, decaimiento, mialgias, fiebre, náuseas y/o vómitos, dolor retroocular, mareos, lumbalgia y exantema. También pueden presentarse leucopenia leve < 4.000/ mm3, plaquetopenia leve < 150.000 plaquetas/ mm3 y microhematuria.
Estas manifestaciones pueden presentarse aisladas o asociadas. Los eventos desaparecen espontáneamente o con tratamiento sintomático.
· Locales: Pueden presentarse reacciones locales leves que incluyen dolor o molestia en el sitio de inoculación, picazón, eritema y leve induración.
Frente a cualquier evento que se presente luego de la vacunación se deberá reportar como ESAVI.
Todas las personas vacunadas que presenten un diagnóstico presuntivo de FHA serán asistidas para evaluar si requieren internación y tratamiento con plasma inmune.
En las personas en la que se confirme un embarazo en los 3 meses posteriores a la aplicación de Candid #1, deberá notificar al vacunatorio correspondiente y éste, a su vez, notificará al laboratorio productor del INEVH.
Junto a la notificación se deberá enviar una muestra de suero de la persona gestante. Para el seguimiento del binomio, se completará con la ficha perinatal y una muestra de suero al momento del parto (suero de la madre y del cordón del recién nacido) y otra muestra al año del nacimiento. Todas las muestras se enviarán refrigeradas al INEVH Pergamino.
Conclusiones
La FHA es una zoonosis no erradicable debido a que su reservorio, Calomys musculinus se encuentra ampliamente distribuido en la naturaleza. Como el control de los roedores no es practicable y debido a la extensión geográfica del área endémica, los esfuerzos deben estar orientados a la estrategia preventiva (vacuna) y el diagnóstico y tratamiento oportuno. Desde el año 2007, se encuentra incorporada al Calendario Nacional de Inmunizaciones, la vacuna Candid#1 en el área endémica de la enfermedad de las provincias de Santa Fe, Córdoba, Buenos Aires y La Pampa. La implementación de la estrategia de vacunación ha demostrado el impacto en la disminución de la enfermedad, siendo una herramienta de demostrada eficacia y seguridad.