|
Resumen Los autores de este trabajo repasan la fisiopatología del daño cerebral en la IC, describen su efecto sobre la evolución de los pacientes, ofrecen un enfoque diagnóstico y analizan las posibles opciones terapéuticas. |
Introducción
La insuficiencia cardíaca (IC) tiene gran impacto sobre las funciones corporales y es así como otros órganos importantes interactúan con el corazón deteriorado para producir lo que se conoce como síndrome cardiorrenal (1) y síndrome cardiohepático (2). Otra interacción esencial, aunque no tan bien definida, es entre el corazón deteriorado y el cerebro. Los síntomas y signos del sistema nervioso central (SNC) forman parte de las manifestaciones de la IC (3). Estos datos son demostrables en pacientes con IC con fracción de eyección disminuida o conservada (ICFEd e ICFEc, respectivamente) y se pueden hallar tanto en pacientes muy sintomáticos así como en pacientes ambulatorios estables.
Esta interacción se pone de relieve por datos específicos hallados cuando se evalúan ambos órganos y por la mejoría recíproca en su funcionamiento cuando el corazón se recupera. Además, en esta época de crecientes opciones terapéuticas, donde el cumplimiento de las indicaciones es indispensable para el éxito terapéutico, no se puede subestimar la importancia del deterioro cognitivo en la evolución de los pacientes con IC.
► FLUJO SANGUÍNEO CEREBRAL
Tras un primer intento de medir el flujo sanguíneo cerebral (FSC) en 1941, se fueron implementando otros métodos menos invasivos y más exactos (por ej., la gammagrafía y la resonancia magnética (RM) (5,6) que mostraron que el FSC es de aproximadamente 50 ml/min/100 g de tejido cerebral (7) y se mantiene a través de una amplia gama de presiones arteriales medias. Esta estabilidad se logra por la sofisticada autorregulación del SNC (8,9) y se mantiene a través de una serie de factores vasculares y neurógenos, como la liberación de compuestos vasoactivos, la respuesta a los valores cambiantes de CO2 y la respuesta singular de la vasculatura del SNC a las presiones intraluminales fluctuantes (7,10,11).
Datos actuales mostraron que el FSC está en peligro en la IC crónica, la que se sugiere que se asocia con síntomas del SNC (12). Este estado de hipoperfusión no es causado solo por el bajo gasto cardíaco hallado en la IC, porque la autorregulación cerebral también está comprometida en estos pacientes (13). Los valores de CO2 fluctúan en los pacientes con IC aguda o crónica y se relacionan inversamente con las presiones telediastólicas del ventrículo izquierdo, con producción de constricción y dilatación de los vasos del SNC (14,15). Además la reactividad cerebrovascular, medida por la respuesta de la vasculatura cerebral a altos niveles de CO2, también está alterada. Georgiadis et al estimaron las velocidades del FSC mediante Doppler transcraneal (13) y demostraron que mientras los pacientes con IC tenían velocidades de flujo al inicio comparables a las de los controles normales, su respuesta a la hipercapnia estaba mitigada.
El trasplante cardíaco produjo la mejoría significativa del FSC, a menudo acompañada por aumento del funcionamiento cognitivo en los pacientes trasplantados (5,16). La interacción entre el FSC y el implante de un dispositivo de asistencia ventricular izquierda (DAVI) es más compleja. El efecto de los DAVI-IC no fisiológicos es un tema discutido, porque se halló que altera la función endotelial y disminuye significativamente las concentraciones de óxido nítrico, un modulador clave de la autorregulación cerebral (17). Sin embargo, Cornwell et al. (18) demostraron que las velocidades del FSC mostraban variaciones significativas en los DAVI de flujo pulsátil, al contrario de los DAVI-IC o los controles normales y la autorregulación cerebral dinámica se mantenía con ambos dispositivos.(18)
► CAMBIOS ANATÓMICOS Y COGNITIVOS CEREBRALES
La deficiencia cognitiva influye sobre la calidad de vida y el riesgo de complicaciones de los pacientes con IC.
Las alteraciones mentales prevalentes asociadas con la IC comprenden numerosos procesos, entre ellos deficiencias de la atención y el aprendizaje; disminución de la velocidad psicomotora; disminución de la función ejecutiva, tipos específicos de disfunciones de la memoria (23,24). Aunque se pensaba que estas alteraciones se limitaban a los pacientes con IC ancianos y debilitados, datos actuales muestran que también se las encuentra en individuos jóvenes, estables (23,24).
Los pacientes con IC tienen mayor grado de deficiencia cognitiva (DC) en relación con controles emparejados (23,25) y peor desempeño cognitivo tras ajustar para la edad, la situación socioeconómica y la educación y también en relación con pacientes con enfermedades concomitantes importantes, (hipertensión, cardiopatía isquémica) distintas de la IC (23,26). La DC influye sobre la calidad de vida y el riesgo de complicaciones de los pacientes con IC.
Un trabajo (28) informó que la DC era un factor pronóstico de autocuidado escaso en pacientes con IC. Otro estudio (29) mostró que los pacientes con IC y DC eran menos proclives a adherir al tratamiento. Por consiguiente, la DC es un factor de riesgo de decompensación de la IC, mayor frecuencia de rehospitalizaciones e incluso mayor mortalidad (30). En un estudio reciente, Huynh et al. (31) informaron que la DC y la depresión eran fuertes factores pronósticos de rehospitalización y mortalidad a 30 días.
En cuanto al aspecto anatómico, se demostraron cambios en la sustancia gris y la sustancia blanca en pacientes con IC (23,32), que no se limitaron a pacientes muy descompensados, sino que también se hallaron en pacientes con IC estables, ambulatorios, con IC sutil revelada solo por ciertas pruebas cognitivas.
► LA FISOPATOLOGÍA DETRÁS DE LOS CAMBIOS CEREBRALES FUNCIONALES Y ANATÓMICOS
Reducción del FSC y gran carga de riesgo cardiovascular. El mecanismo del daño cerebral en la IC es multifactorial y aún no se conoce bien (Figura). Las estructuras cerebrales profundas carecen de colaterales, están irrigadas por las arterias penetrantes profundas o se encuentran en la intersección irrigada por las arterias cerebrales media y anterior y por lo tanto están expuestas a fenómenos de flujo sanguíneo escaso. Por eso son proclives a agresión isquémica cuando sufren hipoperfusión, como sucede habitualmente en los estados con disminución del gasto cardíaco (34).
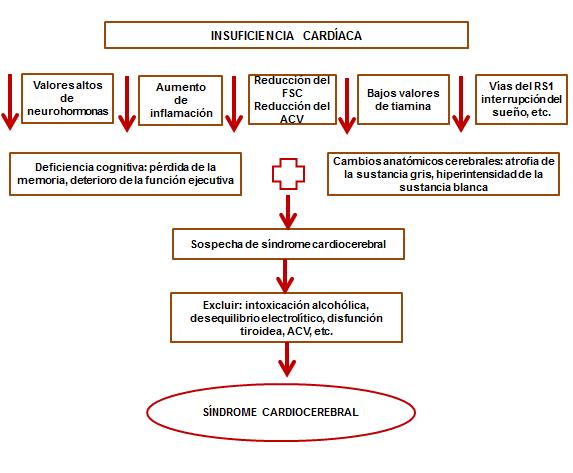
Figura. Lesión cerebral inducida por insuficiencia cardíaca: características, fisiopatología y enfoque. FSC: flujo sanguíneo cerebral, ACV: accidente cerebrovascular, RS1: receptor sigma 1. Elaborado sobre el contenido del artículo de Havakuk et al.
Por eso, diferentes investigadores consideraron que el FSC en peligro era el principal factor causal (32,35). Sin embargo, también se hallaron lesiones de la sustancia blanca (36) y DC(37) en pacientes ICFEc. Considerando el aumento de la rigidez arterial y la disminución de la reserva de vasodilatación hallada en la ICcFE (38), se podría pensar que el FSC estaría disminuido. Sin embargo, dado el gasto cardíaco normal en la población con ICFEc (39), también es posible que el FSC esté conservado.
Además, la disminución del FSC no puede ser la explicación en el caso de pérdida de sustancia gris cortical, donde la vasculatura es abundante y, en cambio, la carga de riesgo cardiovascular se considera el principal responsable (23). Además, a pesar de las características similares de daño cerebral, datos actuales mostraron que pacientes con IC tenían pérdida de la sustancia gris en regiones específicas mucho más extensa que la observada en pacientes con cardiopatía isquémica o en controles sanos (23).
Asimismo, aunque las hiperintensidades de sustancia blanca antes se consideraban consecuencia del envejecimiento o del aumento de la carga de riesgo cardiovascular (41), fueron significativamente más prevalentes en pacientes con IC, incluso tras corregir para la edad y la presencia de cardiopatía isquémica y sus factores de riesgo (32). Es así que parece que aunque hay una fuerte asociación entre la disminución del FSC o el aumento de la carga de riesgo cardiovascular y la gran prevalencia de daño cerebral observada en la IC, no explican totalmente estos datos.
♦ El eje neurohormonal
El eje neurohormonal probablemente interviene en la interacción entre la IC, la cognición y los cambios cerebrales estructurales. El cortisol, hormona relacionada con el estrés, influye sobre el rendimiento cognitivo. Newcomer et al. (42) hallaron que el cortisol estaba aumentado en la saliva de voluntarios sanos que habían tenido peores resultados en una prueba cognitiva de estrés. Además, participantes emparejados tratados con cortisol tuvieron peor desempeño en evaluaciones cognitivas que los tratados con placebo (43). Otros estudios mostraron que la exposición prolongada a niveles altos de cortisol puede causar atrofia de regiones cerebrales específicas debido a la disminución de la neurogénesis (44).
Se halló que los pacientes con IC tenían valores plasmáticos altos de cortisol en relación con controles normales (45) y se hallaron valores significativamente mayores de cortisol en pacientes con IC que estaban deprimidos y tenían DC, pero no en los que no tenían estos síntomas (46), lo que sugiere que los valores de cortisol en la IC podrían influir sobre el desarrollo de DC.
Las catecolaminas están aumentadas en pacientes con IC, con efectos perjudiciales sobre la función cardíaca (47). Karlamangla et al. (48) informaron que en hombres ancianos, los valores altos de epinefrina urinaria se relacionaron con peor desempeño en las pruebas cognitivas. No obstante, la epinefrina no atraviesa la barrera hematoencefálica y se cree que su efecto sobre la función cerebral es a partir principalmente de una relación en U invertida entre la glucemia y la memoria (49).
♦ El eje inflamatorio
La IC se considera un estado de aumento de la inflamación y de la respuesta inmunitaria desencadenado habitualmente por una lesión miocárdica (50). En dos estudios (51, 52), se hallaron valores altos de interleucina (IL)-6 y factor-alfa de necrosis tumoral en pacientes con IC, DC y depresión, pero no en pacientes con IC sin DC ni depresión. Se puede obtener de estudios aleatorizados, doble ciego evidencia que sugiere un mecanismo de causa-efecto.
Estos estudios muestran alteración del funcionamiento cognitivo en personas sanas expuestas a endotoxinas bacterianas versus placebo (53). Estos estudios mostraron una relación inversa entre los valores de IL-6 y el funcionamiento cognitivo (53). Además, en otras enfermedades inflamatorias crónicas, como la artritis reumatoide, los valores más altos de citocinas circulantes se relacionaron con funciones cognitivas significativamente peores (54).
Almeida et al.(23) publicaron que, en relación con controles normales, se hallaron valores altos de IL-6, homocisteína plasmática total (tHcy) y cambios cerebrales más extensos en pacientes con IC, pero no en pacientes con cardiopatía isquémica. Los valores altos de tHcy produjeron atrofia cerebral y disminución cognitiva por apoptosis de las células cerebrales (55) y las intervenciones para disminuir la tHcy retrasaron la aparición de atrofia cerebral (56).
♦ Carencia alimenticia
Un estudio (58) indicó que aproximadamente un tercio de los pacientes con IC hospitalizados padecen insuficiencia de tiamina. Autopsias de cerebros de pacientes con insuficiencia de tiamina demostraron cambios histológicos en zonas relacionadas funcionalmente con la memoria (los cuerpos mamilares y el hipocampo) (60). Resonancias magnéticas efectuadas en pacientes con insuficiencia de tiamina también mostraron atrofia cerebral (61).
Si bien la mayoría de estos estudios se efectuaron en pacientes alcohólicos, no todos los alcohólicos tienen estas alteraciones (62) y se demostraron cambios comparables en modelos en animales con insuficiencia de tiamina sin exposición al alcohol. Si consideramos los datos que indican que la insuficiencia de tiamina se sospechó en solo el 20% de los pacientes con cambios cerebrales comprobados histológicamente de síndrome de Wernicke-Korssakof (60), se podría conjeturar que la insuficiencia de tiamina está también subdiagnosticada en la población con IC.
♦ Depresión
La interacción entre la IC, la DC y la depresión es compleja. La depresión se asocia con disminución de la función cognitiva (63) y cambios anatómicos en el cerebro (64), y también se mostró que se relaciona con mayores valores de biomarcadores inflamatorios (65) y neurohormonales (66). Sin embargo, la depresión también es frecuente entre pacientes con IC (30). Estos datos se pueden interpretar de dos maneras. Primero, porque la depresión se sugirió como posible causa de aumento del riesgo de IC, podría ser un importante factor de confusión en la asociación sugerida entre IC y DC. Por otro lado, la depresión también podría servir como un importante vínculo mecanístico entre la IC y la DC.
Se observó mejoría de las funciones cognitivas en pacientes tratados por su depresión (67). No obstante, no hay datos específicos para la población con IC.
♦ Otras vías
Los receptores sigma participan en diferentes funciones corporales, entre ellas cardíacas y cerebrales y recientemente se halló que participan en el vínculo sugerido entre IC y depresión. Es bien conocida la importancia del receptor sigma-1 (S1R) en la depresión (68). Esto se demostró (70) en modelos de laboratorio de IC.
► DEFINICIÓN DEL SÍNDROME CARDIOCEREBRAL
El término de síndrome cardiocerebral se empleó sin mucha rigidez por los investigadores (71–73) y esta falta de terminología unificadora impidió su aceptación universal.
| Los autores sugieren redefinir el término como un estado de deterioro cognitivo de causa indefinida en pacientes con IC, más allá de lo anticipado en controles emparejados y que se acompaña con cambios anatómicos cerebrales. |
El paciente puede exhibir gran variedad de síntomas neuroconductuales y podría ser necesario un examen específico para reconocer los cambios sutiles (74). La resonancia magnética muestra hiperintensidades de la sustancia blanca, especialmente la periventricular (32), y atrofia de la sustancia gris, sobre todo en el hipocampo y la corteza frontal (23,33). Los análisis mostrarán valores altos neurohormonales y de los marcadores inflamatorios. Se deben descartar otros posibles responsables que causen resultados similares antes de sugerir el síndrome cardiocerebral como generador del daño cerebral.
► OPCIONES TERAPÉUTICAS SUGERIDAS
La mejoría del funcionamiento cardíaco y de la hemodinamia sistémica tiene impacto positivo sobre el cerebro. La función cognitiva mejora tras el trasplante cardíaco y tras el implante de un DAVI (16,75). Al respecto, negar tratamiento avanzado de la IC a pacientes solo sobre la base del DC puede ser equivocado, dado su posible reversibilidad. No obstante, también fueron beneficiosas opciones terapéuticas menos invasivas. Un estudio (76) demostró que los pacientes con IC que recibían inhibidores de la enzima convertidora de angiotensina mejoraron su función cognitiva proporcionalmente a las dosis y la duración del tratamiento. Es probable que este efecto favorable no se limite al mejor funcionamiento cardíaco; la enzima convertidora de angiotensina actúa en las principales arterias cerebrales y por eso, a pesar de la reducción de la presión arterial, se observó aumento de la perfusión cerebral (77,78).
El efecto positivo de la digoxina sobre la función cognitiva (79) podría ser más complejo aún y es probable que no se limite solo al aumento de la contractilidad. Los efectos de otras medidas, como el implante de un marcapasos y el tratamiento de resincronización cardíaca probablemente se relacionan con la mejoría de la función cardíaca (82). Es importante, considerando la frecuencia de la IC en ancianos, que enfoques más directos, como programas de ejercicio (83) y para la memoria (84), también retrasan o revierten el deterioro cognitivo.
► ZONAS DE EQUILIBRIO Y PERSPECTIVAS A FUTURO
La mayoría de los datos presentados en este artículo provienen de estudios unicéntricos, bases de datos y estudios de observación. Por consiguiente, las conclusiones son en general opiniones de especialistas o consensos (Nivel de Evidencia: C). Al mismo tiempo, el peso de la evidencia que vincula la IC con el daño cerebral es indiscutible. El propósito de esta revisión fue presentar los datos acumulados hasta ahora a fin de aumentar la consciencia de los médicos sobre su existencia y motivar nuevas investigaciones que permitan conclusiones más firmes al evaluar esta enfermedad.
► ENFOQUE DEL SÍNDROME CARDIOCEREBRAL
La IC aguda se puede manifestar como disfunción cerebral significativa (3), si bien antes se deben descartar otros diagnósticos. Considerando la alta prevalencia de enfermedades concomitantes y el empleo frecuente de tratamiento antitrombótico en los pacientes con IC, los episodios de isquemia cerebral aguda y los episodios hemorrágicos se deben incluir siempre en el diagnóstico diferencial. También se deben considerar los desequilibrios metabólicos y electrolíticos, así como la susceptibilidad de estos pacientes a la infección y la sepsis.
Los efectos tóxicos del alcohol merecen consideración especial porque pueden producir tanto lesión cardíaca como cerebral. Por lo tanto se recomienda estabilizar la IC aguda, tratando de normalizar la presión arterial mientras se evita el posible daño a la perfusión y la función cerebral. Un estudio reciente mostró que la mortalidad a 30 días del alta y la tasa de rehospitalización sufrían una fuerte influencia de la presencia de DC (31). Por consiguiente, ignorar este problema solucionable podría impactar sobre la adherencia terapéutica de los pacientes, afectando desfavorablemente los resultados.
Debido a que numerosos datos indican que los pacientes con IC, ambulatorios, estables, pueden sufrir disfunción cerebral, el diagnóstico de daño cerebral podría ser más problemático en la IC crónica. Se sugiere efectuar una prueba cognitiva breve, sencilla (por ej.el Mini-Mental test [MMSE], el Montreal Cognitive Assessment [MoCA]) a todos los pacientes con IC durante la primera visita y a partir de allí anualmente, a fin de reconocer posibles cambios cognitivos sutiles que de lo contrario se podrían pasar por alto.
Si el resultado es patológico, se deben excluir los trastornos metabólicos y efectuar una resonancia magnética. Después es necesario derivar al paciente para su evaluación neurológica, que debe incluir la investigación y el tratamiento de una posible depresión. La evaluación se debe repetir tras la optimización del tratamiento de la IC. Se espera que este enfoque aumente las tasas diagnósticas de daño cerebral inducido por IC y podría asimismo mejorar las resultados terapéuticos.
► CONCLUSIONES
Datos significativos avalan la presencia y la importancia del daño cerebral en los pacientes con IC y también hay medidas para diagnosticar, sostener o revertir este daño. El primer paso es ser conscientes de la posibilidad de su existencia.
Resumen y comentario objetivo: Dr Ricardo Ferreira