Introducción
La colitis ulcerosa (CU) es una forma de enfermedad inflamatoria intestinal que en la actualidad afecta a más de 500.000 adultos y niños en los Estados Unidos [1]. Aunque una cantidad de terapias médicas está disponible para el manejo de la enfermedad, cerca del 20% de los pacientes afectados requerirá eventualmente una intervención quirúrgica secundaria al fracaso del tratamiento médico [2]. El advenimiento del procedimiento de la anastomosis bolsa ileal-anal (ABIA), ha permitido que los pacientes que requieren una proctocolectomía total logren continencia intestinal postoperatoria. Mediante la construcción de una pequeña bolsa con el intestino delgado, que sirve como reservorio fecal, los pacientes pueden evitar los desafíos psicológicos y sociales asociados con una colostomía permanente [4-6].
El procedimiento de ABIA se completa usualmente en 2 etapas [3]. En la primera etapa, los pacientes son sometidos a una proctocolectomía total con ABIA y una ileostomía temporaria de derivación. En la segunda etapa se revierte la ileostomía y se restaura la continuidad intestinal. Las etapas pueden modificarse omitiendo la derivación en la primera cirugía (esto es, procedimiento en 1 etapa) o realizando una colectomía subtotal en un procedimiento separado, previo a crear la ABIA con ileostomía (esto es, procedimiento en 3 etapas). La última técnica se reserva generalmente para los pacientes con enfermedad activa severa, aquellos con terapia esteroide desde hace mucho tiempo o con altas dosis o en los casos en que el diagnóstico es poco claro (por ej., CU versus enfermedad de Crohn) [7]. Se considera que, usando el procedimiento en 3 etapas en los pacientes agudamente enfermos, se mejorarán los resultados globales, porque el estado de salud del paciente y la inmunosupresión tendrán tiempo de recuperarse antes de realizar la ABIA, que puede ser susceptible de filtrar [8,9]. Los factores del paciente, preferencia del cirujano y entrenamiento, pueden jugar también un rol en la determinación de las etapas de los pacientes con CU para los procedimientos de ABIA y las tasas de los procedimientos en 3 etapas para pacientes con enfermedad grave varían tremendamente entre las instituciones y los cirujanos [10].
La presunción frecuentemente expresada es que los pacientes tratados con procedimientos en 3 etapas, son sometidos a un procedimiento quirúrgico seguro y se evitan las complicaciones asociadas con el procedimiento en 2 etapas. Sin embargo, hay pocos datos referidos a la validez de esa presunción. En sí, el abordaje óptimo en etapas, para los pacientes tradicionalmente considerados con alto riesgo de filtración anastomótica, permanece incierto [10].
El objetivo de este estudio fue, en consecuencia, determinar si el abordaje en 3 etapas está justificado en pacientes percibidos como de alto riesgo para complicaciones postoperatorias. Para responder esa cuestión, los autores compararon primero las características de los pacientes con CU activa (CUA; por ejemplo, fracaso del tratamiento médico) sometidos a procedimientos de ABIA en 2 y 3 etapas, en la institución en donde se desempeñan. Segundo, evaluaron si los pacientes con una CUA tratados con procedimientos en 3 vs 2 etapas tuvieron verdaderamente mejores resultados perioperatorios y a largo plazo.
Métodos
Diseño del estudio
Se obtuvo la aprobación para efectuar esta investigación por parte de la junta de revisión institucional del hospital antes de su iniciación. Los registros médicos de todos los pacientes sometidos a ABIA en 2 y 3 etapas por CUA, entre el 1 de septiembre de 2000 y el 30 de marzo de 2011, en la institución, fueron revisados para su inclusión en el estudio. Los pacientes potenciales fueron identificados usando una combinación de revisión de las bases de datos personales de los cirujanos y una consulta administrativa usando los códigos de la Current Procedural Terminology. Los pacientes que habían tenido un procedimiento de ABIA por displasia, recibiendo una anastomosis ileo-rectal y que fueron diagnosticados como afectados por una enfermedad de Crohn o una colitis indeterminada en el informe anatomopatológico postoperatorio, o aquellos sometidos a un procedimiento en 1 etapa, fueron excluidos del informe.
Variables de interés
En los pacientes que cumplían con los criterios de inclusión, se consultaron los registros médicos para obtener lo siguiente: (1) características demográficas (edad; sexo; raza; índice de masa corporal [IMC]; edad ajustada por el Charlson Comorbidity Index [CCI] [11]; puntaje de la American Society of Anesthesiologists [ASA]; número de operaciones abdominales previas; consumo de tabaco; uso de esteroides; agentes anti factor de necrosis tumoral [FNT] u otros inmunomoduladores [metotrexato, 6-mercaptopurina, azatioprina, ciclosporina] en la primera operación y movimientos intestinales diarios reportados antes de la operación); (2) detalles del procedimiento quirúrgico (estado de emergencia; etapas [3 etapas vs 2 etapas]; procedimiento laparoscópico; puntaje Apgar quirúrgico [12] y experiencia del cirujano, esto es, cirujano con alto volumen de casos de enfermedad inflamatoria intestinal [EII], definido como un cirujano que ha efectuado ≥ 50 procedimientos de ABIA; (3) hallazgos anatomopatológicos (por ej., inflamación severa en el espécimen determinada por un patólogo certificado); (4) resultados perioperatorios (sepsis abdominal [filtración, absceso]; otras infecciones [neumonía, infección del tracto urinario, infección de la herida]; complicaciones trombóticas [embolia pulmonar, trombosis venosa profunda, trombos asociados a la línea de sutura]; e íleo y obstrucción del intestino delgado, definido como > 3 días entre la cirugía y la inhabilidad del paciente para tolerar una dieta sólida, sin náuseas, vómitos o distensión abdominal y/o evidencia de obstrucción en los estudios radiográficos [13]); (5) duración de la estadía hospitalaria; (6) readmisiones hospitalarias dentro de los 30 días de la cirugía; (7) complicaciones a largo plazo (pouchitis, definida como síntomas de inflamación del reservorio confirmados por endoscopía y/o biopsia [14,15]; fistula o absceso; íleo u obstrucción del intestino delgado [quirúrgica y no quirúrgica]; eventración; estenosis anal; y fracaso de la bolsa) y (8) duración total del seguimiento. El estado de emergencia fue definido como cualquier caso que fue programado para la sala de operaciones, dentro de las 4 horas después de que el cirujano determinara que el paciente necesitaba cirugía, lo que fue marcado en los registros hospitalarios con el puntaje ASA seguido con una “E” (por ejemplo, ASA 2E).
Análisis estadístico
Las características demográficas y otras basales fueron resumidas como medias (error estándar de la media [EEM]) o cuenta con porcentaje, según lo apropiado. Para identificar los predictores que alentaron a los cirujanos para efectuar un abordaje en 3 etapas en sus pacientes, los grupos de 3 etapas vs 2 etapas fueron comparados usando la prueba x2 de Pearson o la exacta de Fisher (variables categóricas), la prueba t de 2 muestras (variables continuas) y un modelo de regresión multivariado. Luego se compararon las complicaciones de los pacientes tratados con procedimientos en 3 etapas vs 2 etapas, utilizando análisis de regresión multivariados que incluyeron a cualquier variable significativa identificada en el análisis univariado, así como las siguientes o variables a priori: presencia de enfermedad colónica severa en la patología de la primera operación, edad ajustada por el CCI, puntaje de Apgar quirúrgico, uso de esteroides en la primera operación, uso de agentes anti FNT en la primera operación, uso de otros inmunomoduladores en la primera operación, estado de emergencia y experiencia del cirujano. Las variables a priori fueron seleccionadas basado en una revisión de la literatura y discusión de los autores (2 de los cuales son cirujanos colorrectales). La duración del seguimiento fue incluida únicamente en el modelo para el análisis de las complicaciones a largo plazo. La incidencia de las complicaciones y otros datos sobre resultados, fueron reportados como media de los mínimos cuadrados (error estándar de la media), basado en estimaciones del modelo de regresión. Todas las pruebas fueron de 2 colas y realizadas con un nivel de significación de 0,05. Los análisis estadísticos fueron realizados usando el programa estadístico JMP, versión 9.0 (SAS Institute, Inc).
Resultados
Características demográficas de los pacientes
Un total de 144 pacientes (77 [53,3%] masculinos; 67 [46,5%] femeninos) con una edad media (EEM) de 34,6 (1,0) años (rango, 11-67 años) fue sometido a procedimientos en 2 y 3 etapas por CUA, debido a fracaso del manejo médico, en un período de 10,5 años (01/09/2000 a 30/03/2011). De esos pacientes, 116 (80,6%) tuvieron un procedimiento en 2 etapas y 28 (19,4%) en 3 etapas. Diez cirujanos diferentes realizaron los procedimientos, 6 de los cuales eran cirujanos con alto volumen de casos de EII. La duración media del seguimiento (EEM) para todos los pacientes fue de 5,15 (0,24) años (rango, 0,26-11,9 años).
Factores asociados con los procedimientos en 3 etapas vs 2 etapas
Los procedimientos en 3 etapas, comparados con los procedimientos en 2 etapas, se asociaron con una frecuencia más alta de estado de emergencia (32,1% vs 2,6%, respectivamente; P < 0,001) y con una mayor inestabilidad hemodinámica intraoperatoria (media [EEM] del puntaje de Apgar quirúrgico, 5,89 (0,27] vs 6,47 (0,12), respectivamente; P = 0,04). No hubo diferencias significativas en la edad, sexo, raza, IMC, edad ajustada por CCI, tabaquismo, número de operaciones abdominales previas o número reportado preoperatoriamente de movimientos intestinales diarios, entre los grupos (P para todos > 0,05) (Tabla 1). Tampoco hubo diferencias significativas en la proporción de pacientes sometidos a procedimientos en 3 etapas vs 2 etapas que estaban usando esteroides (P = 0,48) o agentes anti-FNT (P = 0,22) en la primera operación (Tabla 1), aunque más pacientes sometidos a procedimiento en 2 etapas estaban usando otros inmunomoduladores (por ej., metotrexato, 6-mercaptopurina, azatioprina y ciclosporina), que los pacientes sometidos a procedimientos en 3 etapas (48,3% vs 17,9%, respectivamente; P = 0,004). No hubo diferencias significativas en el uso de laparoscopía (P = 0,23), o experiencia del cirujano (P = 0,84) entre los 2 grupos, o en la frecuencia de colitis severa juzgada por el patólogo (P = 0,45) (Tabla 1).
• TABLA 1: Características demográficas de los pacientes para los grupos de ABIA en 3 etapas vs 2 etapas
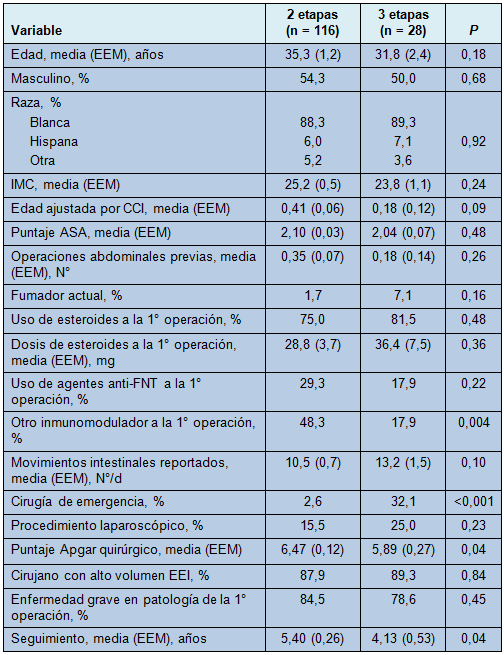
En el modelo de regresión multivariado comparando los factores asociados con los procedimientos en 3 etapas vs 2 etapas, los puntajes CCI más altos (odds ratio [OR] = 3,91; 95% intervalo de confianza [IC]: 1,19-21,72; P = 0,02) y el estado de cirugía de emergencia (OR = 27,20; 95% IC: 5,21-207,52; P < 0,001) se asociaron significativamente con los procedimientos en 3 etapas. Similar a los hallazgos con el análisis univariado, el uso de inmunomoduladores se asoció con probabilidades más bajas de realización de un procedimiento en 3 etapas vs 2 etapas (OR = 0,22; 95% IC: 0,06-0,71). La presencia de enfermedad severa en la primera operación, uso de esteroides, uso de agentes anti-FNT, experiencia del cirujano y puntaje Apgar quirúrgico, no estuvieron asociados significativamente con las etapas operatorias en el modelo (P para todos ≥ 0,11).
Resultados acumulativos con procedimientos en 3 etapas vs 2 etapas
Los pacientes con procedimientos en 3 etapas vs 2 etapas tuvieron estadías hospitalarias más cortas por sus colectomías subtotales vs cirugía de ABIA (media [EEM] 4,3 [0,8] vs 6,6 [0,4] días, respectivamente; P = 0,01), pero duraciones de estadía total similares, cuando todos los procedimientos (proctectomía y cierre de ileostomía subsiguientes) fueron combinados (media [EEM] 11,9 [1,3] vs 10,6 [0,6] días, respectivamente; P = 0,38). El número total de readmisiones dentro de los 30 días de la cirugía fue similar entre los grupos de 3 etapas vs 2 etapas (media [EEM] 0,71 [0,15] vs 0,52 [0,07] readmisiones, respectivamente; P = 0,23), aunque el número de readmisiones por procedimiento fue más bajo en el grupo de 3 etapas que en el de 2 etapas (media [EEM] 0,18 [0,09] vs 0,40 [0,05] readmisiones, respectivamente; P = 0,04).
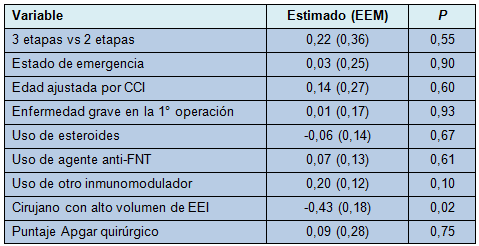
En el análisis univariado, los procedimientos en 2 etapas se asociaron con más complicaciones postoperatorias después del primer procedimiento (incluyendo sepsis abdominal, otras infecciones [neumonía, infección del tracto urinario, infección de la herida, infección de la línea de sutura], complicaciones trombóticas e íleo u obstrucción del intestino delgado, que los procedimientos en 3 etapas (media [EEM] 0,89 [0,09] vs 0,50 [0,18] complicaciones, respectivamente; P = 0,05), pero con un número global similar de complicaciones perioperatorias (media [EEM] 1,18 [0,13] vs 1,29 [0,26] complicaciones, respectivamente; P = 0,71) (Tabla 2). La regresión multivariada controlando las variables a priori (ver Análisis estadístico) sugirió que las complicaciones perioperatorias globales fueron afectadas por la experiencia del cirujano (media [EEM 1,16 [0,31] complicaciones con los cirujanos con alto volumen vs 2,01 [0,46] complicaciones con los cirujanos con bajo volumen de casos; P = 0,02), más que la creación de la ABIA en la primera operación (media [EEM] 1,58 [0,35] complicaciones para los procedimientos en 2 etapas versus 1,80 [0,40] para los procedimientos en 3 etapas; P = 0,55) u otras variables (Tabla 3). Importantemente, los procedimientos en 2 etapas no cambiaron el riesgo de filtración anastomótica cuando todas las operaciones fueron tomadas en cuenta (OR = 1,09; 95% IC: 0,05-8,07; P = 0,94) No hubo muertes perioperatorias en ninguno de los grupos.
• TABLA 2: Análisis univariado comparando resultados perioperatorios y a largo plazo después de procedimientos de ABIA en 3 etapas vs 2 etapas (Ver cuadro)
• TABLA 3: Análisis multivariado de regresión de los factores afectando el total de complicaciones perioperatorias después de procedimientos de ABIA en 3 etapas vs 2 etapas
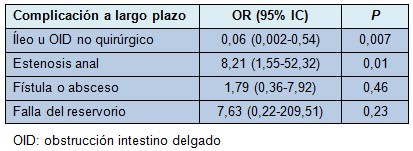
En el seguimiento a largo plazo (media [EEM] 5,2 [0,2] años), la regresión logística sugirió que los pacientes sometidos a procedimientos en 2 etapas podían tener un riesgo más bajo de estenosis anal (P = 0,01), pero un riesgo más alto de íleo u obstrucción del intestino delgado (P = 0,07), comparado con los pacientes sometidos a procedimientos en 3 etapas (Tabla 4). No hubo diferencias significativas en la formación de fístulas o abscesos (P = 0,46) o en la falla del reservorio (P = 0,23) entre los grupos (Tabla 4).
• TABLA 4: Probabilidades de complicaciones a largo plazo para los procedimientos de ABIA en 3 etapas vs 2 etapas
Factores que afectan los resultados después del procedimiento en 2 etapas
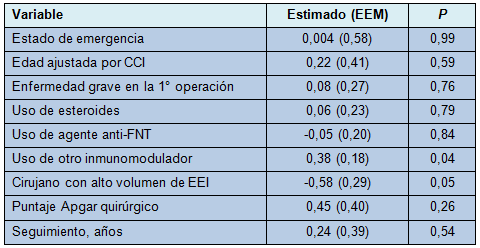
Para los pacientes sometidos a procedimientos en 2 etapas, la regresión multivariada sugirió que el número total de complicaciones postoperatorias era afectado por la experiencia del cirujano (media [EEM] 2,25 [0,59] complicaciones en los cirujanos con alto volumen vs 3,41 [0,85] complicaciones en los cirujanos con bajo volumen; P = 0,05) y el uso de otros inmunomoduladores distintos a los esteroides y a los agentes anti-FNT en la primera operación (media [EEM] 3,21 [0,72] complicaciones con el uso vs 2,45 [0,68] sin el uso; P = 0,04). El estado de emergencia, uso de esteroides y uso de agentes anti-FNT no afectaron significativamente los resultados en 2 etapas (P para todos > 0,05) (Tabla 5).
• TABLA 5: Análisis de regresión multivariada de los factores que afectan globalmente los resultados del procedimiento de ABIA en 2 etapas.
Discusión
La decisión de realizar un procedimiento en 3 etapas vs 2 etapas para un paciente con CU severa es realizada frecuentemente por el “instinto intestinal” del cirujano y una enseñanza quirúrgica individual con respecto al dogma, preconceptos sobre el riesgo y experiencias previas con pacientes obtenidas del entrenamiento previo y de complicaciones previas [10]. La razón para este abordaje no científico, es que no hay un estándar y que son limitados los datos disponibles para indicar los factores que permitirían una óptima opción de etapas para la ABIA, entre los pacientes con CUA en medio de un brote agudo de la enfermedad. Dos fueron los objetivos de este estudio: (1) determinar los predictores de un paciente con CUA (por ej., fracaso del tratamiento médico) que recibe un procedimiento de ABIA en 3 etapas y (2) determinar si el procedimiento en 3 etapas vs 2 etapas mejora los resultados perioperatorios y a largo plazo, después de tomar en cuenta esos predictores. Los resultados presentados aquí sugieren que, en la institución en donde se desempeñan los autores, la mayoría de los pacientes que presentaron una CU severa, fueron tratados con un abordaje en 2 etapas. El uso de esteroides o de agentes anti-FNT y la presencia de comorbilidades médicas, no impidieron que los cirujanos construyeran una ABIA en el procedimiento primario y los resultados postoperatorios no fueron adversamente afectados por abordaje. El 19,4% de los pacientes que fueron tratados con un procedimiento en 3 etapas, fueron aquellos sometidos a cirugía de emergencia y los que tenían un puntaje CCI muy alto.
La alta prevalencia del abordaje en 2 etapas que se reporta es diferente de los abordajes más conservadores usados en otras instituciones, donde es empleado generalmente el procedimiento en 3 etapas para la ABIA en los pacientes con CU que reciben esteroides en dosis altas o desde hace mucho tiempo, aquellos con enfermedad colónica severa o los sometidos a cirugía de emergencia [7,10]. No obstante, esa práctica de llevar a los pacientes agudamente enfermos hacia un abordaje en 3 etapas, se basa en gran proporción en un número limitado de estudios que demostraron que el uso de esteroides y la proctitis severa pueden incrementar el riesgo de sepsis pélvica después de la ABIA [8,9], combinado con observaciones de que la sepsis pélvica fue menos frecuente después de los procedimientos en 3 etapas [16,17]. Además, esos últimos estudios están basados en análisis univariados de datos recolectados más de 20 años después.
Interesantemente, en el presente estudio, los autores hallaron que los pacientes que recibían tratamiento con inmunomoduladores no estándar (por ej., metotrexato, 6-mercaptopurina, azatioprina y ciclosporina), tuvieron en realidad probabilidades más bajas de ser sometidos a procedimientos en 3 etapas. Una explicación posible para ese hallazgo, es que esos agentes de segunda línea fueron más aptos para ser empleados previos a la cirugía entre los pacientes con fracaso del tratamiento previo, pero sin complicaciones de emergencia de su enfermedad. También es posible que la propensión a realizar un procedimiento en 2 etapas con otros inmunomoduladores, sea un reflejo de la actual falta de datos sobre si esos agentes aumentan el riesgo de sepsis pélvica. Para señalar, el uso del metotrexato, 6-mercaptopurina, azatioprina y ciclosporina, se asoció también con probabilidades más altas de complicaciones perioperatorias en este estudio. Si eso fue el reflejo de una estadificación agresiva de los pacientes que recibían ese tratamiento, o un efecto de los agentes sobre la friabilidad de la propia anastomosis, queda por determinarse. El impacto de los agentes inmunomoduladores de segunda línea sobre los resultados postoperatorios y, específicamente, sobre la tasa de filtración anastomótica, puede merecer un examen más focalizado en el futuro.
Datos más recientes que representan a las potenciales variables de confusión, sugieren que no hay diferencia en la frecuencia de sepsis pélvica con los procedimientos de ABIA en 2 etapas vs 3 etapas, así como tampoco hay diferencia global en los resultados postoperatorios [8,9,17-20]. Concordante con esa noción, los autores del presente trabajo hallaron que sus pacientes sometidos a procedimientos en 2 etapas evolucionaron tan bien en el corto y largo plazo, como los pacientes que fueron tratados inicialmente con una colectomia subtotal. Asimismo, hallaron que los resultados después de un procedimiento en 2 etapas fueron afectados principalmente por la experiencia del cirujano y el uso de otros inmunomoduladores (metotrexato, 6-mercaptopurina, azatioprina y ciclosporina), más que por el estado de emergencia o los predictores ampliamente asumidos para las complicaciones, tales como el uso de esteroides, agentes anti-FNT y enfermedad grave [8,9,21-24]. Los pacientes que recibieron procedimientos en 2 etapas parecieron tener también un riesgo más bajo de estenosis anal y ninguna diferencia en el riesgo de formación de fístulas o abscesos o en la falla del reservorio a largo plazo, comparado con los pacientes sometidos al procedimiento “más seguro” en 3 etapas.
Finalmente, el más interesante y estimulante hallazgo de los autores de este trabajo es que, además del uso de otros inmunomoduladores, la experiencia del cirujano jugó un rol significativo en la determinación de los resultados en los pacientes después de la cirugía de ABIA. El procedimiento realizado por un cirujano con alto volumen de casos de EII, disminuyó significativamente la incidencia de complicaciones postoperatorias, tanto en el análisis de los pacientes sometidos a procedimientos en 3 etapas vs 2 etapas, como con los pacientes sometidos sólo a procedimientos en 2 etapas. Ese hallazgo es consistente con datos previos, demostrando que la incidencia de sepsis pélvica postoperatoria disminuye significativamente con el aumento de la experiencia quirúrgica [25]. La tasa de falla del reservorio parece ser también más alta durante la fase inicial de la curva de aprendizaje de la práctica quirúrgica [26]. La asociación entre las complicaciones postoperatorias y la falta de experiencia del cirujano, sugiere que los cirujanos sin un entrenamiento formal colorrectal y con mínima experiencia con la EII, deberían considerar un abordaje tardío a la ABIA, en un esfuerzo para mitigar la morbilidad potencial de un abordaje más agresivo en 2 etapas.
La decisión sobre si realizar una ABIA en 2 etapas vs 3 etapas no tiene sólo importantes implicaciones para los resultados postoperatorios, sino que afecta también los costos globales del tratamiento [10,20,27,28]. Los pacientes con procedimientos en 2 etapas tuvieron similares duraciones totales de la estadía hospitalaria y readmisiones dentro de los 30 días en este estudio, pero eso no significa que los costos globales de tratamiento fueran equivalentes. Swenson y col. [20] reportaron un ahorro de costo total de $ 10.000 (dólares estadounidenses) para el procedimiento de ABIA en 2 etapas, comparado con el procedimiento en 3 etapas, a pesar del hecho de que la duración global de la estadía no fue significativamente diferente entre los 2 grupos. Dados los costos de la sala de operaciones, equipamiento, agentes anestésicos y personal, que se asocian con cada procedimiento quirúrgico, ese hallazgo no es sorprendente. Esta es una consideración importante en esta era de reforma de la salud pública, en donde el futuro del reembolso de costos es incierto y las instituciones médicas, a lo largo de los EEUU, están intentando maximizar la eficiencia de la atención.
Las limitaciones de este estudio merecen alguna discusión. Es un análisis retrospectivo realizado sobre datos de ABIA de una única institución, elevando el potencial de desvíos o de resultados no generalizables. Hay probablemente un número de factores que contribuye a la decisión de realizar un procedimiento en 2 etapas vs 3 etapas, por lo que es posible que el estudio no tenga el suficiente poder estadístico para detectar diferencias entre los grupos. Diez cirujanos diferentes fueron incluidos en el estudio, haciendo difícil el control del uso de distintas técnicas operatorias (por ej., técnica de eversión rectal; anastomosis manuales vs mecánicas, longitud del manguito, etc.). No obstante, uno de los problemas actuales con la optimización del manejo quirúrgico de la CU, es que la mayoría de los estudios están basados en instituciones con significativa experiencia en cirugía colorrectal y/o están basados en la experiencia de un único cirujano. Por lo tanto, las conclusiones de esos estudios son difíciles de aplicar al campo general. Incluyendo datos de varios cirujanos con un rango de experiencia, los resultados del presente trabajo son aplicables potencialmente a una audiencia más amplia. Finalmente, los mayores detalles sobre la dosificación precisa y la duración del tratamiento inmunomodulatorio, pueden haber sido esclarecedores en la evaluación de los verdaderos efectos de esa terapia sobre la cicatrización anastomótica y deberían ser el tema de futuras investigaciones.
En conclusión, los pacientes con una CUA sometidos a la creación inmediata de una ABIA (esto es, un procedimiento de 2 etapas) parecen tener resultados similares a los de los pacientes tratados inicialmente con colectomia subtotal. Los datos del presente estudio sugieren que el uso de esteroides y de agentes anti-FNT, por sí solo, no justifica la decisión de evitar la creación de una ABIA en la primera operación, mientras que el procedimiento sea realizado por un cirujano con alto volumen de casos de EII.
♦ Comentario y resumen objetivo: Dr. Rodolfo D. Altrudi