|
Resumen
|
| Introducción |
La insuficiencia cardíaca (IC) se acompaña de riesgo considerable de morbimortalidad y deteriora la calidad de vida y la capacidad funcional.
Se puede dividir en IC con fracción de eyección (FE) reducida (ICFEr = ≤ 40%) e IC con FE conservada (ICFEc) En personas sanas la FE, que expresa el porcentaje de sangre bombeada desde el ventrículo izquierdo en cada contracción oscila en el 52% - 72% en los hombres y en el 54% - 74% en las mujeres.
Un valor del 40% es suficiente para la clasificación de ICFEr. En los E.E.U.U. alrededor del 50% de los casos de IC son ICFEr. La fisiopatología de la ICFEr es compleja y suele comenzar con un episodio desencadenante, tal como lesión directa al miocardio o enfermedad del mismo (por ejemplo, enfermedad coronaria, infarto del miocardio y miocardiopatía dilatada), que conduce a disminución de la contracción ventricular. Inicialmente se activan varios mecanismos compensatorios que a la larga fallan.
La identificación de los factores desencadenantes permite clasificar a los pacientes en aquellos con riesgo de sufrir ICFEr y aquellos con enfermedad sintomática. Esta clasificación posibilita establecer tratamientos preventivos para los pacientes de alto riesgo y retardar la evolución de la enfermedad. El mayor éxito terapéutico se observa en pacientes con ICFEr, mientras que las opciones son escasas para los casos con ICFEc.
| Epidemiología |
El riesgo de sufrir IC aumenta con la edad, siendo del 20% entre la población mayor de 40 años
> Incidencia y prevalencia
En los E:E.U:U. la prevalencia de IC aumentó de 5,7 millones de personas ≥20 años (de 2009 a 2012) a 6,5 millones (de 2011 a 2014). En Europa, la prevalencia de IC en 2008 fue de alrededor de 15 millones de personas, con prevalencia global del 2% - 3%, aumentando la misma al 10–20% entre los pacientes de 70–80 años.
El número de personas con riesgo de desarrollar IC (personas con obesidad, diabetes mellitus e hipertensión) aumentó debido al aumento de la esperanza de vida. El riesgo de sufrir IC aumenta con la edad, siendo del 20% entre la población mayor de 40 años.
> Hospitalización
Alrededor del 25% de los pacientes hospitalizados por IC son rehospitalizados dentro de los 30 días, con tasas de rehospitalización de alrededor del 50% a los 6 meses. Además el 25–30% de los pacientes fallece dentro del año del alta. Estas cifras aumentan en los países subdesarrollados.
> Factores de riesgo
En estudios epidemiológicos se observaron diferencias fisiopatológicas entre los pacientes with ICFEr y los pacientes con ICFEc.
Algunos factores de riesgo cardiovascular como diabetes mellitus, tabaquismo e hipertensión preceden a ambas clases de IC, pero las personas que sufren ICFEc tienden a ser mayores, de sexo femenino, con antecedentes de hipertensión y con más probabilidades de padecer fibrilación auricular.
El sexo masculino, la hipertrofia ventricular izquierda, el bloqueo de rama, el infarto de miocardio previo y el tabaquismo se relacionan más fuertemente con ICFEr.
Otros factores de riesgo de IC son la aterosclerosis, la obesidad y el síndrome metabólico.
| Mecanismos/fisiopatología |
> Etiología y factores desencadenantes
La ICFEr es causada predominantemente por enfermedad coronaria y el factor de riesgo más importante es la hipertensión. Otras etiologías son: miocardiopatías, infarto del miocardio, miocarditis, valvulopatías e infecciones cardíacas. Las causas extracardíacas de ICFEr son disfunción tiroidea, enfermedades sistémicas (sarcoidosis, lupus), las relacionadas con alcoholismo y drogas y la quimioterapia contra el cáncer.
En pacientes con ICFEr que se encuentran estables, los factores que pueden precipitar un agravamiento son:
|
> Factores médicos
> Factores psicosociales
|
> Fisiopatología
La relación entre la lesión inicial y el desarrollo y la progresión de la ICFEr es sumamente compleja. A nivel genético y molecular, puede haber cambios en la estructura celular (depleción del sarcómero y depósito de glucógeno).
Se producen alteraciones de las proteínas contráctiles, reguladoras y del citoesqueleto que llevan a la disfunción de la miofibrilla (incluyendo desfosforilación y alteración en la localización, expresión y actividad de las proteínas).
En la célula se prolongan los potenciales de acción debido a alteraciones en los canales de membrana de sodio y potasio con la producción de arritmias. Las alteraciones del metabolismo energético del miocardio incluyen mayor dependencia del metabolismo de la glucosa, disminución de la fosforilación oxidativa y alteraciones de la función mitocondrial.
Un aspecto de gran interés es la mejoría del metabolismo miocárdico en el corazón “atontado” o hibernado con el objeto de alterar el remodelado celular patológico.
En el desarrollo de la IC también pueden participar otros cambios como la alteración de las respuestas al estrés, la apoptosis y la autofagia. A pesar de que todas estas alteraciones se identificaron, su tiempo de aparición desde la lesión inicial hasta la progresión de la enfermedad es poco conocido.
También se desconoce por qué algunos pacientes recuperan completamente la función ventricular y otros empeoran. Lo que está claro es que el remodelado cardíaco, generado por estas alteraciones de la función celular, conduce a la ICFEr (Figura 1).
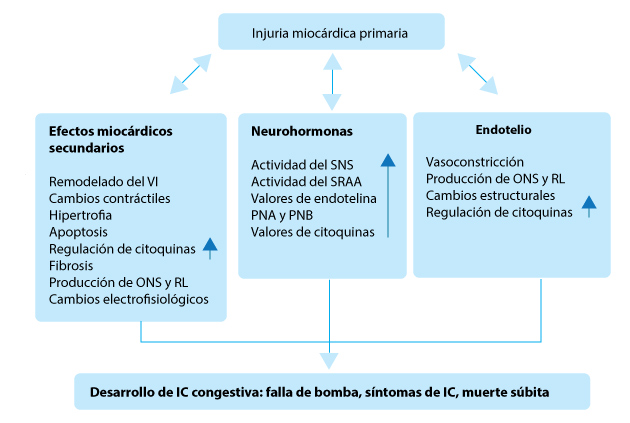
Figura 1. Fisiopatología de la IC. La lesión cardíaca inicial produce una cascada de efectos deletéreos sobre el miocardio y sobre el sistema neurohormonal y endotelial que conducen a la falla de bomba, síntomas de IC y muerte súbita. El mecanismo se inicia con aumento de la regulación del sistema nervioso simpático (SNS) y del sistema renina-angiotensina-aldosterona (SRAA) que son beneficiosos en el corto plazo. La evolución crónica de este mecanismo produce remodelado del ventrículo izquierdo, fibrosis del miocardio y apoptosis. ONS: óxido nítrico sintasa; RL: radicales libres; PNA: péptido natriurético A (PNA); PNB: péptido natriurético B.
En la ICFEr falla uno de los principales mecanismos adaptativos del corazón, la ley de Frank Starling que establece que al llenarse el ventrículo más de lo habitual, aumenta la fuerza contráctil de la sístole siguiente, produciendo mayor volumen sistólico y vaciamiento adecuado de la sobrecarga de volumen.
En la ICFEr los aumentos del volumen de fin de diástole aumentan la presión en la aurícula izquierda, congestionan las venas pulmonares y dan origen a la disnea y otros síntomas pulmonares de IC.
> Mecanismos compensadores.
La caída del volumen minuto debida a la insuficiencia ventricular desencadena varios mecanismos compensadores que son inicialmente adaptativos a fin de favorecer el aumento del gasto cardíaco y de mantener la perfusión de los tejidos. Estos mecanismos son la activación neurohormonal del sistema nervioso simpático (SNS) y del sistema renina-angiotensina-aldosterona (SRAA). (figura 2)
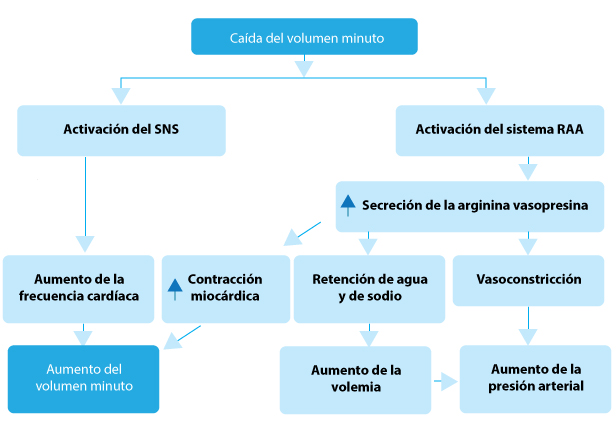
Figura 2. Mecanismos compensadores durante la primera etapa de la IC.
Aunque la activación neurohormonal es inicialmente beneficiosa para mantener el volumen minuto, la activación crónica de estos sistemas puede producir remodelado ventricular patológico y empeoramiento de la IC.
La actividad simpática prolongada disminuye los receptores β-adrenérgicos de los cardiomiocitos, lo que contribuye a la disminución de la sensibilidad miocárdica a las catecolaminas y una respuesta inotrópica reducida, que disminuye la contractilidad ventricular.
Además, la actividad crónica del SMS lleva a taquicardia y arritmia que pueden causar más deterioro clínico o incluso la muerte súbita cardíaca. La activación crónica del SRAA conduce al aumento de angiotensina II y aldosterona, que inician procesos patológicos, entre ellos hipertrofia de los miocitos y fibrosis intersticial, ambas patognomónicas del remodelado ventricular patológico.
Como compensación de la activación neurohormonal crónica nociva, aumentan factores reguladores opuestos, como los péptidos natriuréticos, la bradicinina y las prostaglandinas. Estos péptidos contrarrestan los efectos nocivos de la activación crónica del sistema SRAA y del simpático al promover la natriuresis, además de la vasodilatación y la diuresis. Pero a medida que la IC avanza, los efectos de los péptidos natriuréticos se atenúan.
> Remodelado cardíaco. El remodelado cardíaco se refiere a los cambios estructurales producidos en respuesta a las alteraciones hemodinámicas, la activación neurohormonal y la lesión miocárdica, que al inicio son adaptativos, pero pueden causar el desarrollo y la progresión de la ICFEr.
La hipertrofia miocárdica se desarrolla en pacientes con ICFEr en respuesta al aumento sostenido del estrés de la pared debido a dilatación ventricular o poscarga excesiva, para mantener la firmeza adecuada y el aumento de la presión ventricular de fin de diástole, lo que causa aumento de la presión auricular izquierda y de las presiones venosas pulmonares y disnea.
Otros factores que pueden producir remodelado ventricular patológico y manifestaciones clínicas de IC son la fibrosis miocárdica, la necrosis y la inflamación. La identificación y el tratamiento temprano de este proceso podrían proporcionar nuevos blancos terapéuticos para prevenir la progresión de la enfermedad.
| Diagnóstico, pesquisa y prevención |
El diagnóstico de IC puede ser difícil, especialmente en sus primeras fases. La ecografía transtorácica (ETT) se emplea para determinar la presencia de disfunción sistólica y/o diastólica, que puede confirmar el diagnóstico de ICFEr (cuando la fracción de eyección es ≤40%).
La ETT también es útil para determinar la función valvular, la presencia de hipertrofia ventricular izquierda y el grado de hipertensión pulmonar. Otras técnicas, como la evaluación de la anamnesis, el examen físico y el empleo de biomarcadores, estudios por imágenes y registros fisiológicos del corazón se pueden emplear para determinar la etiología de la IC y la presencia de congestión y/o hipoperfusión. El diagnóstico temprano y la iniciación inmediata del tratamiento son esenciales para una buena evolución.
> Anamnesis y examen físico
La anamnesis inicial debe incluir la identificación de los factores de riesgo y de los factores cardiovasculares y no cardiovasculares precipitantes de IC, además de las enfermedades concomitantes.
Los antecedentes familiares de muerte súbita cardíaca o IC pueden ayudar a identificar los casos genéticos o familiares. La anamnesis se puede emplear para identificar los síntomas de congestión. La evaluación de los medicamentos del paciente puede identificar los tratamientos que podrían empeorar la IC.
Asimismo, se pueden identificar factores que podrían afectar el pronóstico, como la caquexia cardíaca, shocks con el desfibrilador cardioversor implantable o si el paciente ha estado hospitalizado por IC. Además se pueden identificar síntomas isquémicos (por ej. precordialgia o presión torácica), arritmia (por ej. palpitaciones) y trastornos respiratorios del sueño, que pueden empeorar la IC. También se debe evaluar la alimentación del paciente.
| El examen físico debe comenzar con la evaluación cuidadosa de los signos vitales y posteriormente confirmar la presencia de congestión (por ej, edema y ascitis) y evaluar el volumen minuto (por ej la presión arterial). |
> Exámenes complementarios
La presencia de biomarcadores (péptidos natriuréticos) dentro de límites normales en un paciente no tratado descarta la IC
Además del examen físico se debe efectuar un electrocardiograma (ECG) Entre las pruebas de laboratorio se pueden incluir la evaluación de la función renal (urea, creatinina y estimación de la filtración glomerular) y la medición de los valores de potasio.
Los biomarcadores cardíacos cambiaron el panorama del diagnóstico y el pronóstico de los pacientes con IC. Los más utilizados son los péptidos natriuréticos, como el péptido natriurético cerebral (BNP), y el N-terminal-pro BNP.
La presencia de ellos dentro de límites normales en un paciente no tratado descarta la IC. Para pacientes en riego de sufrir IC, pesquisar los valores de los péptidos natriuréticos podría ayudar a orientar el inicio precoz del tratamiento y prevenir así el comienzo de disfunción ventricular izquierda o una nueva IC.
La función de la biopsia endomiocárdica es limitada, pero se la recomienda en situaciones en las que la etiología de la ICFEr de nueva aparición o compleja no está clara o no responde al tratamiento habitual.
> Otras pruebas
La ETT puede proporcionar información para ayudar al diagnóstico y el tratamiento de los pacientes con ICFEr. Entre los datos de la ETT 2D en estos pacientes, además de la reducción de la fracción de eyección, se podrían incluir la dilatación o hipertrofia de las cámaras auriculares y ventriculares, la disfunción valvular, la patología pericárdica y las altas presiones de llenado ventricular.
El ecocardiograma transesofágico se puede emplear, cuando las imágenes de la ETT son insuficientes, para visualizar mejor las anomalías valvulares complejas y cuando es necesario descartar trombos intracardíacos o una fuente infecciosa que contribuye a la IC.
El ecocardiograma de esfuerzo y la prueba nuclear de esfuerzo sirven para descartar la isquemia como causa precipitante de IC, y la prueba farmacológica de esfuerzo, como la ecografía de esfuerzo con dobutamina (es decir cuando los tratamientos farmacológicos, en general vasodilatadores, se emplean para evaluar el flujo sanguíneo al corazón tras el ejercicio) pueden ayudar a evaluar la gravedad de la estenosis aórtica en pacientes con mala función ventricular.
La radiografía de tórax tiene baja sensibilidad y especificidad para detectar congestión pulmonar, ya que puede ser normal a pesar de disfunción ventricular izquierda considerable y sobrecarga de volumen. No obstante, la radiografía de tórax es importante porque contribuye a detectar el agrandamiento cardíaco y la patología pulmonar no cardíaca que pueden influir sobre las manifestaciones clínicas.
La tomografía por emisión de fotón único o PET se puede emplear para evaluar la presencia de isquemia y la viabilidad miocárdica. La resonancia magnética cardíaca se considera como la prueba de referencia para evaluar el volumen, la masa y la movilidad de la pared y es útil para determinar la etiología de la miocardiopatía al identificar la presencia de inflamación, fibrosis y patología infiltrativa.
La prueba de esfuerzo cardiopulmonar puede ayudar a relacionar la disnea y la fatiga con las respuestas metabólica, cardiovascular y pulmonar al ejercicio. Con el empleo de la cinta sin fin o la bicicleta y el análisis del intercambio gaseoso, los resultados de esta prueba son importantes componentes del algoritmo para determinar si el paciente es candidato para tratamientos avanzados, como el apoyo circulatorio mecánico y el trasplante cardíaco.
El umbral de consumo máximo de oxígeno con el ejercicio de 10–12 ml por kg por min en pacientes que logran su umbral anaeróbico se considera criterio para tratamientos avanzados.
Aunque no se recomienda el empleo habitual de catéteres en la arteria pulmonar para el diagnóstico de ICFEr, los mismos pueden ser útiles para pacientes con shock cardiogénico y para aquellos en quienes el tratamiento de la IC grave exige tratamiento con inotrópicos, o vasodilatadores.
Los catéteres en la arteria pulmonar también son útiles para el diagnóstico de la hipertensión y cuando se considera la candidatura para trasplante cardíaco. Sin embargo, quizás el uso más importante de catéteres en la arteria pulmonar sea para pacientes con estado hemodinámico incierto.
> Estadificación
La clasificación y estadificación de la IC es esencial para el diagnóstico y el tratamiento de los pacientes. La American College of Cardiology Foundation (ACCF) y la American Heart Association (AHA) crearon un sistema de estadificación donde las fases más tempranas incluyen a los pacientes en riesgo de sufrir IC y destacan así la importancia de modificar los factores de riesgo para prevenir la IC (Cuadro 1).
Los pacientes también se pueden clasificar según su estado funcional mediante la clasificación de la New York Heart Association (NYHA)
Los estadios de ACCF y AHA son progresivos y los pacientes van progresando a los estadios siguientes, que se asocian con mortalidad creciente. A la inversa, la clase de la NYHA del paciente puede cambiar según sus síntomas en breve tiempo.
| Estadio ACCF y AHA | Descripción de estadios ACCF AHAe | Clasificación funcional de NYHA | Descripción de la clasificación funciona |
| A | Alto riesgo de IC, pero sin cardiopatía estructural o síntomas | Ninguna | No aplicable |
| B | Cardiopatía estructural, pero sin signos o síntomas de IC | I | Sin limitación de la actividad física; la actividad física común no causa síntomas de IC |
| C | Cardiopatía estructural con síntomas previos o actuales de IC | I | Limitación leve de la actividad física; cómodo en reposo, pero la actividad física común produce síntomas de IC |
| II | Limitación leve de la actividad física; cómodo en reposo, pero la actividad física común produce síntomas de IC | ||
| III | Limitación importante de la actividad física cómodo en reposo, pero la actividad física más leve de lo común causa síntomas de IC | ||
| IV | No puede efectuar ninguna actividad física sin síntomas de IC, o síntomas de IC en reposo | ||
| D | IC resistente al tratamiento que exige intervenciones especializadas | IV | No puede efectuar ninguna actividad física sin síntomas de IC, o síntomas de IC en reposo |
> Prevención
Se hace mucho hincapie en la identificación, prevención y tratamiento las enfermedades que conducen a la IC, entre ellas la hipertensión, la hiperlipemia, la diabetes mellitus, la obesidad y el tabaquismo.
Para los pacientes en estadio A, el objetivo es prevenir la aparición de enfermedad cardiovascular y de patologías ventriculares estructurales, tratando los factores de riesgo y aconsejando sobre las modificaciones necesarias en la alimentación y el ejercicio.
Para los pacientes en estadio B, el objetivo es prevenir el desarrollo de más remodelado cardíaco e IC sintomática a través del inicio apropiado de tratamiento específico para la IC e intervenciones cuando estén indicadas. En pacientes con aumento del riesgo cardiovascular (pacientes >75 años, aquellos con enfermedad vascular, nefropatía crónica o un puntaje de riesgo de Framingham >15%), la presión arterial se debe mantener por debajo de 130/80.
| Tratamiento |
El tratamiento de los pacientes con IC es multifactorial y puede incluir tratamientos farmacológicos, implante de dispositivos médicos y trasplante cardíaco.
> Tratamiento farmacológico
Las recomendaciones actuales aconsejan tratar a todos los pacientes con ICFEr sintomática con un inhibidor de la enzima convertidora de angiotensina (IECA), un β-bloqueante y un antagonista de los mineralocorticoides. Los pacientes que no pueden tolerar los IECA deben recibir un bloqueante del receptor de angiotensina.
Estudios de observación efectuados en diferentes países muestran que si bien estos fármacos se recetan según las recomendaciones, la mayoría de los pacientes reciben una dosis subóptima.
Un estudio mostró la superioridad de sacubitril/valsartan (un receptor de la angiotensina II e inhibidor de la neprilisina) para disminuir la muerte cardiovascular, la hospitalización por IC y la mortalidad por todas las causas, la muerte súbita cardíaca y la muerte debida al agravamiento de la IC.
Además, el tratamiento con sacubitril/valsartan se asoció con menos síntomas y limitaciones físicas causadas por la IC. En conjunto, estos datos sugieren que este tratamiento se debe considerar para todos los pacientes salvo que haya contraindicaciones específicas o intolerancia comprobada.
Otros tratamientos farmacológicos para la ICFEr son los inhibidores del canal-1, los diuréticos y los anticoagulantes.
Varios estudios mostraron la falta de utilidad o, en algunos casos, el efecto perjudicial asociado con el empleo de ciertos tratamientos farmacológicos en pacientes con ICFEr. Por consiguiente, el empleo de estatinas, inhibidores de la renina, diltiazem o verapamilo, glitazona, AINE e inhibidores de COX2 no se recomiendan para pacientes sintomáticos.
>Tratamientos no farmacológicos
Estos tratamientos se considerarán cuando los pacientes con ICFEr no mejoran con el tratamiento farmacológico. La actividad física y el ejercicio regular se recomiendan a los pacientes que están en condiciones de hacerlo y la rehabilitación cardíaca puede ser útil en pacientes con IC, clínicamente estables, a fin de mejorar su estado funcional, calidad de vida y mortalidad.
> Dispositivos médicos
• Desfibrilador cardioversor implantable (DCI). Los pacientes con ICFEr, aún estando bien medicados, pueden sufrir muerte súbita por arritmias ventriculares. Las guías de Europa y de Estados Unidos recomiendan el empleo de DCI en pacientes con ICFEr sintomáticos (estadios C y D) y FE ≤ 35% a pesar de tratamiento farmacológico óptimo, durante ≥ 3 meses, siempre que el paciente tenga posibilidades de vivir > 1 año con buen estado funcional.
También se recomienda para pacientes con ICFEr que se recobraron de una arritmia ventricular con inestabilidad hemodinámica y que se espera que sobrevivan más de 1 año con buen estado funcional. El DCI no se recomienda en los primeros 40 días de un infarto de miocardio. Tampoco está demostrado que mejore la supervivencia en pacientes con baja FE sin enfermedad coronaria.
> Resincronización cardíaca. Este procedimiento es eficaz para mejorar la FE, el remodelado ventricular, los síntomas y para reducir la mortalidad en pacientes sintomáticos con ICFEr. Las guías lo recomiendan para pacientes sintomáticos con QRS ≥ 130 msec, morfología de bloqueo de rama izquierda y FE ≤ 35% a pesar del tratamiento médico óptimo.
El procedimiento es menos eficaz en pacientes con enfermedad coronaria y con fibrilación auricular.
> Insuficiencia cardíaca avanzada
Se trata de pacientes en estadio D, muy sintomáticos, resistentes al tratamiento convencional y con antecedentes de hospitalizaciones por descompensación cardíaca. Estos pacientes son candidatos a recibir apoyo mecánico circulatorio o trasplante cardíaco.
El apoyo mecánico circulatorio es un puente o intermedio hacia el trasplante cardíaco. Los avances en los dispositivos de asistencia ventricular de flujo continuo se asociaron con mejoría significativa en la calidad de vida, los síntomas y la supervivencia en estos pacientes y mostraron ser superiores a los dispositivos pulsátiles.
En los pacientes con insuficiencia biventricular, los dispositivos para ambos ventrículos resultaron ser mucho menos eficaces. La solución definitiva será el corazón artificial total, que por ahora está solo aprobado como puente al trasplante.
El tratamiento puente hacia el trasplante está especialmente indicado en pacientes en los que la espera de un donante afecta la supervivencia.
Sobre la indicación de apoyo mecánico circulatorio la clasificación de la Interagency Registry for Mechanically Assisted Circulatory Support (INTERMACS), permite diferenciar el nivel de gravedad de los pacientes con IC clase III o IV y sus implicancias pronósticas.
En Estados Unidos se implantaron 2.642 dispositivos de asistencia circulatoria mecánica y en el transcurso de un año el 31% de ellos recibió un trasplante. También se comprobó que son superiores a los dispositivos de asistencia pulsátil. La necesidad de cambiar el dispositivo por mal funcionamiento o trombosis fue del 9%. La supervivencia al año fue del 80% y del 70% a los dos años. Las experiencias europeas son similares.
> Trasplante cardíaco
La supervivencia al año es del 82% y del 69% a los 5 años, con un promedio de vida de 11 años
El trasplante cardíaco ofrece la mejor calidad de vida y la mayor supervivencia. Está indicado en pacientes con estadio D de ICFEr, dependientes de inotrópicos o con escaso rendimiento en las pruebas de ejercicio a pesar de un tratamiento óptimo.
Está contraindicado en pacientes con obesidad mórbida, hipertensión pulmonar irreversible, insuficiencia renal terminal, enfermedad cerebrovascular grave, diabetes con lesión de órgano blanco, abuso de drogas y cáncer activo o reciente|.
El número anual de trasplantes a nivel mundial según el registro de la International Society for Heart and Lung Transplantation (ISHLT) superó en 2014 los 4700 casos. La supervivencia al año es del 82% y del 69% a los 5 años, con un promedio de vida de 11 años. Las causas de mortalidad son:
- A los 30 días por rechazo del homoinjerto e insuficiencia multiorgánica.
- Al año por infecciones y rechazo agudo.
- A los 5 años por tumores y enfermedad coronaria.
Los nuevos inmunosupresores permiten tratamientos personalizados para disminuir las complicaciones, pero algunas de ellas siguen siendo frecuentes, como la hipertensión, la disfunción renal y la enfermedad coronaria del homoinjerto.
Para aumentar la cantidad de órganos disponibles se aumentó la proporción de donantes de más edad, especialmente en Europa. La media de edad de los donantes aumentó de 29 años en 1994 a 33 años en 2014. Para responder a la creciente población de pacientes ancianos se ampliaron los criterios para emparejar donantes y receptores que habitualmente están excluidos de los programas de trasplante.
> Monitoreo de los pacientes
El monitoreo remoto de los pacientes puede ser una manera de evaluar el agravamiento de la IC a fin de disminuir las hospitalizaciones y la mortalidad.
Las estrategias son el telemonitoreo, los cambios en la bioimpedancia, el empleo de biomarcadores y el monitoreo hemodinámico invasivo. Los resultados de estudios de telemonitoreo son promisorios.
Aunque más sensibles que el telemonitoreo, las estrategias basadas en la bioimpedancia en la actualidad se limitan a los pacientes que tienen otras indicaciones para dispositivos implantables.
Los monitores implantables pueden medir la frecuencia y el ritmo cardíacos, además de la presión arterial pulmonar o auricular. Las diversas formas de monitoreo remoto pueden complementar el tratamiento ambulatorio tradicional de los pacientes con IC, aunque aún restan desafíos a enfrentar con esas estrategias.
> Biomarcadores
La mayoría de los estudios se centraron en los péptidos natriuréticos BNP y NT-proBNP, que proporcionan información pronóstica. Los valores de los mismos aumentan debido a congestión, remodelado miocárdico, valvulopatía y arritmia, todos los cuales son posibles blancos terapéuticos. indicando que los valores de los péptidos natriuréticos pueden orientar el tratamiento.
Sin embargo, los resultados de los estudios no fueron uniformes, pero cuando se logró la reducción importante de los valores de BNP or NT-proBNP los pacientes evolucionaron mejor. Sin embargo, existe gran discrepancia entre los distintos estudios respecto de la fidelidad de estos péptidos como información pronóstica.
> Programas de tratamiento de la enfermedad
Varias de las recomendaciones actuales sobre IC señalan la importancia de un enfoque de tratamiento de la enfermedad para el manejo óptimo de estos pacientes. Un enfoque así incluye varios elementos clave como un sistema coordinado de tratamiento, provisión de sistemas de apoyo (visitas en el domicilio y telecuidado), identificación de poblaciones en riesgo, reciclado continuo entre el paciente y los proveedores de salud y mejoría de la salud global.
Estos programas demostraron que reducen las hospitalizaciones por IC y la mortalidad de los pacientes dados de alta después de un episodio de descompensación aguda. Sin embargo, después de más de 50 estudios no se alcanzó el modelo óptimo de tratamiento de la IC que pueda adaptarse al sistema de salud, la disponibilidad de recursos y las necesidades del paciente.
> Medicina personalizada
A diferencia de otras enfermedades crónicas, la ICFEr se trata sin objetivos individualizados, enfatizando poder alcanzar las dosis más altas toleradas de tratamiento médico. La estrategia de ajustar las dosis hasta el máximo tolerable es problemática ya que no todos los pacientes responden de la misma manera a las mismas dosis.
Lograr el tratamiento según las recomendaciones es difícil debido a la necesidad de ajuste frecuente de las dosis y evaluación especializada para asegurar las dosis más altas sin efectos tóxicos.
| Calidad de vida |
La IC afecta la calidad de vida del paciente y su familia con mayor intensidad que en otras enfermedades crónicas. Todos los aspectos de la calidad de vida se ven afectados y afectan la independencia y las relaciones sociales del paciente. El grado en que el paciente acepte su diagnóstico de IC y encuentre estrategias para afrontar sus consecuencias impacta favorablemente en la calidad de vida.
Para muchos pacientes es más importante recibir tratamientos que mejoren la calidad de vida que los que prolongan la esperanza de vida.
> Problemas terapéuticos actuales
Hay líneas de investigaciones abocadas a identificar a los pacientes de alto riesgo y prevenir la evolución hacia la IC.
En los pacientes con IC manifiesta es importante mejorar la función cardíaca, las morbilidades asociadas y desarrollar mejores sistemas de atención médica. Estos tópicos están subvalorados en los pacientes con ICFEr.
La respuesta variable de los pacientes ante los tratamientos convencionales sugiere el desarrollo y la aplicación de la farmacogenética y principalmente la aplicación de tratamientos personalizados.
Es necesario profundizar el conocimiento sobre los procesos fisiopatológicos (metabolismo cardíaco y producción de energía, reciclado proteico de los miocitos, función mitocondrial, comportamiento del calcio, microcirculación y fibrosis intersticial), para lograr mejores resultados.
A pesar de considerables avances en la creación de tratamientos farmacológicos y tratamientos con dispositivos para la ICFEr la gran mayoría de los pacienyes siguen teniendo mal pronóstico y alto riesgo de mortalidad
> Nuevos tratamientos
Los nuevos tratamientos para la ICFEr que están siendo evaluados en estudios clínicos son tratamientos farmacológicos, además del tratamiento con genes y tratamientos basados en implantes de células madre.
| Tratamiento | Mecanismo |
| Farmacológico | |
| Rivaroxaban | Anticoagulante oral directo |
| Omecamtiv Mecarbil/AMG 423 | Activador molecular pequeño de la miosina cardíaca |
| Empagliflozina | Inhibidor del cotransportador 2 de sodio/glucosa |
| Vericiguat | Aumenta la actividad enzimática de la guanilato ciclasa soluble y promueve la generación de cGMP (guanosina monofosfato cíclico) |
| Dapagliflocina | Inhibidor del SGLT2 (co-transportador de sodio-glucosa tipo 2) |
| Carboximaltosa férrica | Permite la entrega controlada de hierro a los tejidos blanco |
| Digitoxina | Inhibe la bomba de membrana Na+/K+-ATPasa |
| Procedimientos quirúrgicos | |
| Sistema de clipado mitral | Dispositivo percutáneo para el tratamiento de la insuficiencia mitral funcional |
| Trasplante de células | |
| Células pluripotenciales de la médula ósea | Tratamiento regenerativo de los mocitas |