Progresión y manejo de la neoplasia duodenal en la poliposis adenomatosa familiar

Introducción
La colectomía profiláctica ha mostrado que disminuye la incidencia de cáncer colorrectal y, en consecuencia, mejora las vidas de los pacientes con poliposis adenomatosa familiar (PAF) [1,2]. El cáncer duodenal y los desmoides son ahora las causas principales de muerte en la PAF [3,4]. Casi todos los pacientes con PAF desarrollarán pólipos duodenales; la mayoría tendrá una enfermedad en estadio temprano, con lenta progresión a estadios avanzados y un riesgo global de cáncer duodenal del 5% para la edad de 70 años, una tasa 100 a 330 veces mayor que la de la población general [5,6].
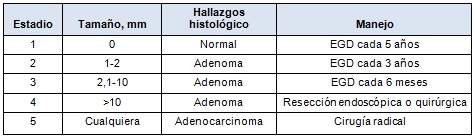
La severidad del adenoma duodenal ha sido clasificada por diferentes sistemas, para brindar un riesgo estratificado y opciones de manejo. Spigelman y col. [3], describieron 5 estadios (0-IV) de acuerdo con el número, tamaño, histología y grado de displasia de los pólipos, resultando en un riesgo de cáncer duodenal del 36% para los pacientes con enfermedad en estadio 4 (adenomatosis duodenal avanzada). Otro sistema de clasificación desarrollado por el grupo de los autores de este trabajo en el Familial Gastrointestinal Cancer Registry, en el Zane Cohen Centre del Mount Sinai Hospital, en Toronto, brinda un sistema de clasificación similar, más práctico clínicamente (1-5), basado principalmente en el tamaño de los pólipos (Tabla 1) [7]. La mayoría de los pacientes con PAF tendrá pólipos pequeños (< 2 mm) y tendencia a una lenta progresión de la enfermedad, con la mayoría no progresando a los estadios más avanzados [5,8,9]. La vigilancia del tracto gastrointestinal alto, para prevenir el desarrollo del cáncer duodenal, ha sido recomendada por la mayoría de las autoridades. Las guías para la frecuencia de la vigilancia y el manejo de las lesiones duodenales no son uniformes, y el resultado clínico ha sido decepcionante en algunas series, que han reportado una progresión al cáncer duodenal en el rango del 22% al 36%, en pacientes con poliposis duodenal avanzada [10-12].
Los defectos relativos de los programas de vigilancia son debidos, en parte, a la falta de conocimiento en relación con el riesgo de progresión maligna de los adenomas periampulares, y la controversia relacionada con el grado apropiado de agresividad necesario para erradicar los pólipos periampulares, previniendo – por lo tanto – el cáncer periampular [13]. La morbilidad y potencial mortalidad del manejo endoscópico o quirúrgico de la enfermedad duodenal debe ser balanceada contra el riesgo de desarrollar un carcinoma duodenal, teniendo el conocimiento de que la mayoría de las intervenciones no prevendrán completamente la recidiva de la enfermedad y que la vigilancia de por vida puede estar indicada para pacientes seleccionados [14-16].
Los objetivos de este estudio fueron tres: (1) identificar los factores de riesgo para desarrollar una poliposis duodenal avanzada y cáncer en la PAF; (2) evaluar la efectividad de sus protocolos de investigación y tratamiento para reducir el riesgo de cáncer duodenal en la PAF; y (3) describir la historia natural y el manejo de los pacientes con PAF con cáncer duodenal.
Métodos
Selección y descripción de los participantes
Este reporte describe el seguimiento a largo plazo de pacientes con PAF y adenomatosis duodenal, enrolados prospectivamente en el Familial Gastrointestinal Cancer Registry, en el Zane Cohen Centre del Mount Sinai Hospital, en Toronto, en un protocolo de vigilancia endoscópica gastrointestinal alta, desde 1980 hasta 2012. Todos los participantes tenían diagnóstico de PAF, basado en cualquiera de los siguientes [17]: (a) más de 100 pólipos adenomatosos colorrectales; (b) más de 10 pólipos y edad menor de 40 años; (c) más de 25 pólipos y edad mayor de 40 años y antecedentes familiares característicos (>100 pólipos en un miembro de la familia de primera generación; >25 pólipos en 2 parientes en 2 generaciones, incluyendo un miembro de la familia de primer grado; o una mutación adenomatous polposis coli [APC] en la línea germinal, diagnosticada en un pariente); o (d) confirmación de una mutación APC en la línea germinal. Los participantes fueron excluidos de este análisis si no estaban enrolados en el programa de vigilancia, o si fueron seguidos por diferentes médicos fuera del Mount Sinai Hospital.
Protocolo endoscópico
El sistema de estadificación del pólipo duodenal en la PAF y el programa de vigilancia y manejo han sido publicados previamente y se detallan en la Tabla 1 [7,18]. En resumen, el protocolo recomienda empezar la vigilancia a los 25 años de edad, aunque puede realizarse más tempranamente a criterio del médico tratante. Todos los exámenes endoscópicos fueron efectuados con un endoscopio de visión lateral, bajo sedación, y las biopsias fueron tomadas en la ampolla de Vater y en lesiones visibles en la primera, segunda o tercera porción del duodeno. El tamaño de los pólipos fue medido por comparación con las pinzas de biopsia abiertas. Se usaron rutinariamente fotografías para facilitar las comparaciones de la mucosa duodenal entre las sesiones endoscópicas. Los participantes con enfermedad en estadio 1 o 2, fueron categorizados como no teniendo o teniendo pólipos duodenales pequeños; aquellos con enfermedad en estadio 3 o 4 fueron categorizados como teniendo adenomatosis duodenal avanzada.
Los pacientes con estadio 1 (sin pólipos) y estadio 2 (pólipos de tamaño pequeño: 0,1-2 mm) fueron seguidos con esofagogastroduodenoscopía (EGD) cada 5 y 3 años, respectivamente; aquellos con enfermedad en estadio 3 (pólipos de tamaño medio: 2,1-10 mm) fueron seguidos con EGD cada 6 meses. Los pólipos de tamaño medio fueron removidos si abrigaban una displasia de alto grado (DAG). Si esos pólipos eran únicos o unos pocos, eran removidos endoscópicamente; no obstante, si la biopsia con DAG había sido obtenida de una mucosa tapizada por pólipos, se prefirió la resección quirúrgica. A los pacientes con enfermedad en estadio 4 (pólipos de gran tamaño: > 10 mm) se les ofreció terapia endoscópica de los pólipos, a cargo de un endoscopista intervencionista. Los pólipos grandes aislados (> 10 mm) no susceptibles de tratamiento endoscópico, fueron removidos a través de un abordaje quirúrgico transduodenal. Si los pólipos eran numerosos sin una lesión única dominante (tapizado) o si el paciente tenía evidencias de cáncer (enfermedad en estadio 5), se ofreció una duodenopancreatectomía. A los pacientes con enfermedad en estadio 3 que tenían DAG se les ofreció el mismo abordaje que aquellos con enfermedad en estadio 4.
• TABLA 1: Estadificación y manejo de la poliposis duodenal en la PAF
Todos los pacientes fueron sometidos a evaluación endoscópica 6 meses después de cualquier intervención endoscópica o quirúrgica. La vigilancia alejada del duodeno o del asa yeyunal aferente post duodenopancreatectomía, se basó en los hallazgos endoscópicos postoperatorios y en la clasificación de la estadificación. Los casos que fueron bajados de estadio 4, fueron seguidos y tratados indefinidamente como pacientes de alto riesgo [16].
Intervenciones endoscópicas
Se ofreció una variedad de intervenciones endoscópicas a los pacientes, tanto con enfermedad en estadio 3 con DAG, como con enfermedad en estadio 4, con o sin DAG. La polipectomía usando la técnica simple con asa fue el procedimiento endoscópico más común, especialmente para los pólipos de 10-20 mm de diámetro, o para aquellos menores a 10 mm con evidencia de DAG en la biopsia previa. El uso de técnicas endoscópicas ablativas – terapia fotodinámica o coagulación con plasma de argón (ERBE, Marietta, GA) – fue empleado comúnmente para los pólipos sésiles, aquellos mayores de 20 mm, o para lesiones con “tapizado” extenso, tanto para reducción, ablación o tratamiento de lesiones remanentes, después de una resección “fragmentada”. La coagulación con plasma de argón fue realizada usando una sonda de disparo hacia delante ajustada a 1 L por minuto y 30 Watts. El abordaje a los pacientes con pólipos grandes, que no podían ser resecados endoscópicamente con la técnica en asa, ha cambiado con los años, y el abordaje fragmentado no es usado más, debido a la alta tasa de recidiva en el área resecada. Los autores prefieren en la actualidad la resección mucosa endoscópica (RME), para las lesiones sésiles elevadas mayores a 10 mm.
El manejo de los pólipos ampulares fue similar al de los pólipos duodenales. La ampulectomia endoscópica fue realizada cuando un pólipo confinado a la ampolla medía más de 10 mm o tenía evidencia de DAG, aún si era menor a 10 mm. Ese procedimiento endoscópico involucró la técnica en asa y electrocauterio con corriente monopolar mezclada. La colangiopancreatografia endoscópica retrógrada (CPER) fue realizada en todos los pacientes sometidos a ampulectomía endoscópica y se colocó rutinariamente un stent en el conducto pancreático, para prevenir la pancreatitis.
Evaluación anatomopatológica
Tres patólogos con interés en la patología gastrointestinal y con experiencia en la clasificación de pólipos adenomatosos del tracto gastrointestinal, particularmente en la PAF, examinaron todos los pólipos duodenales de los casos locales y de los derivados de afuera. Las biopsias de los especímenes duodenales fueron sometidas a un estricto protocolo, para determinar la DAG (complejidad arquitectónica marcada con alteración neoplásica inequívoca del epitelio duodenal equivalente a un carcinoma in situ) [19-21]. Los tres patólogos gastrointestinales revisaron todas las consultas externas y se obtuvo una consulta liberal, de modo que 2 patólogos gastrointestinales examinaron cualquier pólipo con componente de DAG.
Recolección de datos
El estudio se realizó con la aprobación del Mount Sinai Hospital Research Ethics Board (REB: 12-0224-C). Todos los pacientes dieron su consentimiento informado para la inclusión de sus datos en la base de datos. Los datos fueron recolectados e ingresados prospectivamente en el Familial Gastrointestinal Cancer Registry. Las características basales, seleccionadas a priori por estar potencialmente asociadas con progresión de la adenomatosis duodenal, incluyeron: sexo, edad de la primera EGD, antecedentes familiares, tipo de la primera cirugía colorrectal, tiempo desde la primera operación colorrectal hasta la primera EGD y estadio en la primera EGD. Las variables recolectadas de cada espécimen obtenido durante la biopsia endoscópica o cirugía incluyeron: tamaño y número de los pólipos, reportes histopatológicos incluyendo tipo de pólipo (mucosa normal, tubular, tubulovellosa o adenoma velloso), grado de displasia (baja o DAG), tipo de intervención (polipectomía endoscópica, ampulectomía, coagulación con plasma de argón, ablación térmica, RME o cirugía) y resultados periprocedimiento o perioperatorios. La enfermedad fue estadificada desde 1 a 5, con base en los hallazgos endoscópicos y anatomopatológicos.
Análisis estadístico
Las características basales son presentadas como variables categóricas. Las curvas acumulativas de eventos de Kaplan-Meier fueron estimadas desde el momento en que cada paciente entró al estudio con su primera EGD, hasta la EGD más temprana detectando enfermedad en estadio 4 o 5, para la cohorte como un todo y subdividida por el estadio a la presentación. Los pacientes fueron censurados en su última EGD si no tenían resultado de interés en ese momento. Las regresiones univariables de riesgo proporcional para todas las características basales fueron estimadas para el tiempo a los estadios 4 y 5. Se estimó una regresión multivariable de riesgos proporcionales incluyendo a todas las co-variables basales, con log-rank P < 0,25 para el tiempo al estadio 4, pero no para el estadio 5, debido al número escaso de eventos. Para evitar una matriz de covarianza singular, se estimaron 2 modelos multivariables con diferente tratamiento de las cirugías colorrectales: el Modelo 1 incluyó la cirugía colorrectal, pero no el tiempo desde la misma hasta la primera EGD, y el Modelo 2 incluyó el tiempo desde la cirugía colorrectal hasta la primera EGD, pero no el tipo de cirugía. Se usó la prueba del coeficiente de probabilidad para calcular los valores de P para las covariables en las regresiones proporcionales de riesgo. Las complicaciones de los procedimientos endoscópicos o quirúrgicos son presentadas como porcentaje del número total de exámenes. Se definió la significación estadística como P < 0,05 y todas las pruebas fueron de 2 lados. Los cálculos fueron realizados utilizando el programa R, versión 2.15.2.
Resultados
Características basales en la primera EGD y seguimiento
La cohorte incluyó el espectro habitual de pacientes con PAF. Hubo un total de 218 pacientes (todos los estadios), de los que 98 tenían poliposis duodenal avanzada (estadios 3 y 4 de la enfermedad). Hubo un número similar de hombres y mujeres. La edad de los pacientes al momento de la primera EGD estaba normalmente distribuida e iba desde los 10 a los 72 años. Aunque todos los pacientes habían tenido eventualmente una cirugía colorrectal, aproximadamente el 16% no habían tenido una colectomía al momento de la primera EGD. La mayoría de los pacientes que había tenido una cirugía colorrectal antes de ingresar al estudio, tuvieron una colectomía con anastomosis ileorrectal; los restantes tuvieron una proctocolectomía restauradora o una hemicolectomía derecha. Menos de la mitad de los pacientes que tuvieron una cirugía colorrectal antes de ingresar al estudio, había sido operada dentro de los 5 años, con muchos ingresando después de 20 años. Cerca de la mitad de los pacientes tenía enfermedad en estadio 1 cuando ingresaron al estudio; 14 pacientes (8%) tenían enfermedad en estadio 4.
Tres cuartos de los pacientes fueron seguidos por más de 5 años y más de la mitad por más de 10 años. El 16% de los pacientes tuvo sólo 1 EGD durante el período del estudio y no fueron incluidos en el análisis de progresión de la enfermedad. Hubo 15 muertes en la cohorte, 2 de las cuales fueron atribuidas a cáncer duodenal, 3 a cáncer pancreático y 2 a enfermedad desmoide. Otras causas de muerte incluyeron: melanoma y cáncer de colon, pulmón, cerebro, yeyuno, tiroides y estómago. Un paciente falleció por complicaciones sépticas de una intervención endoscópica. Para señalar: hubo 5 pacientes no incluidos en la cohorte porque rechazaron el seguimiento con EGD y fueron reportados al Registry como habiendo muerto por cáncer duodenal.
Progresión a estadios 4 y 5
Sesenta y seis de los 167 pacientes con enfermedad en estadios 1, 2 y 3, en la primera EGD, progresaron a un estadio 4. La mediana global del tiempo desde la primera EGD hasta la enfermedad en estadio 4 fue de 22,4 años. El riesgo de enfermedad en estadio 4 fue del 4,2% (95% intervalo de confianza [IC]: 1,1-7,3), 12,2% (95% IC: 6,9-17,3), 20,1% (95% IC: 13,3-27,4) y 34,4% (95% IC: 23,8-43,4), a 1, 5, 10 y 15 años, respectivamente. Las características basales asociadas significativamente con el riesgo de enfermedad en estadio 4 en las regresiones univariables fueron: sexo, edad, tipo de cirugía colorrectal, años desde la cirugía colorrectal y estadio en la primera EGD. En el Modelo 1, el sexo, tipo de cirugía colorrectal y estadio, estuvieron asociados significativamente con el riesgo de progresión al estadio 4. En el Modelo 2, el sexo, los años desde la cirugía colorrectal y el estadio, estuvieron significativamente asociados con el riesgo de progresión al estadio 4. En los modelos multivariables, la edad no estuvo más asociada significativamente con la progresión.
El estadio 5 de la enfermedad se desarrolló en 5 de 184 pacientes con estadios 1, 2, 3 y 4 en la primera EGD, que tuvieron endoscopías subsiguientes. El riesgo de estadio 5 de la enfermedad fue de 0%, 0,7% (95% IC: 0-2,2) y 2,1% (95% IC: 0-5,2) a los 5, 10 y 15 años, respectivamente. Todos los pacientes que desarrollaron un estadio 5 tuvieron un diagnóstico previo de enfermedad en estadio 4, con DAG en la biopsia endoscópica. El cáncer duodenal se desarrolló después de una mediana de 15 años (rango: 13-17), después de la primera endoscopía. La mediana del tiempo transcurrido desde una enfermedad en estadio 3 hasta el cáncer fue de 14 años (rango: 5-17) y desde estadio 4 hasta el cáncer, de 11,6 años (rango: 2,2-18). El cáncer duodenal no fue un hallazgo incidental en la cirugía de ninguno de los pacientes. Aunque hubo muy pocos eventos significativos para la estimación de la tasa de riesgo, las características basales que estuvieron significativamente asociadas con el desarrollo del cáncer en las regresiones univariables fueron, el tipo de cirugía colorrectal y el estadio al momento de la primera EGD.
Intervenciones endoscópicas y quirúrgicas para los pacientes con poliposis duodenal avanzada
Entre aquellos pacientes que desarrollaron una poliposis duodenal avanzada, se efectuó un total de 104 polipectomías endoscópicas durante el período del estudio, en 57 de 98 pacientes (60%), con una mediana de 2 polipectomías por paciente. La mediana de la edad de la primera polipectomía endoscópica fue de 47,5 años (rango: 26-75), de 5,8 años (rango: 1-25) desde la primera EGD y de 19 años (rango: 0-42) desde la primera cirugía colorrectal. Nueve pacientes (9/98; 9%) fueron sometidos a ampulectomía endoscópica a una mediana de edad de 47 años (rango: 26-75). Los hallazgos histopatológicos de las polipectomías endoscópicas fueron pólipos mayores de 10 mm, con o sin DAG, en 64 de 104 procedimientos (62%). El 90% de los pacientes (8/9) sometidos a ampulectomía endoscópica, tuvo pólipos mayores de 10 mm, con o sin DAG. La tasa de complicación fue del 20% con 11 de 104 casos (11%) con hemorragia, 9 de 104 casos (9%) con pancreatitis y 1 muerte en 104 casos (1%) a causa de una pancreatitis grave que condujo a la sepsis, después de una ampulectomía endoscópica. La recidiva en el área resecada después de una resección endoscópica “fragmentada” fue común. Todos los pacientes desarrollaron recidiva después de polipectomía con asa o técnicas ablativas, aunque ese patrón de recurrencia estuvo generalmente localizado en el área proximal al sitio de resección.
Hubo 21 pacientes que fueron sometidos a resección quirúrgica de neoplasias periampulares, con un total de 25 procedimientos efectuados, incluyendo 15 (60%) duodenopancreatectomías, 9 (36%) polipectomías/ampulectomías abiertas, y 1 (4%) resección duodenal segmentaria. La primera resección quirúrgica fue realizada a una mediana de edad de 51 años (rango: 1,5-50), de 6,3 años (rango: 1-25) desde la primera EGD y de 17,5 años (rango: 1,5-50) desde la primera cirugía colorrectal. Los hallazgos anatomopatológicos después de la intervención quirúrgica fueron los siguientes: numerosos pólipos mayores de 10 mm, sin DAG, en 7 de 25 casos (28%); numerosos pólipos mayores de 10 mm, con DAG, en 13 de 25 casos (52%) y cáncer duodenal en 5 de 25 casos (20%). Hubo 9 de 15 pacientes (60%) con complicaciones mayores (clasificación de Clavien-Dindo ≥ 3) [22], después de la duodenopancreatectomía y una tasa de filtración pancreática del 40% (6/15), la mayoría de Grado B (3/6), de acuerdo con el International Study Group of Postoperative Pancreatic Fistula [23]. No hubo complicaciones mayores o muertes perioperatorias después de las polipectomías o ampulectomías abiertas. La tasa de recidiva, después del tratamiento quirúrgico local, fue del 100% en el duodeno remanente, y la tasa de recidiva, en la rama aferente, después de la duodenopancreatectomía, fue de 33% (5/15), con 1 paciente desarrollando cáncer del intestino delgado en la rama aferente biliopancreática.
Pacientes con cáncer duodenal
Cinco pacientes desarrollaron cáncer duodenal. Caso N° 1: hombre de 59 años de edad, con enfermedad en estadio 2, que desarrolló estadio 4 a la edad de 63 años. Su estatus de alto riesgo cardíaco impidió una cirugía abdominal mayor y sus pólipos duodenales eran demasiado grandes para tratamiento endoscópico; por lo tanto, fue sometido a reducción de masa endoscópica, hasta que se le diagnosticó un adenocarcinoma a la edad de 65 años. Fue sometido a resección duodenal segmentaria, en vez de una duodenopancreatectomía, debido a su alto riesgo quirúrgico, falleciendo eventualmente por carcinomatosis. Caso N° 2: mujer de 32 años de edad, con enfermedad en estadio 2, que progresó a estadio 4 a los 52 años. Se le realizaron múltiples polipectomías endoscópicas hasta los 58 años, cuando se le efectuó una duodenopancreatectomía por un adenocarcinoma duodenal T3N1. Recibió quimioterapia adyuvante con gemcitabina y está viva en la actualidad, sin enfermedad, 5 años después de la cirugía por cáncer. Caso N° 3: hombre de 39 años de edad, con enfermedad en estadio 2 que progresó a estadio 4, no susceptible de terapia endoscópica debido al patrón difuso de la enfermedad, a la edad de 46 años.
Comentarios
Para ver los comentarios de sus colegas o para expresar su opinión debe ingresar con su cuenta de IntraMed.










