 En este artículo, el autor se centra sobre estudios recientes con espectroscopia por resonancia magnética (ERM) sobre la acumulación de lípidos ectópicos en la patogenia de la resistencia a la insulina en el músculo y el hígado.
En este artículo, el autor se centra sobre estudios recientes con espectroscopia por resonancia magnética (ERM) sobre la acumulación de lípidos ectópicos en la patogenia de la resistencia a la insulina en el músculo y el hígado.
Habría un posible vínculo entre la inflamación y la lipólisis inducida por macrófagos en la progresión de la resistencia a la insulina - inducida por lípidos ectópicos - a intolerancia a la glucosa y diabetes 2.
Resumen
La reducción inducida por lípidos en el transporte de la glucosa estimulado por la insulina se podría atribuir a un defecto proximal de las señales de insulina debido a una señal intracelular derivada de los ácidos grasos. La causa más frecuente de depósito ectópico de lípidos en el músculo esquelético y el hígado es el consumo de calorías superior al gasto calórico y la disminución de estos lípidos ectópicos se asocia con la neutralización de la resistencia a la insulina en estos órganos.
También se observó que la disfunción mitocondrial adquirida es un importante factor predisponente para la acumulación ectópica de lípidos y la resistencia a la insulina en los ancianos.
Los estudios muestran la importancia de la acumulación ectópica de lípidos en la patogenia de la resistencia a la insulina en el músculo y el hígado. Este modelo también explica la mejor acción de la insulina con el ejercicio, el adelgazamiento y las tiazolidinedionas. Asimismo, aumentar el gasto hepático de energía al favorecer el desacoplamiento mitocondrial podría ser un enfoque novedoso para tratar la epidemia de hígado graso no alcohólico, el síndrome metabólico y la diabetes tipo 2.
Introducción
La diabetes tipo 2 afecta a gran número de personas en todo el mundo y es la causa principal de nefropatía terminal, de pérdida de un miembro no causada por traumatismo y de ceguera. Según las proyecciones, cabe esperar que la prevalencia mundial de diabetes tipo 2 aumente en más de un 75% durante las próximas dos décadas, en especial en Asia.
Aunque la disfunción de las células beta es responsable de la progresión de la normoglucemia a hiperglucemia, la resistencia a la insulina es anterior a esta disfunción y tiene una importante función en la patogenia de la diabetes tipo 2. Tras el consumo de hidratos de carbono, la glucosa se deposita principalmente en los músculos y en el hígado en forma de glucógeno y las alteraciones de la sensibilidad a la insulina en estos órganos producen hiperglucemia en ayunas y posprandial.
En este artículo, el autor se centra sobre estudios recientes con espectroscopia por resonancia magnética (ERM) sobre la acumulación de lípidos ectópicos en la patogenia de la resistencia a la insulina en el músculo y el hígado y dilucidaron la importancia de la resistencia a la insulina específica del músculo para favorecer el aumento de la lipogénesis hepática, el hígado graso no alcohólico y la dislipidemia aterógena. Propone después un posible vínculo entre la inflamación y la lipólisis inducida por macrófagos en la progresión de la resistencia a la insulina - inducida por lípidos ectópicos - a intolerancia a la glucosa y diabetes tipo 2.
Hipótesis del ciclo de los ácidos grasos en la resistencia a la insulina en el músculo
La asociación entre el depósito excesivo de lípidos en la obesidad y la resistencia a la insulina se conoce desde hace tiempo, y estudios ERM de protones (1H) mostraron una relación aún más estrecha entre el contenido intramiocelular de lípidos y la resistencia a la insulina en el músculo. No obstante, aún no hay acuerdo sobre el mecanismo molecular por el cual la grasa causa resistencia a la insulina. Hace más de un siglo, Randall y colaboradores propusieron la primera hipótesis, que posteriormente fue refutada por otros estudios.
La hipótesis actual es que la acumulación de un metabolito lipídico intracelular interviene en la resistencia a la insulina asociada con la obesidad y la diabetes tipo 2 al causar defectos en las señales de la insulina y disminuir la actividad de transporte de la glucosa estimulada por la insulina.
Mecanismos moleculares de la resistencia a la insulina en el músculo y en el hígado
La acción de la insulina en el músculo y el hígado exige la transmisión coordinada de las señales intracelulares que afectan sobre todo la fosforilación y la desfosforilación. En el músculo esquelético, la insulina fija y activa el receptor de insulina tirosinacinasa, con la ulterior fosforilación del sustrato 1 del receptor de insulina (IRS-1 por las siglas del inglés).
Una vez fosforilado, IRS-1 fija y activa la fosfatidilinositol 3-cinasa (PI3K), que a su vez, a través de intermediarios de señales, promueve la traslocación del transportador de glucosa tipo 4 (GLUT4) a la membrana celular, lo que produce la captación de glucosa en el músculo esquelético.
La fosforilación de la tirosina del IRS-1 estimulada por la insulina y la activación asociada de PI3K están alteradas en el músculo durante la infusión de lípidos en seres humanos y en roedores. Esto indica que la reducción inducida por lípidos en el transporte de la glucosa estimulado por la insulina se podría atribuir a un defecto proximal de las señales de insulina debido a una señal intracelular derivada de los ácidos grasos. Esta señal se identificó en estudios en roedores a los que se les administró una infusión de lípidos o se los alimentó con alto contenido de grasas. Los roedores tuvieron aumentos transitorios del contenido muscular de diacilglicerol (DAG) y activación sostenida de la forma teta de la proteína cinasa C (PKCθ), que activó la cascada de una serina– treonina y la inhibición de las señales de insulina.
En seres humanos se mostró que el contenido de DAG aumenta transitoriamente en el músculo esquelético tras la infusión de lípidos más heparina o de lípidos solos, El aumento del contenido de DAG en el músculo se asocia con aumentos en la actividad de PKCθ y la fosforilación de IRS-1 en Ser 1101.
Además, se observó aumento del contenido muscular de DAG, junto con aumento de la actividad de PKCθ y aumento de la fosforilación de la serina de IRS-1, en el músculo de personas obesas con resistencia a la insulina y personas con diabetes tipo 2.
La activación por DAG de una nPKC causa resistencia a la insulina tanto en el hígado como en el músculo. La esteatosis hepática y la resistencia hepática a la insulina aparecen en roedores tras sólo unos pocos días de alimentación abundante en grasas, sin cambios significativos en el contenido lipídico o la resistencia a la insulina en el músculo. En este modelo, la esteatosis hepática y la acumulación hepática de DAG se asociaron con defectos proximales de las señales de insulina con disminución de la fosforilación de la tirosina del IRS-1 e IRS-2 estimulada por la insulina y por el receptor de insulina, que finalmente interfiere con la activación de la síntesis de glucógeno y la supresión de la producción de glucosa en el hígado, inducidas por la insulina.
La alteración de la síntesis de glucógeno hepático estimulada por la insulina es similar a la de los pacientes con diabetes tipo 2. La asociación entre la activación de DAG–PKCε en el hígado y la resistencia hepática a la insulina se mostró en numerosos modelos de roedores transgénicos con hígado graso no alcohólico. Más importante, el aumento del contenido hepático de DAG y el aumento de la actividad de PKCε son los factores pronósticos más fuertes de resistencia hepática a la insulina en personas obesas con hígado graso no alcohólico.
Disociación entre la obesidad y la resistencia a la insulina en el músculo y en el hígado
La causa más frecuente de depósito ectópico de lípidos en el músculo esquelético y el hígado es el consumo de calorías superior al gasto calórico. Al contrario de la obesidad, las lipodistrofias ofrecen la oportunidad de evaluar la función del depósito de lípidos ectópicos sin la contribución de ninguna expansión de masa de tejido adiposo periférico o visceral. La falta de grasa subcutánea lleva a la hipertrigliceridemia, el depósito ectópico de grasa (incluida una considerable esteatosis hepática) y una profunda resistencia a la insulina en el músculo y el hígado.
En ratones lipoatróficos A-ZIP/F-1, que no tienen adipocitos, se acumula grasa en el hígado y el músculo esquelético, tejidos en los que se produce una profunda resistencia a la insulina. Si se les trasplanta grasa por vía subcutánea, se normaliza el contenido lipídico ectópico en el músculo y el hígado, así como las señales y la acción de la insulina en estos órganos.
Otra evidencia que apoya la importancia de la acumulación de lípidos ectópicos en la patogenia de la resistencia a la insulina en el músculo y el hígado surge de estudios en ratones transgénicos. Ratones transgénicos con sobrexpresión de la lipoproteína lipasa en el hígado tienen acumulación de grasa específica para el hígado y resistencia a la insulina específica para el hígado.
Asimismo, ratones transgénicos con sobrexpresión de la lipoproteína lipasa en el músculo esquelético tienen acumulación de grasa específica para el músculo y resistencia a la insulina específica para el músculo. En conjunto, estos estudios muestran que la acumulación ectópica de lípidos intracelulares conduce a la resistencia a la insulina en el músculo y el hígado, incluso en ausencia de adiposidad periférica y visceral y que los DAG son los metabolitos derivados de los lípidos responsables de desencadenar la resistencia a la insulina mediante la activación de PKCε en el hígado y PKCθ en el músculo.
En unas pocas excepciones, la acumulación de lípidos ectópicos en el músculo y el hígado se disocia de la resistencia a la insulina. Una de estas excepciones es el síndrome de Chanarin–Dorfman, debida a la deficiencia de la proteína llamada identificación de genes comparativa 58 (CGI-58). Estudios mostraron que la compartimentación de los DAG dentro de las gotitas lipídicas es la probable explicación de la disociación entre la acumulación de lípidos ectópicos y la resistencia a la insulina en este síndrome. Aún no se sabe si la explicación es la misma para la disociación entre el aumento de la acumulación de líquidos ectópicos y la resistencia a la insulina en otros casos, como la hipobetalipoproteinemia familiar y en el músculo de los atletas de resistencia.
Importancia de la disfunción mitocondrial en la acumulación de lípidos ectópicos
El contenido lipídico de las células musculares refleja un equilibrio entre la captación de ácidos grasos por las células y la oxidación de las grasas mitocondriales. La disfunción mitocondrial adquirida es un importante factor predisponente para la acumulación ectópica de lípidos y la resistencia a la insulina en los ancianos. Se halló que en personas ancianas, delgadas, la captación de glucosa estimulada por la insulina era mucho menor que la de personas jóvenes emparejadas para la masa magra y la masa grasa.
En ancianos, la resistencia a la insulina en el músculo se asoció con aumento de la acumulación lipídica en las células musculares y reducción de aproximadamente el 40% en la actividad oxidativa y de fosforilación mitocondrial, evaluada mediante ERM C y P in vivo, en relación con la actividad oxidativa y de fosforilación en controles jóvenes. Estos datos avalan la hipótesis de que las reducciones de la función mitocondrial asociadas con la edad, posiblemente debidas a daño acumulado por las especies reactivas del oxígeno (ERO), predisponen a los ancianos a la acumulación ectópica de lípidos y la resistencia a la insulina en el músculo.
Estudios en ratones transgénicos con sobrexpresión de catalasa humana dirigida hacia las mitocondrias apoyan esta hipótesis.
En conjunto, estos datos muestran que las reducciones adquiridas de la función mitocondrial asociadas con la edad promueven la acumulación ectópica de lípidos en el músculo esquelético y la resistencia a la insulina en el músculo. También sugieren que conservar la función mitocondrial mediante la reducción del daño oxidativo mitocondrial puede ser un objetivo terapéutico para prevenir la disminución de la función mitocondrial en el músculo asociada con la edad, la resistencia a la insulina en el músculo y la diabetes tipo 2 en los ancianos.
Disminuciones de aproximadamente el 40% en la actividad oxidativa y de fosforilación mitocondrial en el músculo se observaron en jóvenes sanos, delgados, con resistencia a la insulina, cuyos padres padecen diabetes tipo 2. La disminución del flujo en el ciclo del ácido tricarboxílico y de la síntesis del ATP en el músculo fue paralela a la disminución de aproximadamente el 40% del contenido mitocondrial.
Es así probable que la reducción del contenido mitocondrial, debida a la disminución de la biogénesis mitocondrial, sea responsable de la reducción de la actividad oxidativa y de fosforilación de las mitocondrias y puede ser una alteración adquirida. No obstante, dada la función clave de la actividad mitocondrial en la regulación del metabolismo del as grasas en las células musculares, estos datos sugieren que la función mitocondrial reducida puede ser un importante factor predisponente que promueve la acumulación de DAG en las células musculares y la resistencia a la insulina en el músculo en personas con resistencia a la insulina cuyos padres padecen diabetes tipo 2.
Alteraciones que favorecen la acumulación de lípidos ectópicos en el hígado
Aunque el hígado graso no alcohólico casi siempre se asocia con obesidad, hay excepciones importantes a esta regla, donde se observan hígado graso no alcohólico y resistencia hepática a la insulina en personas delgadas.
Polimorfismos en la respuesta a la insulina del gen que codifica la apolipoproteína C3 (APOC3) predisponen a estas personas al hígado graso no alcohólico y la resistencia hepática a la insulina.
Estos polimorfismos generan un aumento del 30% de la apolipoproteína C3 plasmática. Este aumento inhibe la actividad de la lipoproteína lipasa, limitando la depuración periférica de quilomicrones y causando hipertrigliceridemia posprandial. Como resultado, los portadores de las variantes de APOC3 tienen aumento de la captación hepática de lípidos de los restos de los quilomicrones, que los predisponen al hígado graso no alcohólico y a la resistencia hepática a la insulina.
La evidencia genética en apoyo de la importancia de las alteraciones de la apolipoproteína en la regulación de la síntesis hepática de triglicéridos proviene de estudios en ratones transgénicos con sobreexpresión de la apolipoproteína C3 en el hígado.
Estos estudios sugieren que las interacciones entre genes y medioambiente pueden predisponer a personas delgadas al hígado graso no alcohólico, la resistencia hepática a la insulina y la diabetes tipo 2 y estas interacciones pueden también afectar muchas posibles variantes de las apolipoproteínas plasmáticas que involucran la actividad de la lipoproteína lipasa. La interacción gen-ambiente de la APOC3 se observó sólo en hombres. Es probable que esto refleje un efecto protector del estradiol sobre la capacidad de la apolipoproteína C3 para inhibir la actividad de la lipoproteína lipasa y favorecer el depósito de grasa ectópica en mujeres premenopáusicas.
Además, la interacción gen APOC3- ambiente no se observa en personas obesas; éstas tienen esteatosis hepática, que enmascara el efecto relativamente sutil de las variantes de APOC3 para predisponer a las personas al hígado graso y la resistencia hepática a la insulina.
Los hispanoamericanos son otro gran grupo étnico en riesgo de hígado graso no alcohólico, resistencia a la insulina y diabetes tipo 2. Se identificó una mutación de aminoácido (I148 M in PNPLA3) que es más frecuente en hispanoamericanos que en otros grupos étnicos y se asocia fuertemente con el hígado graso.
Por último, los genes que regulan la lipogénesis (e.g., AGPAT2 y PPARG), y llevan a la lipodistrofia, y las alteraciones de los genes que regulan la lipólisis (e.g., los genes que codifican la perilipina [PLIN1]) también generan acumulación de lípidos ectópicos y resistencia a la insulina.
Neutralización de la resistencia a la insulina y la diabetes mediante la reducción de la grasa ectópica
Otra evidencia de que la acumulación de lípidos ectópicos en el músculo y el hígado tiene una función causal en la patogenia de la resistencia a la insulina y la diabetes tipo 2 proviene de estudios que muestran que la disminución del contenido de lípidos ectópicos se asocia con la neutralización de la resistencia a la insulina en estos órganos. Un estudio indicó que el restablecimiento de la leptina plasmática a niveles fisiológicos en pacientes con diabetes y lipodistrofia normalizó la glucemia en ayunas y las concentraciones plasmáticas de lípidos.
Estas mejorías del metabolismo de la glucosa estimulado por la insulina, que se pueden atribuir a la neutralización de la resistencia a la insulina en el músculo y el hígado, se asociaron con grandes disminuciones del contenido hepático de triglicéridos y del contenido de grasa en los miocitos.
Asimismo, el descenso de aproximadamente el 10% del peso corporal con una dieta hipocalórica disminuyó notablemente las concentraciones de triglicéridos hepáticos y normalizó la sensibilidad hepática a la insulina, la producción hepática de glucosa y la glucemia en ayunas en pacientes con diabetes tipo 2.
Se observaron disminuciones de la grasa de los miocitos y neutralización de la resistencia a la insulina en el músculo tras el descenso de aproximadamente el 10% del peso en personas jóvenes y delgadas con resistencia a la insulina cuyos padres sufrían diabetes tipo 2.
Las tiazolidinedionas también disminuyen la esteatosis hepática y mejoran la sensibilidad a la insulina en el músculo y el hígado, al aumentar la sensibilidad a la insulina de los adipositos y desplazar los lípidos ectópicos del músculo y el hígado al tejido adiposo subcutáneo.
Resistencia a la insulina en el músculo esquelético, dislipidemia e hígado graso no alcohólico
El aumento de las grasas en los miocitos y la resistencia a la insulina en el músculo esquelético son defectos iniciales observados en la patogenia de la diabetes tipo 2.
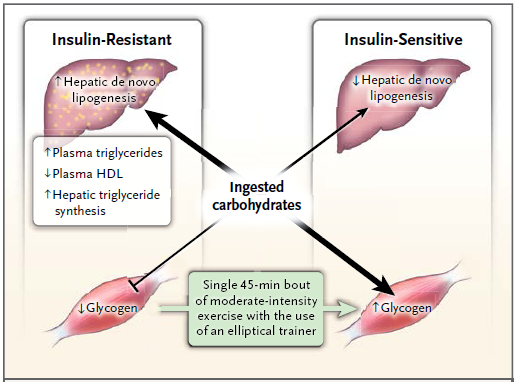
En personas jóvenes sanas, la resistencia selectiva a la insulina en el músculo favorece la dislipidemia aterógena al cambiar el patrón de los hidratos de carbono consumidos, de la síntesis de glucógeno en el musculo esquelético a la lipogénesis hepática de novo, produciendo aumento de los triglicéridos plasmáticos y disminución de las lipoproteínas de alta densidad.
Además, este patrón anormal de almacenamiento energético fue suprimido por completo tras un único episodio de ejercicio de intensidad moderada con la elíptica, que favoreció la síntesis de glucógeno muscular tras el consumo de hidratos de carbono, mediante el aumento de la actividad de transporte de la glucosa. Estos datos muestran que la resistencia a la insulina en el músculo es un objetivo inicial para el tratamiento y la prevención de la dislipidemia aterógena y del hígado graso no alcohólico en personas jóvenes con resistencia a la insulina, que son propensas al síndrome metabólico y la diabetes tipo 2.
Lipólisis inducida por los macrófagos, inflamación e hiperglucemia en ayunas
Aunque la resistencia a la insulina inducida por lípidos aparece precozmente en la patogenia de la diabetes tipo 2, es esencial identificar los factores que promueven la progresión de la resistencia a la insulina asociada con la acumulación de lípidos ectópicos a la intolerancia a la glucosa y la hiperglucemia en ayunas.
El punto de vista tradicional atribuye la alteración de la función las células pancreáticas beta y alfa, junto con la inflamación, a esta transición, en la que defectos de las células beta y alfa llevan al aumento de la transcripción de genes gluconeogénicos hepáticos y la inflamación inhibe la acción de la insulina a través de la liberación de citocinas y adipocitocinas.
El aumento de las citocinas a su vez causa inhibición de las señales de insulina y aumento de la transcripción de la proteína gluconeogénica hepática a través de la activación del factor nuclear kβ, la cinasa Jun N-terminal y las vías biosíntéticas de la ceramida.
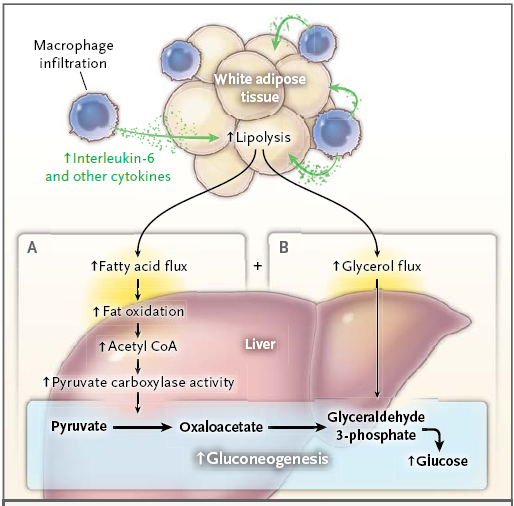
Otra hipótesis que vincula la inflamación con la progresión a la hiperglucemia en ayunas es el posible efecto de la lipólisis inducida por macrófagos sobre la regulación de la gluconeogénesis hepática. Estudios en ratones avalan esta hipótesis. Aunque especulativa, esta hipótesis propone que la lipólisis inducida por macrófagos, al contrario de las alteraciones en las citocinas circulantes y la transcripción de la proteína gluconeogénica hepática, es el principal culpable de la transición de la resistencia a la insulina a la intolerancia a la glucosa y la diabetes tipo 2. Esta hipótesis también coincide con un estudio que mostró la ausencia de relación entre la expresión de la proteína gluconeogénica
hepática y la hiperglucemia en ayuna en personas obesas.
Posibles tratamientos para la acumulación ectópica de lípidos y la resistencia a la insulina
La resistencia a la insulina inducida por lípidos ectópicos representa un exceso de energía intracelular en forma de DAG, que genera la activación de PKCθ en el músculo y de PKCε en el hígado y la ulterior inhibición de las señales de insulina en estos tejidos. Esta hipótesis puede explicar la resistencia a la insulina asociada con la obesidad, el envejecimiento, la lipodistrofia, la prediabetes y la diabetes tipo 2 y la neutralización de la resistencia a la insulina y de la diabetes tras el descenso de peso y el tratamiento con tiazolidinediona.
Teleológicamente, la resistencia a la insulina en el músculo y el hígado inducida por DAG y nPKCs puede representar un mecanismo celular autónomo para detener el depósito de energía en el hígado y el músculo ante el exceso de lípidos intracelulares y encauzar ese exceso de energía al tejido adiposo para su almacenamiento.
Aunque la reducción del contenido de lípidos ectópicos y de la resistencia a la insulina mediante intervenciones para el descenso de peso (idealmente junto con ejercicio) es el tratamiento preferido para estos trastornos, la recidiva tras el adelgazamiento es muy frecuente. La cirugía bariátrica es más exitosa para lograr el descenso de peso a largo plazo, pero es un procedimiento invasivo, caro y con ciertos riesgos. Por consiguiente, se necesita un fármaco que disminuya la grasa ectópica del hígado y la resistencia a la insulina.
El factor de crecimiento fibroblástico 21 es eficaz para reducir la actividad hepática de DAG–PKCε, así como la resistencia hepática a la insulina en animales y actualmente se lo está investigando en ensayos clínicos.
Otro enfoque para disminuir el contenido de lípidos ectópicos es la aplicación de protonoforo mitocondrial dirigido al hígado para favorecer aumentos sutiles del desacoplamiento mitocondrial hepático.
Este enfoque neutraliza la hipertrigliceridemia, la esteatosis hepática, la resistencia a la insulina y la hiperglucemia en modelos murinos de hígado graso no alcohólico y diabetes tipo 2. Además de disminuir los triglicéridos y el DAG hepático, la actividad de PKCε y la resistencia hepática a la insulina, este enfoque reduce el contenido hepático de acetil CoA, disminuye la gluconeogénesis hepática y la hiperglucemia en ayunas y posprandial. Además, al disminuir la oxidación de la grasa hepática en un 60%, disminuye la producción hepática de lipoproteína de muy baja densidad y produce así menor pasaje de triglicéridos al músculo y protege contra la resistencia a la insulina en el músculo inducida por lípidos.
En resumen, estos estudios muestran la importancia de la acumulación ectópica de lípido en la patogenia de la resistencia a la insulina en el músculo y el hígado. Este modelo también explica la mejor acción de la insulina con el ejercicio, el adelgazamiento y las tiazolidinedionas. Asimismo, aumentar el gasto hepático de energía al favorecer el desacoplamiento mitocondrial podría ser un enfoque novedoso para tratar la epidemia de hígado graso no alcohólico, el síndrome metabólico y la diabetes tipo 2.
*Traducción y resumen objetivo Dr. Ricardo Ferreira