| 1. Introducción |
La hipocalcemia es un problema metabólico común en el período neonatal y la infancia. Existe consenso sobre el tratamiento de los casos sintomáticos, mientras que el nivel de calcio con el que se iniciará el tratamiento y las opciones de tratamiento aún son controvertidos en la hipocalcemia asintomática.
Este artículo de revisión cubrirá la hipocalcemia con un énfasis específico en la definición y la homeostasis del calcio, la etiología, el diagnóstico y el tratamiento de la hipocalcemia en el período neonatal y la infancia.
| 2. Rol del calcio en los humanos |
El calcio está involucrado en muchos procesos bioquímicos corporales, como coagulación sanguínea, transducción de señales intracelulares, transmisión neural, funciones musculares, integridad celular y función de membrana, actividades enzimáticas celulares, diferenciación celular y mineralización ósea [1, 2].
Cerca del 99% del calcio corporal reside en el tejido óseo y el restante está presente en el líquido extracelular [3]. Casi la mitad del calcio que se encuentra en el líquido extracelular está en forma ionizada activa, mientras que el 10% está formando complejos con aniones tales como fosfato, citrato, sulfato y lactato, y el 40% está unido a albúmina [4, 5].
| 3. Factores que afectan el nivel de calcio sérico |
El nivel sérico de calcio se ve afectado por los niveles séricos de fosfato, magnesio, albúmina y bicarbonato. El cambio en la concentración de albúmina no cambia el nivel de calcio ionizado en sangre pero cambia la medición del nivel de calcio total.
En general, la concentración plasmática de calcio se reduce en 0,8mg/dl por cada reducción de 1,0g/dl del nivel de albúmina en plasma [6]. Cuando el calcio ionizado, la forma activa, no es medido directamente, se debe calcular el calcio corregido para el calcio total medido y la albúmina medida. Además, el pH de la sangre afecta el nivel de calcio ionizado.
La alcalosis aumenta la cantidad de albúmina unida al calcio y disminuye el nivel de calcio ionizado, lo que lleva a síntomas de hipocalcemia [7]. En alcalosis respiratoria aguda, el nivel de calcio ionizado cae 0,16mg/dl por cada 0,1 unidad de aumento del pH [7].
Por el contrario, en la acidosis metabólica, la unión calcio-albúmina se reduce y aumenta el nivel de calcio ionizado. El magnesio también participa en la regulación de la liberación intracelular de hormona paratiroidea. El nivel bajo de magnesio puede reducir la actividad de la hormona paratiroidea o causar resistencia a la hormona paratiroidea (PTH), y a largo plazo la deficiencia de magnesio inhibe la liberación de PTH [8].
La homeostasis del calcio es mantenida por hormonas, como PTH, calcitonina, vitamina D y receptores sensibles al calcio. La PTH aumenta la resorción ósea y, en consecuencia, el nivel de calcio en suero.
En los riñones, la PTH aumenta la actividad de 1-α-hidroxilasa en los túbulos proximales, aumentando la producción de la forma activa 1,25-dihidroxivitamina D de la 25-hidroxivitamina D. Además, la PTH aumenta la excreción de fosfato, y la reabsorción de calcio y magnesio en los túbulos distales.
La forma activa de la vitamina D actúa sobre huesos, intestino y glándulas paratiroides. Aumenta la mineralización osteoide en los huesos y provoca resorción a altas dosis. La 1,25-dihidroxivitamina D también aumenta la absorción intestinal de iones de calcio y fosfato y disminuye la excreción renal de estos iones.
La vitamina D inhibe la secreción de PTH por las glándulas paratiroides. La calcitonina principalmente reduce la resorción ósea, promueve la deposición de calcio en el hueso por mineralización y, en consecuencia, disminuye el nivel de calcio en suero.
La calcitonina también aumenta la excreción renal de iones de calcio y fosfato y disminuye la absorción gastrointestinal de estos iones [9].
| 4. Homeostasis fetal y neonatal del calcio |
El calcio se transfiere de la circulación materna a la circulación fetal por transporte activo desde la placenta en el último trimestre. Por lo tanto, la concentración de calcio es mayor en sangre de cordón umbilical que en sangre materna al momento del parto.
En el embarazo a término, las concentraciones totales de calcio fetal e ionizado son de 10–11mg/dl (2,5–2,75 mmol/l) y 6 mg/dl (1,5 mmol/l), respectivamente, en sangre de cordón umbilical [10]. La PTH y la calcitonina no pueden atravesar la barrera placentaria. El péptido relacionado con hormona paratiroidea es el principal regulador del balance positivo de calcio en la placenta [11].
El nivel sérico de calcio posparto en recién nacidos está asociado con varios factores como la secreción de PTH, la ingesta dietética de calcio, la reabsorción renal de calcio, las reservas esqueléticas de calcio y el estado de la vitamina D.
Después de que el neonato es separado de la placenta, los niveles de calcio sérico total y ionizado disminuyen, alcanzando un nadir fisiológico en un lactante sano de término de 2 días. Por el contrario, los niveles de fosfato aumentan.
El ritmo y la cantidad de tal disminución en los niveles de calcio están inversamente relacionados con la semana gestacional [12]. Tal disminución del nivel de calcio se asocia con hipoparatiroidismo, falta de respuesta de órganos diana a la PTH, trastornos del metabolismo de la vitamina D, hiperfosfatemia, hipomagnesemia e hipercalcitonemia en los primeros días de vida [12].
La secreción de PTH aumenta en las primeras 48 hs de vida y con el aumento de la secreción de PTH, la absorción intestinal de calcio y fosfato, la reabsorción renal de calcio y la excreción renal de fosfato aumentan en el recién nacido.
Del mismo modo, los niveles de calcio en suero comienzan a aumentar y los niveles de fosfato en suero a disminuir. Dentro de las primeras cuatro semanas de nacimiento, la absorción intestinal y la reabsorción renal de calcio maduran [13].
| 5. Definición de hipocalcemia |
La hipocalcemia se define como calcio sérico total < 8 mg/dl (2 mmol/l) o calcio ionizado < 4,4 mg/dl (1,1 mmol/l) para recién nacidos a término o prematuros que pesen > 1500 g al nacer, y calcio sérico total < 7 mg/dl (1,75 mmol/l) o calcio ionizado < 4 mg/dl (1 mmol/l) para lactantes con muy bajo peso al nacer con un peso <1500 g [14].
Los principales síntomas clínicos de hipocalcemia incluyen apnea, cianosis, mala alimentación, vómitos, taquicardia, insuficiencia cardíaca, intervalo QT prolongado, irritabilidad, temblor, laringoespasmo, tetania, hiperacusia, episodios de sacudidas y espasmos, y convulsiones focales y generalizadas [15]. La hipocalcemia neonatal de inicio temprano es principalmente asintomática.
| 6. Etiología de la hipocalcemia en el periodo neonatal y la infancia |
Según el momento de inicio, la hipocalcemia se define como de inicio temprano o tardío.
> 6.1. Hipocalcemia de inicio temprano. Generalmente se presenta dentro de las primeras 72 hs de vida. Se produce por un incremento de la reducción del nivel de calcio sérico que ocurre fisiológicamente dentro de los primeros tres días en recién nacidos, y la secreción retrasada de PTH en respuesta a la hipocalcemia [13].
La hipocalcemia neonatal de inicio temprano es más común en prematuros, lactantes con retraso del crecimiento intrauterino, lactantes con asfixia perinatal y lactantes hijos de madres diabéticas.
Aproximadamente un tercio de los recién nacidos prematuros y la mayoría de los bebés de muy bajo peso al nacer tienen un bajo nivel de calcio sérico durante las primeras 48 h de vida [12].
Las causas de hipocalcemia en bebés prematuros incluyen la interrupción temprana de la transferencia de calcio a través de la placenta, una exagerada disminución en el nivel de calcio sérico que ocurre fisiológicamente después del parto, la respuesta reducida de los órganos diana a la PTH y el aumento de los niveles de calcitonina [16].
Las causas principales de hipocalcemia en lactantes con asfixia incluyen aumento de la carga de fosfato debido al daño celular, aumento de la producción de calcitonina, insuficiencia renal y disminución de la secreción de PTH [16, 17].
La principal causa de hipocalcemia en los lactantes de madres diabéticas es la hipomagnesemia en la madre y el lactante debido al aumento de la excreción urinaria materna de magnesio durante el embarazo. La hipomagnesemia causa hipoparatiroidismo funcional en el lactante [18].
El exceso de calcio materno debido al hiperparatiroidismo pasa al lactante a través de la placenta suprimiendo la síntesis fetal de PTH y afectando la respuesta de la PTH a la hipocalcemia posparto.
La supresión de la PTH, en este caso, puede ser grave y conducir a convulsiones en el período neonatal temprano, pudiendo persistir durante meses [19]. Las madres pueden ser asintomáticas para hipercalcemia.
Por lo tanto, en el curso de la hipocalcemia neonatal de inicio temprano, deben medirse los niveles séricos maternos de calcio y PTH para la evaluación etiológica. La Tabla 1 presenta las causas de hipocalcemia neonatal de inicio temprano.
> 6.2. ¿Quién debe ser examinado para detectar hipocalcemia?
Ya que la mayoría de los lactantes con hipocalcemia de inicio temprano generalmente son asintomáticos, se debe medir el calcio sérico, preferiblemente el ionizado, en lactantes con factores de riesgo para hipocalcemia.
Los lactantes prematuros con una edad gestacional < 32 semanas, los lactantes hijos de madres diabéticas y los lactantes con asfixia prenatal severa y un puntaje de Apgar al minuto de < 4 y que están en riesgo de hipocalcemia deben examinarse a las 24 y 48 hs después del nacimiento [20]. Para los lactantes con un peso al nacer extremadamente bajo (peso al nacer <1000 g), los niveles de calcio deben medirse a las 12, 24 y 48 hs de nacimiento.
Para prematuros con un peso al nacer de 1000–1500 g, el nivel de calcio se mide a las 24 y 48 hs de nacimiento. El monitoreo de los niveles de calcio debe continuar hasta que los valores vuelvan a la normalidad y la ingesta de calcio sea adecuada.
> 6.3. Hipocalcemia de inicio tardío. La hipocalcemia de inicio tardío, que generalmente es sintomática, ocurre después de las primeras 72 hs y generalmente al final de la primera semana de nacimiento. Las causas más comunes de hipocalcemia de inicio tardío incluyen ingesta excesiva de fosfato, hipomagnesemia, hipoparatiroidismo, y deficiencia de vitamina D [21-23].
La alimentación con leche de vaca puede causar hiperfosfatemia, que conduce a hipocalcemia [24]. La hipomagnesemia puede causar alteración de la secreción de PTH y una respuesta periférica reducida a la PTH, lo que lleva a hipocalcemia [25]. Las causas de deficiencia neonatal de vitamina D incluyen deficiencia materna de vitamina D, malabsorción, insuficiencia renal y enfermedades hepatobiliares de lactantes.
En la deficiencia de vitamina D, la hipocalcemia suele acompañarse de hipofosfatemia. Si la hipocalcemia se acompaña de hiperfosfatemia, entonces el hipoparatiroidismo debe ser considerado como la causa más común. El hipoparatiroidismo puede ser primario o secundario.
El hipoparatiroidismo primario puede ser aislado o asociarse con síndromes como el síndrome de Di George [26]. Además, mutaciones activadoras de los receptores sensibles al calcio pueden causar hipoparatiroidismo primario con herencia autosómica dominante [27].
En dichas mutaciones, las funciones del canal de potasio en los riñones son inhibidas, lo que lleva a un síndrome tipo Bartter, alcalosis metabólica hipokalémica, hiperreninemia, hiperaldosteronismo, e hipocalcemia hipercalciúrica [28].
Las condiciones más comunes de hipoparatiroidismo primario sindrómico incluyen el síndrome de Di George que se caracteriza por hipoplasia de las glándulas paratiroides, hipoplasia tímica, cardiopatías congénitas y anomalías faciales, y el síndrome CATCH 22 con anomalía cardíaca, anomalía facial, cara de llanto asimétrica, hipoplasia tímica, paladar hendido, hipotiroidismo y delección en el cromosoma 22 [29].
La resistencia a la PTH del pseudohipoparatiroidismo puede ser transitoria como en el caso de la displasia renal o la uropatía obstructiva o permanente debido a mutaciones GNAS.
El peudohipoparatiroidismo tipo 1a (osteodistrofia hereditaria de Albright) debido a mutaciones GNAS incluye resistencia hormonal generalizada (PTH, TSH, FSH y LH), baja estatura y varias anomalías esqueléticas [30]. Sin embargo, los síntomas esqueléticos que son típicos de los períodos posteriores no se observan generalmente en el período neonatal.
El pseudohipoparatiroidismo tipo 1b no incluye síntomas esqueléticos pero si resistencia a la PTH y la TSH; y aunque el AMPc urinario aumenta después de la administración de PTH no ocurre fosfaturia [31]. Las causas de hipocalcemia de inicio tardío se resumen en la tabla 1.
| 7. Enfoque de la hipocalcemia en el período neonatal y la infancia |
Debe obtenerse una historia detallada que incluya los antecedentes del embarazo y familiares en casos de hipocalcemia en el período neonatal y la infancia. La historia del embarazo debe ser cuestionada, especialmente en casos de diabetes gestacional, toxemia del embarazo y deficiencia materna de vitamina D.
Además, el interrogatorio debe incluir condiciones que pueden estar asociadas con hipocalcemia de inicio temprano como prematuridad, bajo peso al nacer, asfixia, sepsis neonatal, historial de uso de medicamentos para la madre y el bebé, estado de alimentación con fórmula, carga de fosfato de la fórmula (si se utiliza), antecedentes de transfusión de sangre y presencia de hiperparatiroidismo materno.
Deben obtenerse los antecedentes familiares para enfermedades genéticas que causan hipocalcemia en neonatos y niños pequeños.
El examen físico debe hacerse después de considerar la presencia de anomalías faciales, hendidura de paladar y cara de llanto asimétrica en términos de hipocalcemia sindrómica. En los análisis de sangre deben medirse los niveles de calcio ionizado, fosfato, fosfatasa alcalina, magnesio, albúmina y calcio total en suero.
La medición del calcio ionizado proporciona información sobre la forma activa del calcio.
La unión albúmina-calcio aumenta y el nivel de calcio ionizado disminuye en la alcalosis metabólica o respiratoria. La baja albúmina sugiere pseudohipocalcemia; y la medición de calcio debe corregirse en base a los niveles de albúmina. Los niveles de PTH, 25-hidroxivitamina D y, si es necesario, 1,25-dihidroxivitamina D, calcio urinario y creatinina deben ser medidos.
Para los recién nacidos con hipercalciuria a pesar de la hipocalcemia, debe considerarse la hipocalcemia hipercalciúrica familiar (mutación activadora de receptores sensibles al calcio). En caso de hipocalciuria, la medición de fosfato sérico y PTH podría ser diagnóstica. Una PTH baja o inapropiadamente normal a pesar de la hipocalcemia puede sugerir hipoparatiroidismo primario o hipomagnesemia. El hipoparatiroidismo puede ser transitorio, asociado con hiperparatiroidismo materno, o permanente.
En el hipoparatiroidismo, el nivel de calcio en suero disminuye, mientras que el nivel de fosfato sérico aumenta. Si el nivel de PTH se eleva en respuesta a la hipocalcemia, se considera que las glándulas paratiroides funcionan normalmente, y los niveles de fosfato en suero deben ser evaluados para diagnósticos diferenciales.
Si el nivel de fosfato en suero es bajo, entonces deben considerarse las enfermedades del metabolismo de la vitamina D. En dichas enfermedades, la hipofosfatemia acompaña a la hipocalcemia y a los niveles elevados de fosfatasa alcalina. El nivel de PTH se eleva en respuesta a la hipocalcemia y la absorción de calcio y fosfato está alterada. En tales casos, la deficiencia nutricional de vitamina D o la malabsorción de vitamina D o un trastorno genético del metabolismo de la vitamina D pueden ser la causa subyacente.
En casos con niveles elevados de fosfato sérico y aumento de los niveles de PTH en respuesta a la hipocalcemia, debe considerarse la excesiva ingesta exógena de fosfato, la insuficiencia renal y el pseudohipoparatiroidismo (resistencia a la PTH).
En tales casos, debe medirse la creatinina sérica y el nitrógeno urinario para evaluar la insuficiencia renal. Los síntomas esqueléticos típicos no están presentes en casos de pseudohipoparatiroidismo neonatal y se requiere el análisis de GNAS para el diagnóstico en tales casos.
La hipomagnesemia es otra causa de hipocalcemia y puede deberse a pérdida renal de magnesio debido a diuresis osmótica, tubulopatía o uso de diuréticos o pérdida de magnesio gastrointestinal, incluso aunque esto sea raro (diarrea crónica, malabsorción). El nivel de magnesio en suero debe medirse especialmente en casos sin respuesta al tratamiento de la hipocalcemia.
Otras causas de hipomagnesemia son deficiencia materna de magnesio, diabetes materna, retraso del crecimiento intrauterino, trastornos intestinales del transporte de magnesio, pérdida renal aislada de magnesio infantil, nefrocalcinosis e hipercalciuria [32, 33]. Existe un estado de hipoparatiroidismo funcional en la hipomagnesemia.
De realizarse un electrocardiograma (ECG) para establecer el efecto de la hipocalcemia severa en los tejidos y el corazón. En casos de hipocalcemia, el ECG puede revelar un intervalo QT prolongado, cambios en el QRS y el ST y arritmia ventricular [34]. La radiografía de rodilla puede ayudar a diagnosticar raquitismo en la infancia.
La radiografía de tórax se puede usar para evaluar la presencia de una sombra tímica en casos sospechosos de Síndrome de Di George. Además, pueden utilizarse métodos inmunológicos para determinar la función de las células T en el síndrome de Di George.
En tales casos, se detecta un recuento reducido de linfocitos CD4 además de la apariencia facial dismórfica, y puede usarse análisis de hibridación in situ fluorescente (FISH) para mostrar microdelección en el cromosoma 22q11.2 [35]. El enfoque diagnóstico de la hipocalcemia en el período neonatal y la infancia se resume mediante un algoritmo en la Figura 1.
| 8. Tratamiento de la hipocalcemia en el periodo neonatal y la infancia |
La piedra angular del tratamiento de la hipocalcemia es el reemplazo del calcio y las opciones de tratamiento pueden variar según los síntomas y el grado de hipocalcemia.
La hipocalcemia de inicio temprano suele ser asintomática y se recomienda tratamiento cuando el nivel de calcio en suero es < 6mg/dl en prematuros y de 7mg/dl en lactantes de término [35].
Se recomienda administrar 40 a 80 mg/kg/día de calcio elemental de reemplazo en recién nacidos asintomáticos [20]. Para lactantes que requieren nutrición parenteral, se puede agregar calcio como gluconato de calcio al 10% (500 mg/kg/d, 50 mg/kg/d de calcio elemental) en infusión continua.
Si se administra calcio parenteral durante > 2 días, el fósforo también debe ser reemplazado en base a los niveles de fosfato en suero. En recién nacidos con síntomas como tetania o convulsiones, se administra 10 a 20 mg/kg de calcio elemental IV (1–2 ml/kg/dosis de gluconato de calcio al 10%) en infusión lenta durante aproximadamente 10 minutos bajo monitorización cardíaca para el tratamiento de la hipocalcemia aguda. Este tratamiento no normaliza el nivel de calcio pero previene los síntomas graves de la hipocalcemia, como la convulsión.
Después de la administración del bolo de calcio, debe iniciarse la infusión de 50 a 75 mg/kg/d o 1 a 3 mg/kg/h de calcio elemental [13]. Se prefiere la infusión continua de gluconato de calcio a la administración de bolos intravenosos de calcio a 1 ml/kg/dosis cada 6 hs.
La cantidad de calcio se debe ajustar midiendo el calcio cada 8 a 12 hs hasta alcanzar los valores normales de calcio. Puede ocurrir necrosis tisular severa debido a la extravasación de calcio en la terapia intravenosa con gluconato de calcio.
Por lo tanto, se debe garantizar un acceso vascular apropiado y la velocidad de infusión no debe exceder 1 mg/min. Pueden ocurrir arritmias cardíacas como bradicardia e incluso puede desarrollarse un paro cardíaco durante la infusión del gluconato de calcio; por lo tanto, la administración intravenosa debe realizarse lentamente durante 10 a 30 minutos bajo monitorización cardíaca.
Si se utiliza un catéter venoso umbilical para la administración de calcio, entonces la punta del catéter debe estar en la vena cava inferior; una punta de catéter en la vena porta puede causar necrosis hepática.
En pacientes asintomáticos o con síntomas leves o que han alcanzado la normocalcemia mediante el calcio intravenoso, se puede administrar terapia de calcio oral. En dichos pacientes, puede utilizarse lactato, carbonato o citrato de calcio y se puede administrar de 40 a 80 mg/kg/día de calcio elemental en 3 a 4 dosis.
Después de que el nivel de calcio vuelve a la normalidad, deben evaluarse los niveles séricos y urinarios de calcio y creatinina a intervalos frecuentes y la dosis debe ajustarse para que la excreción urinaria diaria de calcio sea < 4mg/kg/d. Las complicaciones como la hipercalcemia iatrogénica, la nefrocalcinosis, y la insuficiencia renal puede ser evitadas.
En pacientes con deficiencia de vitamina D, se recomienda el reemplazo con 1000 a 2000 UI/día de vitamina D. Dado que la producción de la vitamina D activa está alterada en los trastornos del metabolismo de la vitamina D o en el hipoparatiroidismo, deben administrarse preparaciones activas de vitamina D (20–60 ng/kg/d de calcitriol).
El tratamiento del hipoparatiroidismo debe tratar de mantener el nivel de calcio sérico en el límite inferior de lo normal para evitar la hipercalciuria y la nefrocalcinosis. Por el contrario, el objetivo del tratamiento en el pseudohipoparatiroidismo es normalizar los niveles de PTH manteniendo el nivel de calcio sérico cerca del límite superior de lo normal.
No se puede lograr respuesta en el tratamiento de la hipocalcemia sin tratar primero la hipomagnesemia.
Debe administrarse sulfato de magnesio (25–50mg/kg o 0,2–0,4 mEq/l por dosis cada 12 hs, por vía intravenosa durante más de 2 hs o intramuscular) hasta que la concentración sérica de magnesio se eleve por encima de 1,5 mg/dl (0,62 mmol/l).
La infusión intravenosa rápida de magnesio debe evitarse debido al riesgo de arritmias. En lactantes con carga excesiva de fosfato, el objetivo del tratamiento es reducir el nivel de fosfato sérico.
Por lo tanto, se debe evitar la alimentación con alto contenido de fosfato y los bebés deben ser alimentados con dieta alta en calcio y baja en fosfato, ya sea con leche materna o con fórmula con bajo contenido de fosfato. Las sales de calcio también pueden ser útiles para disminuir el nivel de fosfato en suero.
| 9. Conclusión |
La hipocalcemia es un problema metabólico común en los recién nacidos. Dado que la mayoría de los lactantes con hipocalcemia son generalmente asintomáticos, los niveles de calcio sérico total o ionizado deben ser monitoreados en prematuros con una edad gestacional < 32 semanas, en neonatos pequeños para la edad gestacional, en los hijos de madres diabéticas y en bebés con asfixia prenatal severa.
El tratamiento de la hipocalcemia debe iniciarse de inmediato en lactantes con niveles reducidos de calcio mientras se investiga la etiología.
Tabla 1. Causas de hipocalcemia de inicio temprano y tardío en el período neonatal y la infancia
|
Hipocalcemia de inicio temprano |
Hipocalcemia de inicio tardío |
|
|
* Modificado de Root AW, Diamond FB. (2008) Disorders of Mineral Homeostasis in the Newborn, Infant, Child, and Adolescent. In: Sperling MA, editor. Pediatric Endocrinology, 3rd ed. Philadelphia: Saunders/Elsevier. p. 686-769; from Carpenter TO. (2006) Neonatal hypocalcemia. In: Favus MJ, editor. Primer on the Metabolic Disease and Disorders of Mineral Metabolism, 6th ed. Washington, D.C. American Society for Bone and Mineral Research. p. 224-227.
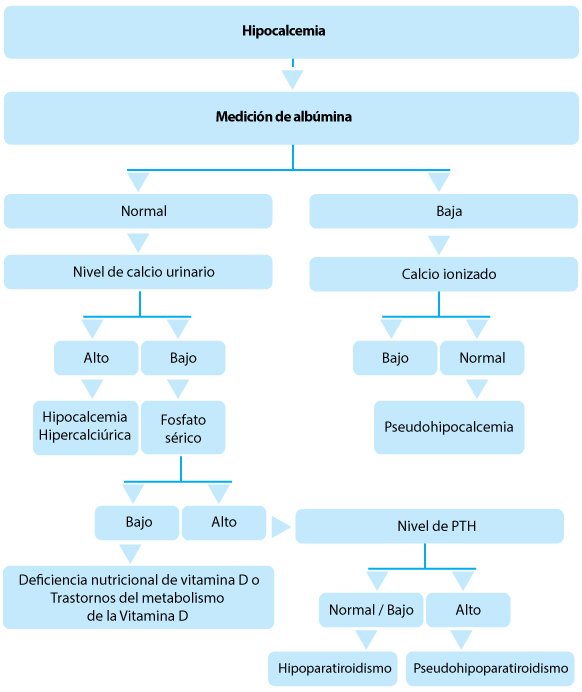
Figura 1: Enfoque diagnóstico de la hipocalcemia en el período neonatal y la infancia. *Modificado de Root AW, Diamond FB. (2008) Disorders of Mineral Homeostasis in the Newborn, Infant, Child, and Adolescent. In: Sperling MA, editor. Pediatric Endocrinology, 3rd ed. Philadelphia: Saunders/Elsevier. p. 686-769.
| Comentario |
La hipocalcemia es un problema metabólico común en el período neonatal y la infancia, y puede ser de inicio temprano o tardío. Si bien la mayoría de los casos son asintomáticos, la etiología y los factores predisponentes marcarán la posible presencia de signos y síntomas asociados.
Para su diagnóstico será útil obtener una historia clínica detallada que incluya los antecedentes del embarazo, familiares, de enfermedades genéticas y de condiciones que pueden asociarse con hipocalcemia de inicio temprano.
El examen físico deberá considerar la presencia de anomalías morfológicas como parte de cuadros sindrómicos, y se deberá acompañar de un laboratorio para medir los niveles de calcio ionizado, fosfato, fosfatasa alcalina, magnesio, albúmina y calcio total en suero, además de otros estudios (hormonales, moleculares, etc.) que se consideren pertinentes según la sospecha clínica.
El tratamiento de la hipocalcemia deberá iniciarse de inmediato en lactantes con niveles reducidos de calcio o sintomáticos mientras se investiga la probable etiología y se abordan los distintos síntomas.
Resumen y comentario objetivo: Dra. María Eugenia Noguerol