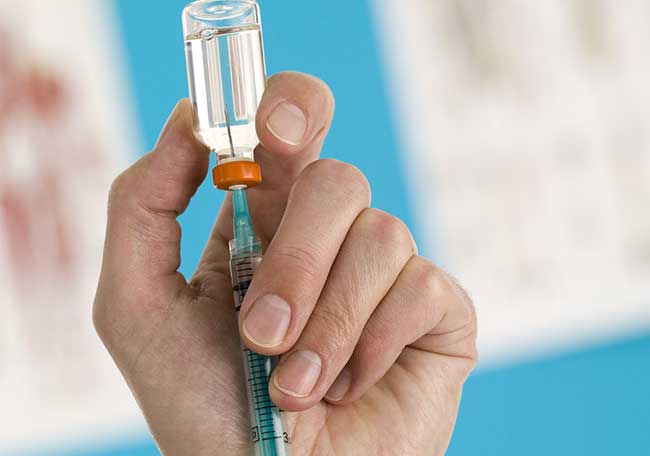
Inyección intravítreo de ranibizumab e implante intravítreo de dexametasona

► Introducción
El edema macular secundario a oclusión de vena retiniana es común y puede causar pérdida de visión significativa. La patogénesis es multifactorial, pero las venas retinianas normalmente se obstruyen debido a un coagulo, compresión vascular externa o patología de la pared vascular. La obstrucción puede producirse en la vena retiniana central o en las ramas y se conoce como oclusión de vena retiniana central o de rama, respectivamente, siendo esta última más común.
La oclusión de vena retiniana provoca aumento de la presión capilar, lo que induce expresión de factor de crecimiento endotelial vascular (FCEV) e interleukina 6. Esto deriva en el colapso de la barrera hemato retiniana y aumenta la permeabilidad vascular, causando complicaciones como edema macular e isquemia retiniana provocando pérdida de visión.
Hasta hace poco, el tratamiento para el edema macular consistía en corticosteroides y fotocoagulación láser, sin embargo, actualmente los agentes anti FCEV proporcionan una opción tanto para la oclusión de vena retiniana central como de rama.
La eficacia y seguridad de ranibizumab intravítreo ha sido evaluada en dos importantes ensayos clínicos: BRAVO y CRUISE, en ambos estudios un mayor porcentaje los pacientes tratados con ranibizumab lograron una mejoría de la visión que los controles. La mejoría se mantuvo durante 12 meses. Hubo una menor frecuencia de efectos adversos también. Posteriormente la FDA aprobó el tratamiento con ranibizumab para edema macular secundario a oclusión de vena retiniana en 2010, al igual que la Agencia de Medicación Europea en 2011.
La dexametasona, es un corticosteroide que también resulta eficaz en el tratamiento de la misma patología. La dexametasona es administrada directamente a la cavidad del vítreo por un implante intravítreo. Si bien el porcentaje de pacientes que mejoraron fue superior a los controles, hubo un mayor porcentaje de efectos adversos.
El tratamiento fue aprobado para tratar edema macular asociado con oclusión de vena retiniana por la FDA en 2009. La repetición del tratamiento para la mayoría de los pacientes con edema macular secundario a OVR es <6 meses luego del primer tratamiento.
Debido a los distintos regímenes de tratamiento y dosificación, el principal objetivo del presente estudio fue comparar el promedio de consultas oftalmológicas de los pacientes tratados con ranibizumab intravítreo o dexametasona con implante intravítreo para el tratamiento de oclusión de vena retiniana central o de rama a los 12 meses de realizado el tratamiento.
► Pacientes y métodos:
Se utilizó la base de datos IMS Health Rel-World Data Medical Claims, para identificar pacientes que recibieron ranibizumab intravítreo o implante intravítreo de dexametasona entre junio 2010 y febrero 2014, con seguimiento de 12 meses.
Comentarios
Para ver los comentarios de sus colegas o para expresar su opinión debe ingresar con su cuenta de IntraMed.