El consumo de cocaína se ha relacionado con una amplia variedad de condiciones clínicas incluyendo lesiones destructivas de la línea media (CIMDL), vasculitis cutánea inducida por cocaína contaminada con levamisol, y pioderma gangrenoso eruptivo (PG). Algunas patologías han sido relacionadas con la presencia de anticuerpos citoplasmáticos antineutrofílicos peri-nucleares (p ANCA) con especificidad contra la elastasa neutrófila humana (HNE). Se describe un caso de autoinmunidad ocasionado por cocaína, con compromiso cutáneo, pulmonar, oreja, naríz y garganta. La clave principal para el diagnóstico etiológico fue la detección de HNE-positiva p ANCA.
Reporte:
Se presenta una mujer de 54 años con antecedentes de úlceras múltiples dolorosas en ambas piernas de 2 meses de evolución. Durante este período, había sido tratada con antibióticos tópicos y orales sin mejoría. El estado de salud era bueno, pero presentaba episodios ocasionales de tos seca y esputo con sangre. Había consumido cocaína por inhalación (aproximadamente 3.5 g /semana) por 5 años.
Al exámen físico, se observaban múltiples úlceras dolorosas en las piernas del paciente. Eran purpúricas, con una morfología cribiforme con bordes ligeramente elevados, y variaban de 10 a 50 mm de tamaño (Fig 1 a).
Cada úlcera primero se manifestaba como una pústula, que luego se transformaba en úlcera en 3 días (Fig 1 b). La paciente presentaba deformidad en nariz en silla de montar, asociada con fístula oronasal en paladar (Fig 1 c), ocasionada por abuso de cocaína.
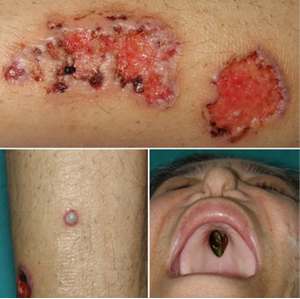
Figura 1. Imagenes clínicas. (a) Ulceras con borde violeta dolorosas en las piernas; (b) pústulas con halo violeta en la pierna; (c) deformidad en silla de montar con fístula oronasal.
Al examen histológico de la biopsia de un borde de la úlcera se observó un infiltrado inflamatorio denso en dermis, con neutrófilos y depósitos de fibrina en los vasos (Fig 2). No presentaba granulomas ni vasculitis. La inmunofluorescencia directa fue negativa, como así también cultivos de bacterias, hongos y ácido alcohol resistente.
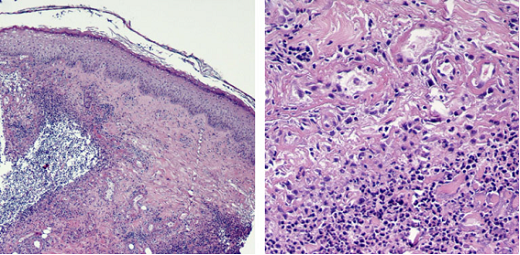
Figura 2 (a) Ulceración e infiltrado inflamatorio denso y profundo; (b) neutrófilos en el infiltrado inflamatorio asociado a depósitos de fibrina en los vasos
Basado en los hallazgos clínicos e histológicos, se diagnosticó PG, y se realizaron otras investigaciones. La radiografía de tórax mostró infiltrados pulmonares en lóbulos de pulmón derecho, acompañado de un patrón pulmonar intersticial (Fig 3 a). La tomografía computada (CT) de tórax identificó nódulos pulmonares bilaterales y cavitación (Fig 3 b), y una CT facial mostró destrucción de la línea media con una fístula oronasal (Fig 3 c).
El hemograma completo, los test de coagulación y bioquímicos fueron negativos o dentro de límites normales: anti-Sm, anti-RNP, anti-Ro, anti-La, anti-Scl 70, anticentrómero, anti-b2-glicoproteína, anticardiolipina y anticuerpos antihistonas, anti ADN doble cadena, crioglobulinas, niveles de complemento, factor reumatoideo, y test de sedimento urinario.
Las investigaciones para sífilis, hepatitis B y C, virus de inmunodeficiencia humana y tuberculosis (TB) fueron negativos.
Los niveles circulantes de pANCA sin especificidad para mieloperoxidasa (MPO) o proteinasa (PR)3 fue de 1:80 (Fig 3 d).
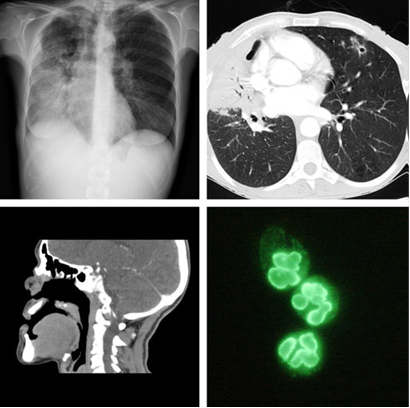
Figura 3 (a) Radiografía que muestra la presencia de infiltrados pulmonares en lóbulos medio y derecho de pulmón derecho (b,c) Tomografía computada (b) infiltrados pulmonares en pulmón derecho y un nódulo cavitado en pulmón izquierdo y (c) destrucción extensa del tracto respiratorio superior asociado a fístula oronasal. (d) Inmunofluorescencia muestra un patrón perinuclear de anticuerpos antinucleares citoplasmáticos a la elastasa.
Debido a que la paciente presentaba antecedentes de abuso de cocaína, se investigó para ANCAs atípico que fueran positivos para elastasa. La paciente presentó positivos los anticuerpos antinucleares 1:40.
Debido a los hallazgos pulmonares se realizó una fibrobroncoscopía que no indicó malignidad, y se estudió para bacterias, hongos y bacilos ácido alcohol resistentes. La histología de la biopsia de pulmón mostró una enfermedad pulmonar intersticial no específica.
El diagnóstico final fue PG y síndrome símil granulomatosis de Wegener inducido por cocaína, basado en la destrucción de la línea media de naríz y paladar, acompañado de infiltrado pulmonar mixto y nódulos cavitarios pulmonares bilaterales. La cocaína fue implicada como la causa de la enfermedad debido a la mejoría clínica o recaída luego del cese o consumo, respectivamente, con incremento de los títulos de pANCA de 1:160 luego del abuso de consumo y la detección de ANCAs HNE específico.
Luego de la presentación inicial, la paciente presentaba episodios severos de PG, asociado con el consumo de cocaína. El brote más reciente se acompañó de púrpura retiforme significativa y compromiso de piernas y orejas. Actualmente la enfermedad permanece estable con la administración de ciclofosfamida en bolo, a pesar del consumo continuado de cocaína, verificado con el testeo de la orina de la paciente.
La inhalación de cocaína puede ocasionar inflamación nasal y necrosis por el efecto vasoconstrictor, microtraumas causados por cocaína y las sustancias acompañantes y el incremento de incidencia de infecciones causadas por Estafilococo aureus. Estos factores se conocen como causa de lesiones destructivas de la línea media inducidas por cocaína (CIMDL). El principal problema radica en diferenciar CIMDL de WG primario. Para este propósito, Trimarchi y col evaluaron los hallazgos clínicos, radiológicos, histopatológicos y serológicos en pacientes con WG, y compararlos con los casos de CIMDL. El grado de destrucción nasal y paranasal es más severo en pacientes con CIMDL; sin embargo, el compromiso pulmonar, renal y la destrucción de orejas y órbita son más comunes en WG.
Al compararlo con CIMDL, la WG se asoció con una frecuencia más alta de fiebre, malestar general, artralgias y mialgias, y también anormalidades de laboratorio como incremento de los reactantes de fase aguda, microhematuria, proteinuria y daño renal. Radiológicamente, la perforación del septum nasal y el compromiso de otras estructuras nasales fue más frecuente en pacientes con CIMDL. Histológicamente, la presencia de cambios no específicos en las biopsias fue mayor en CIMDL. Las biopsias de pacientes con WG mostraron microabcesos, granulomas o células gigantes multinucleadas a nivel extravascular, con necrosis localizada y profunda.
Un importante hallazgo para el diagnóstico diferencial de WG y CIMDL es la presencia de ANCAs. Los antígenos de ANCA clásico asociados a vasculitis son PR3 y MPO. La presencia de PR3 apoya el diagnóstico de WG, mientras que el MPO se asocia con granulomatosis de Churg Strauss y poliangeítis microscópica. El p ANCA está casi siempre asociado con MPO, y el ANCA citoplasmático se asocia típicamente con PR3. Sin embargo, existen otros ANCA atípicos que están normalmente asociados con patrón perinuclear
Estos ANCA atípicos incluyen el HNE, lactoferrina, azuricidina, catalasa K, incremento de la proteína bactericida y de permeabilidad (BPI), catepsina G, defensina y lisozima.
El HNE es un ANCA atípico que se lo ha relacionado estructuralmente y funcionalmente el ANCA PR3, y por esta razón puede simular a favor de WG en esta paciente.
El ANCA HNE fue recientemente descripto como un marcador de CIMDL; sin embargo, es raro detectarlo en pacientes con WG.
El diagnóstico diferencial de lesiones destructivas de la línea media incluye entre otros CIMDL, WG, linfoma extranodal, carcinoma de células escamosas, reticulosis maligna de la línea media, TB, sífilis, leishmaniasis, blastomicosis y actinomicosis.
Otro detalle interesante de este caso es la relación con el abuso de cocaína y desarrollo de PG. Los dos casos descriptos por Roche y col en 2008 son los únicos casos similares publicados actualmente (Tabla 1).
En conclusión, se reporta el caso en el que los hallazgos clínicos fueran gatillados por el abuso de cocaína acompañado de un título elevado de HNE ANCA. La similitud de estos autoanticuerpos de ANCA PR3, junto con los efectos tóxicos de cocaína, podría explicar la destrucción de la línea media y las lesiones pulmonares que simulan WG. Las lesiones de PG, una dermatosis neutrofílica, podría relacionarse con la presencia de estos anticuerpos.
Según el conocimiento de los autores, este es el tercer caso de PG reportado, y el primero en incluir compromiso pulmonar simulando WG inducido por cocaína, ilustrando los hallazgos clínicos que producen autoinmunidad relacionada con esta droga. El título elevado de elastasa ANCA parece relacionarse con el abuso de cocaína y empeoramiento del PG en este caso. Este caso destaca la importancia de ANCA HNE para el diagnóstico, y la incorporación del abuso de cocaína en la etiología del PG.
![]()
¿Qué aporta este artículo a la práctica dermatológica?.
El abuso de cocaína se asocia con varias enfermedades cutáneas y reumatológicas que simulan enfermedades autoinmunes, incluyendo la púrpura retiforme con compromiso de orejas, lesiones destructivas de la línea media inducidas por cocaína (CIMDL), y pioderma gangrenoso eruptivo.
Reportes previos han sugerido la utilidad de los anticuerpos citoplasmáticos antineutrofílico perinucleares (pANCA) con especificidad contra la elastasa neutrofílica humana (HNE) para diferenciar estas enfermedades inducidas por cocaína de enfermedades autoinmune primarias.
La púrpura retiforme, destrucción de la línea media y PG son síndromes asociados con el consumo de cocaína. El p ANCA con especificidad contra HNE es un marcador de enfermedades dermatológicas y reumatológicas inducidas por cocaína.
La correlación clínico patológica permite la diferenciación de WG de síndromes clínicos inducidos por cocaína.
La cocaína debería considerarse en la lista de causas de PG. El suspender el abuso de cocaína es el tratamiento más efectivo, pero la ciclofosfamida puede ser útil si el paciente continúa usando la droga.
♦ Comentario y resúmen objetivo: Dra. Geraldina Rodríguez Rivello.