
La ministra de Salud de la Nación, Carla Vizzotti, y su par de Ciencia, Tecnología e Innovación, Daniel Filmus, informaron el 18 de octubre que la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) aprobó la inscripción en el Registro de Especialidades Medicinales de la vacuna argentina ARVAC Cecilia Grierson bivariante contra la COVID-19, desarrollada en conjunto por el CONICET, la Universidad Nacional de San Martín (UNSAM) y el Laboratorio Pablo Cassará. Se trata de un hecho histórico, ya que es la primera vez que una vacuna contra enfermedades infecciosas fue diseñada y desarrollada integralmente en Argentina.
ANMAT aprobó la versión bivalente de esta vacuna de segunda generación, diseñada para administrarse como refuerzo, por ahora, a mayores de 18 años. Se basa en la tecnología de proteína recombinante, segura y muy probada en otras vacunas previas.
Vizzotti felicitó a la ANMAT por “todo el camino que hizo con esta vacuna” que es “un reaseguro enorme para nuestro país y también una puerta de entrada a la región para poder exportarla”. Y concluyó: “Este es el país que nos da orgullo, el país por el que trabajamos y por el que vamos a seguir trabajando siempre”. Por su parte, su par de Ciencia, Daniel Filmus, dijo que el aval a esta vacuna se trata de “un hito para la ciencia y la tecnología argentina luego de tres años muy duros, de mucha inversión pública y de mucha articulación pública y privada”.
“Es la primera vez que Argentina tiene un desarrollo íntegramente propio en vacunas que no solo va a abastecer al mercado local si no que se va a exportar, y que deja una plataforma que va a posibilitar transferir la tecnología para el desarrollo de otras vacunas. Argentina importa vacunas por 500 millones de dólares al año y este desarrollo va a significar un gran paso para sustituir importaciones”, agregó Filmus.

Por su parte, la investigadora del CONICET a cargo del proyecto, Juliana Cassataro, presentó los resultados de fase 2/3 de la vacuna y tras detallar que “la ARVAC Cecilia Grierson nació como un proyecto de un grupo de investigadores de la UNSAM y el CONICET, en una mesada de laboratorio, a comienzos de la pandemia” agregó que “desde el inicio el proyecto tuvo un fuerte apoyo y financiamiento del Estado, a través del Ministerio de Ciencia y de la Agencia I+D+i. Rápidamente se acopló el sector privado, a través del Laboratorio Cassará. Y a partir de ahí se conformó una red federal de más de 600 investigadores, 24 instituciones científicas públicas y privadas y, algo importantísimo, más de 2 mil voluntarios”.
Así, subrayó “la satisfacción de haber completado todas las fases de una vacuna 100% argentina, nos queda el orgullo de contar con una capacidad instalada y las redes para encarar nuevos proyectos”.
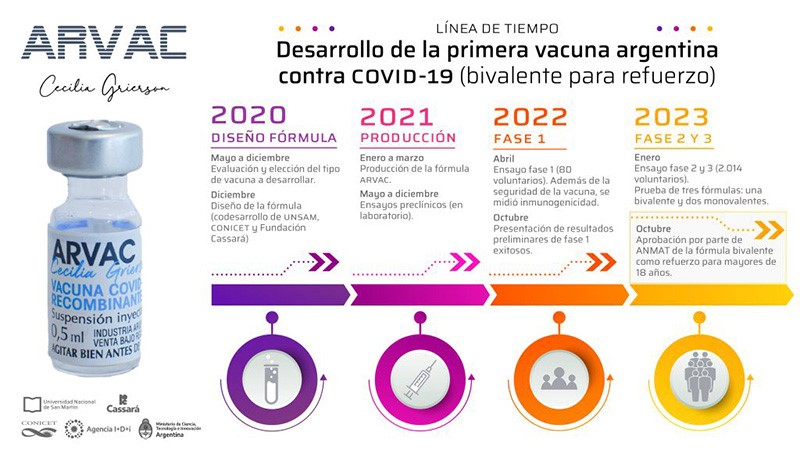
Datos sobre la vacuna ARVAC Cecilia Grierson
• Es una vacuna de segunda generación, diseñada para usarse como refuerzo. Podrá utilizarse en individuos ya vacunados con otras plataformas de vacunas, como las de adenovirus o ARNm.
• En los ensayos de fase 2/3 se probaron tres fórmulas de la vacuna: dos monovalentes y una bivalente. Las tres variantes demostraron ser seguras y eficaces en 2.014 personas. La ANMAT aprobó la versión bivalente para mayores de 18 años, pero en un futuro podría aprobar las otras dos versiones.
• Se puede almacenar bajo temperatura de heladera, entre 2 y 8°C.
• Se basa en la tecnología de proteínas recombinantes, una tecnología segura que puede aplicarse a embarazadas, bebés, inmunosuprimidos y se utiliza desde hace más de 20 años en las vacunas contra la Hepatitis B en niños recién nacidos, o más recientemente con la vacuna contra la VPH. Se trata de una plataforma que además puede adaptarse fácilmente ante el surgimiento de nuevas variantes de preocupación en un tiempo relativamente breve de entre tres y cuatro meses.