Los Estándares de Atención de la Diabetes de la Asociación Estadounidense de Diabetes (ADA) se actualizan y publican anualmente y son desarrollados por el Comité de Práctica Profesional multidisciplinario de la ADA, que está compuesto por profesionales expertos en atención médica (HCP, por sus siglas en inglés) en diabetes. Incluye las recomendaciones basadas en evidencia más actuales para diagnosticar y tratar adultos y niños con todas las formas de diabetes. El sistema de calificación de la ADA usa A, B, C o E para mostrar el nivel de evidencia que respalda cada recomendación.
A: Evidencia clara de ensayos controlados aleatorios generalizables y bien realizados que tienen el poder estadístico adecuado
B: Evidencia de apoyo de estudios de cohortes bien realizados
C: Evidencia de apoyo de estudios mal controlados o no controlados
E: Consenso de expertos o experiencia clínica
| 1. Mejorar la atención y promover la salud en las poblaciones |
| Diabetes y salud de la población |
La atención centrada en la persona considera las comorbilidades y los pronósticos de los pacientes individuales; es respetuosa y sensible a las preferencias, necesidades y valores del paciente; y asegura que estas consideraciones guíen todas las decisiones clínicas. Además, los determinantes sociales de la salud (SDOH), a menudo fuera del control directo del individuo y que potencialmente representan un riesgo de por vida, contribuyen a los resultados psicosociales y de atención médica y deben abordarse para mejorar todos los resultados de salud.
|
Recomendaciones 1.1 Asegúrese de que las decisiones de tratamiento sean oportunas, se basen en pautas basadas en evidencia, incluyan el apoyo de la comunidad social y se tomen en colaboración con los pacientes en función de las preferencias individuales, los pronósticos, las comorbilidades y las consideraciones financieras informadas. (B) 1.2 Alinear los enfoques para el control de la diabetes con el Modelo de Atención Crónica. Este modelo enfatiza la atención en equipo centrada en la persona, los enfoques de tratamiento integrados a largo plazo para la diabetes y las comorbilidades, y la comunicación colaborativa continua y el establecimiento de objetivos entre todos los miembros del equipo. (A) 1.3 Los sistemas de atención deben facilitar la atención presencial y virtual en equipo, incluidos aquellos con conocimientos y experiencia en el control de la diabetes como parte del equipo y la utilización de registros de pacientes, herramientas de apoyo a la toma de decisiones y participación de la comunidad para satisfacer las necesidades de los pacientes. (B) |
| Estrategias para la mejora a nivel del sistema |
- Equipos de atención
Los equipos colaborativos y multidisciplinarios son los más adecuados para brindar atención a las personas con diabetes y facilitar el autocontrol de los pacientes, con énfasis en evitar la inercia terapéutica para lograr los objetivos metabólicos recomendados.
- Telesalud
La telesalud puede aumentar el acceso a la atención de las personas con diabetes. La telesalud debe usarse como complemento de las visitas en persona para optimizar el control glucémico en personas con diabetes no controlada. La evidencia sugiere que la telesalud puede ser eficaz para reducir la hemoglobina glicosilada (A1C) en personas con diabetes tipo 2 en comparación con la atención habitual o además de ella. Las estrategias interactivas que facilitan la comunicación entre los profesionales de la salud y los pacientes parecen más efectivas.
- Comportamientos y Bienestar
El cuidado exitoso de la diabetes requiere un enfoque sistemático para apoyar los esfuerzos de cambio de comportamiento de los pacientes, incluida la educación y el apoyo para el autocontrol de la diabetes (DSMES, por sus siglas en inglés) de alta calidad.
| Adaptación del tratamiento al contexto social |
|
Recomendaciones 1.5 Evaluar la inseguridad alimentaria, la inseguridad de vivienda, la falta de vivienda, las barreras financieras y el capital social y apoyo comunitario social para informar las decisiones de tratamiento, con referencia a los recursos comunitarios locales apropiados. (A) 1.6 Proporcionar a los pacientes apoyo adicional para el autocontrol de parte de entrenadores de salud o trabajadores comunitarios de la salud cuando estén disponibles. (A) |
Las desigualdades en salud relacionadas con la diabetes están bien documentadas y se han asociado con un mayor riesgo de diabetes, una mayor prevalencia en la población y peores resultados de la diabetes. Las barreras financieras para el uso de medicamentos continúan contribuyendo a las disparidades en la salud.
| 2. Clasificación y Diagnóstico de la Diabetes |
| Clasificación |
La diabetes se puede clasificar en las siguientes categorías generales:
- Diabetes tipo 1: debida a la destrucción autoinmune de las células β, que generalmente conduce a una deficiencia absoluta de insulina, incluida la diabetes autoinmune latente de la edad adulta.
- Diabetes tipo 2: debida a una pérdida progresiva de la secreción de insulina de las células β frecuentemente en el contexto de la resistencia a la insulina.
- Tipos específicos de diabetes debido a otras causas, p. ej., síndromes de diabetes monogénica (como la diabetes neonatal y la diabetes de inicio en la madurez de los jóvenes), enfermedades del páncreas exocrino (como la fibrosis quística y la pancreatitis) y las inducidas por fármacos o sustancias químicas, diabetes (como con el uso de glucocorticoides, en el tratamiento del VIH/SIDA o después de un trasplante de órganos).
- Diabetes mellitus gestacional (DMG): diabetes diagnosticada en el segundo o tercer trimestre del embarazo que no era claramente una diabetes manifiesta antes de la gestación.
La clasificación del tipo de diabetes no siempre es sencilla en la presentación y puede ocurrir un diagnóstico erróneo. Por lo tanto, es necesaria una diligencia constante y, en ocasiones, una reevaluación.
- Los niños con diabetes tipo 1 suelen presentar poliuria y polidipsia, y aproximadamente la mitad presenta cetoacidosis diabética (CAD).
- Los adultos con diabetes tipo 1 pueden ser diagnosticados a cualquier edad y es posible que no presenten los síntomas clásicos. Pueden tener una remisión temporal por la necesidad de insulina. El diagnóstico puede volverse más obvio con el tiempo y debe reevaluarse si existe alguna preocupación.
| Pruebas de detección y diagnóstico de prediabetes y diabetes tipo 2 |
Los criterios de diagnóstico para diabetes y prediabetes se muestran en la Tabla siguiente. Se recomienda la detección del riesgo de prediabetes y diabetes tipo 2 a través de una evaluación informal de los factores de riesgo o con una herramienta de evaluación, como la Prueba de Riesgo de Diabetes de la ADA (diabetes.org/socrisktest) y puede informar quién necesita pruebas de laboratorio.
| Tabla: Criterios para la detección de diabetes o prediabetes en adultos asintomáticos |
|
1. Se debe considerar la realización de pruebas en adultos con sobrepeso u obesidad (IMC ≥25 kg/m2 o ≥23 kg/m2 en individuos asiático-americanos) que tengan uno o más de los siguientes factores de riesgo: - Familiar de primer grado con diabetes. - Raza/origen étnico de alto riesgo (p. ej., afroamericano, latino, nativo americano, asiático americano, isleño del Pacífico). - Historia de enfermedad cardiovascular (ECV). - Hipertensión (≥140/90 mmHg o en terapia para la hipertensión). - Nivel de colesterol HDL <35 mg/dL (0,90 mmol/L) y/o nivel de triglicéridos >250 mg/dL (2,82 mmol/L). - Individuos con síndrome de ovario poliquístico. - Inactividad física. - Otras condiciones clínicas asociadas con la resistencia a la insulina (p. ej., obesidad severa, acantosis nigricans). 2. Las personas con prediabetes (A1C ≥5,7 % [39 mmol/mol], IGT o IFG) deben hacerse la prueba anualmente. 3. Las personas a las que se les diagnosticó diabetes mellitus gestacional (DMG) deben hacerse pruebas de por vida al menos cada 3 años. 4. Para todas las demás personas, las pruebas deben comenzar a los 35 años. 5. Si los resultados son normales, las pruebas deben repetirse en intervalos mínimos de 3 años, con la consideración de pruebas más frecuentes según los resultados iniciales y el estado de riesgo. 6. Personas con VIH. Siglas: IFG, alteración de la glucosa en ayunas; IGT, alteración de la tolerancia a la glucosa; A1C: Hemoglobina glicosilada |
| Detección basada en el riesgo de diabetes tipo 2 o prediabetes en niños y adolescentes asintomáticos en un entorno clínico |
Se debe considerar la detección en jóvenes *que tienen sobrepeso (≥ percentil 85) u obesidad (≥ percentil 95) y que tienen uno o más factores de riesgo adicionales según la fuerza de su asociación con la diabetes:
- Antecedentes maternos de diabetes o diabetes mellitus gestacional (DMG) durante la gestación del niño (A).
- Antecedentes familiares de diabetes tipo 2 en familiar de primer o segundo grado (A).
- Raza/origen étnico (nativo americano, afroamericano, latino, asiático americano, isleño del Pacífico) (A).
- Signos de resistencia a la insulina o afecciones asociadas con la resistencia a la insulina (acantosis nigricans, hipertensión arterial, dislipidemia, síndrome de ovario poliquístico o peso al nacer pequeño para la edad gestacional) (B).
*Después del inicio de la pubertad o después de los 10 años de edad, lo que ocurra primero. Si las pruebas son normales, se recomienda repetir las pruebas en intervalos mínimos de 3 años (o con mayor frecuencia si el IMC aumenta o el perfil de factores de riesgo se deteriora). Existen informes de diabetes tipo 2 antes de los 10 años, y esto se puede considerar con numerosos factores de riesgo.
Las marcadas discrepancias entre la A1C medida y los niveles de glucosa en plasma deben hacer pensar que el análisis de A1C puede no ser confiable para esa persona, y se debe considerar el uso de un análisis de A1C alternativo o criterios de glucosa en sangre plasmática para el diagnóstico. (Hay disponible una lista actualizada de ensayos de A1C con interferencias en ngsp.org/interf.asp).
Si un individuo tiene un resultado de la prueba cerca de los márgenes del umbral de diagnóstico, el médico debe seguir de cerca a esa persona y repetir la prueba en 3 a 6 meses. Si se utiliza la prueba de tolerancia a la glucosa oral (OGTT), se debe evitar el ayuno o la restricción de carbohidratos 3 días antes de la prueba, ya que puede elevar falsamente los niveles de glucosa.
| Criterios para el Tamizaje y Diagnóstico de Prediabetes y Diabetes | ||
| A1C | 5,4-6,4% (39-47 mmol/mol) | ≥6,5 %(48mmol/mol) |
| FPG | 100-125 mg/dL (5,6-6,9 mmol/mol/L) | ≥126 mg/dl (7,0 mmol/l) |
| Glucemia dos horas después de sobrecarga 75 gr | 140-199 mg/dL (7,8-11,0 mmol/mol/L) | ≥200 mg/dl (11,1 mmol/l) |
| Glucemia al azar | - | ≥200 mg/dl (11,1 mmol/l) |
| Detección antes del embarazo |
|
Recomendación 2.26 (A) En las personas que planean quedarse embarazadas, evalúe a aquellas con factores de riesgo (B) y considere realizar pruebas a todas las personas en edad fértil para detectar diabetes no diagnosticada. |
| 3. Prevención o retraso de la diabetes tipo 2 y comorbilidades asociadas |
|
Recomendación 3.1 Supervisar el desarrollo de diabetes tipo 2 en personas con prediabetes al menos una vez al año; modificar en función de la evaluación individual de riesgos/beneficios. |
| Cambio de comportamiento en el estilo de vida para la prevención de la diabetes |
|
Recomendaciones 3.2 Referir a los adultos con sobrepeso/obesidad con alto riesgo de diabetes tipo 2, según lo tipificado por el Programa de Prevención de la Diabetes (DPP), a un programa intensivo de cambio de comportamiento de estilo de vida para lograr y mantener una reducción de peso de al menos el 7% del peso corporal inicial a través de dieta saludable baja en calorías y ≥150 minutos/semana de actividad física de intensidad moderada. (A) 3.3 Se puede considerar una variedad de patrones de alimentación para prevenir la diabetes en personas con prediabetes. (B) |
El ensayo DPP demostró que una intervención intensiva en el estilo de vida podría reducir el riesgo de diabetes tipo 2 incidente en un 58 % durante 3 años. Se ha demostrado que DPP es rentable y que los programas asistidos por tecnología pueden ser efectivos y deben ser considerados.
Hay disponible una lista de los programas de cambio de estilo de vida para la prevención de la diabetes reconocidos por los Centros para el Control y la Prevención de Enfermedades (CDC)
| Intervenciones farmacológicas |
|
Recomendaciones 3.6 La terapia con metformina para la prevención de la diabetes tipo 2 se debe considerar en adultos con alto riesgo de diabetes tipo 2, según lo tipificado por el DPP, especialmente aquellos de 25 a 59 años con un IMC ≥35 kg/m2, glucosa plasmática en ayunas más alta (FPG) (p. ej., ≥110 mg/dl) y A1C más alta (p. ej., ≥6,0 %) y en personas con DMG previa. (A) 3.7 El uso a largo plazo de metformina puede estar asociado con la deficiencia bioquímica de vitamina B12; considere la medición periódica de los niveles de vitamina B12 en individuos tratados con metformina, especialmente en aquellos con anemia o neuropatía periférica. (B) |
Se han evaluado varios agentes farmacológicos para la prevención de la diabetes tipo 2, y la metformina tiene la base de evidencia más sólida. Sin embargo, la Administración de Drogas y Alimentos de los Estados Unidos (FDA) no ha aprobado ningún agente para la prevención de la diabetes.
| Prevención de enfermedades vasculares y mortalidad |
|
Recomendaciones 3.8 La prediabetes se asocia con un mayor riesgo cardiovascular (CV); por lo tanto, se sugiere la detección y el tratamiento de factores de riesgo modificables de enfermedad cardiovascular (ECV). (B) 3.9 La terapia con estatinas puede aumentar el riesgo de diabetes tipo 2 en personas con alto riesgo de desarrollar diabetes tipo 2. En tales individuos, el estado de la glucosa debe controlarse regularmente y deben reforzarse los enfoques de prevención de la diabetes. No se recomienda suspender las estatinas. (B) 3.10 En personas con antecedentes de accidente cerebrovascular y evidencia de resistencia a la insulina y prediabetes, se puede considerar que la pioglitazona reduce el riesgo de accidente cerebrovascular o infarto de miocardio (IM). Sin embargo, este beneficio debe equilibrarse con el mayor riesgo de aumento de peso, edema y fractura. A Las dosis más bajas pueden mitigar el riesgo de efectos adversos. (C) |
| Metas de atención centradas en la persona |
|
Recomendaciones 3.11 En adultos con sobrepeso/obesidad con alto riesgo de diabetes tipo 2, los objetivos de atención deben incluir la pérdida de peso o la prevención del aumento de peso, minimizando la progresión de la hiperglucemia y la atención del riesgo CV y las comorbilidades asociadas. (B) 3.12 Se puede considerar la farmacoterapia (p. ej., para controlar el peso, minimizar la progresión de la hiperglucemia, reducir el riesgo CV) para apoyar los objetivos de atención centrados en la persona. (B) 3.13 Se deben considerar enfoques preventivos más intensivos en individuos que tienen un riesgo particularmente alto de progresión a diabetes, incluidos individuos con IMC ≥35 kg/m2, aquellos con niveles de glucosa más altos (p. ej., GPA 110–125 mg/dL, 2- una hora después de la exposición, glucosa 173–199 mg/dL, A1C ≥6,0 %) e individuos con antecedentes de DMG. (A) |
| 4. Evaluación Médica Integral y Valoración de Comorbilidades |
| Atención colaborativa centrada en la persona |
|
Recomendaciones 4.1 Un estilo de comunicación centrado en la persona que usa un lenguaje centrado en la persona, culturalmente sensible y basado en fortalezas y escucha activa; suscita preferencias y creencias individuales; y evalúa la alfabetización, la aritmética y las posibles barreras a la atención deben utilizarse para optimizar los resultados de salud y la calidad de vida (QoL) relacionada con la salud. (B) |
Los objetivos del tratamiento de la diabetes son prevenir o retrasar las complicaciones y optimizar la calidad de vida (QoL) relacionada con la salud. El uso de un lenguaje inclusivo y empoderador que sea respetuoso y libre de estigma puede ayudar a informar y motivar a las personas.
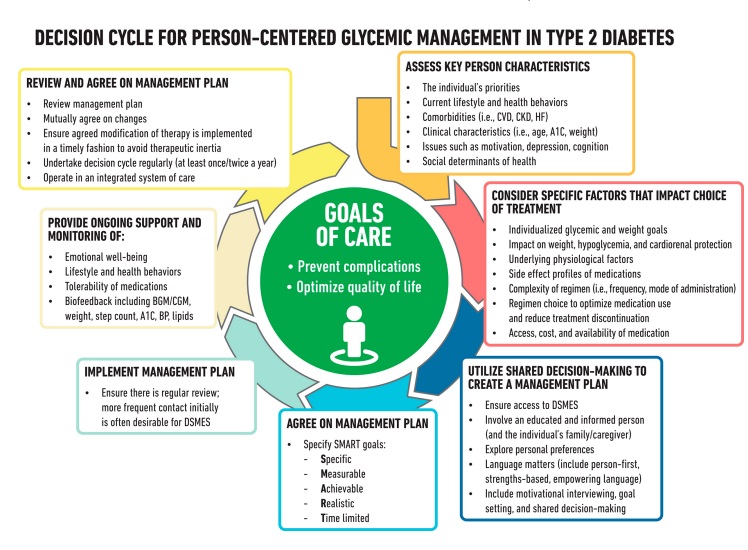
Figura 4.1
Ciclo de decisión para el control glucémico centrado en la persona en la diabetes tipo 2. Adaptado de Davies MJ, Aroda VR, Collins BS, et al. Cuidado de la diabetes 2022;45:2753–2786.
| Evaluación Médica Integral |
|
Recomendaciones 4.3 Se debe realizar una evaluación médica completa en la visita inicial para: Confirmar el diagnóstico y clasificar la diabetes. (A) Evalúe las complicaciones de la diabetes, las posibles condiciones comórbidas y el estado general de salud. (A) Revisar el tratamiento previo y el control de los factores de riesgo en personas con diabetes establecida. (A) Comience a comprometerse con la persona con diabetes en la formulación de un plan de gestión de la atención que incluya los objetivos iniciales de la atención. (A) Desarrolle un plan para la atención continua. (A) 4.4 Una visita de seguimiento debe incluir la mayoría de los componentes de la evaluación médica integral inicial. (A) 4.5 El manejo continuo debe guiarse por la evaluación del estado de salud general, las complicaciones de la diabetes, el riesgo cardiovascular, el riesgo de hipoglucemia y la toma de decisiones compartida para establecer objetivos terapéuticos. (B) |
| Vacunas SARS-CoV-2 y otras inmunizaciones |
La importancia de las vacunas de rutina para las personas con diabetes ha aumentado debido a la pandemia de la enfermedad por coronavirus 2019 (COVID-19). La prevención de infecciones evitables no solo previene directamente la morbilidad, sino que también reduce las hospitalizaciones, lo que además puede reducir el riesgo de contraer infecciones como la COVID-19. Los niños y adultos con diabetes deben recibir vacunas de acuerdo con las recomendaciones apropiadas para su edad.
En las personas con diabetes, los niveles más altos de glucosa en sangre antes y durante el ingreso por COVID-19 se han asociado con malos resultados, incluida la mortalidad. Se debe priorizar a las personas con diabetes y ofrecerles vacunas contra el SARS-CoV-2.
| Evaluación de comorbilidades seleccionadas |
- Cáncer
Se debe alentar a las personas con diabetes a que se sometan a las pruebas de detección del cáncer recomendadas según su edad y sexo y a que reduzcan sus factores de riesgo de cáncer modificables (obesidad, inactividad física y tabaquismo).
- Enfermedad del hígado graso no alcohólico
|
Recomendación 4.10 Las personas con diabetes tipo 2 o prediabetes con factores de riesgo cardiometabólico, que tienen enzimas hepáticas elevadas (ALT) o hígado graso en imágenes o ecografías, deben ser evaluadas para detectar la presencia de esteatohepatitis no alcohólica y fibrosis hepática. (C) |
| 5. Facilitar comportamientos de salud positivos y bienestar para mejorar los resultados de salud |
Esencial para lograr los objetivos del tratamiento de la diabetes son la educación para el autocontrol de la diabetes y apoyo (DSMES), terapia de nutrición médica (MNT), actividad física de rutina, asesoramiento para dejar de fumar cuando sea necesario, asesoramiento sobre comportamiento de salud y atención psicosocial.
| Educación para el autocontrol de la diabetes y apoyo (DSMES) |
|
Recomendaciones 5.2 Hay cuatro momentos críticos para evaluar la necesidad de que DSMES promueva la adquisición de habilidades para ayudar a la implementación del plan de tratamiento, MNT y bienestar: en el momento del diagnóstico, anualmente y/o cuando no se cumplen los objetivos del tratamiento, cuando se desarrollan factores de complicación (médicos, físicos, psicosociales), y cuando ocurren transiciones en la vida y el cuidado. (E) 5.4 Los DSMES deben estar centrados en la persona, pueden ofrecerse en entornos grupales o individuales y deben comunicarse con todo el equipo de atención de la diabetes. (A) 5.5 Las intervenciones de coaching digital y autogestión digital pueden ser métodos efectivos para brindar DSMES. (B) 5.9 Considere abordar las barreras para el acceso a DSMES a través de la prestación de atención de telesalud (B) y otras soluciones de salud digital. (C) |
| Terapia de Nutrición Médica (MNT) |
Todos los profesionales de la salud deben referir a las personas con diabetes para que reciban MNT individualizados proporcionados por un nutricionista dietista registrado que tenga conocimientos y habilidades para proporcionar MNT específicos para la diabetes.
| Objetivos de la terapia nutricional para adultos con diabetes |
- Para promover y apoyar patrones de alimentación saludables, enfatizando una variedad de alimentos densos en nutrientes en porciones apropiadas, para mejorar la salud general.
- Lograr y mantener los objetivos de peso corporal.
- Lograr objetivos individualizados de glucemia, presión arterial (PA) y lípidos
- Retrasar o prevenir las complicaciones de la diabetes.
- Abordar las necesidades nutricionales individuales en función de las preferencias personales y culturales, la alfabetización en salud y la aritmética, el acceso a alimentos saludables, la voluntad y la capacidad de realizar cambios de comportamiento y las barreras existentes para el cambio.
- Para mantener el placer de comer al proporcionar mensajes sin prejuicios sobre las opciones de alimentos y limitar las opciones de alimentos solo cuando lo indique la evidencia científica.
- Proporcionar a una persona con diabetes las herramientas prácticas para desarrollar patrones de alimentación saludables en lugar de centrarse en macronutrientes, micronutrientes o alimentos individuales.
| Evaluación de la inseguridad alimentaria |
Cualquier miembro del equipo de atención médica puede detectar la inseguridad alimentaria utilizando The Hunger Vital Sign. Los hogares se consideran en riesgo si responden una o ambas de las siguientes afirmaciones como "a menudo cierto" o "a veces es cierto" (en comparación con "nunca es cierto"):
1. “En los últimos 12 meses, nos preocupaba si nuestra comida se acabaría antes de que tuviéramos dinero para comprar más”.
2. “En los últimos 12 meses, la comida que comprábamos simplemente no duraba y no teníamos dinero para comprar más”.
| Actividad física |
|
Recomendaciones 5.28 Los niños y adolescentes con diabetes tipo 1 (C) o diabetes tipo 2 o prediabetes (B) deben participar en 60 minutos/día o más de actividad aeróbica de intensidad moderada o vigorosa, con actividades vigorosas de fortalecimiento muscular y de fortalecimiento óseo al menos 3 días/ semana. 5.29 La mayoría de los adultos con diabetes tipo 1 (C) y diabetes tipo 2 (B) deben participar en 150 minutos o más de actividad aeróbica de intensidad moderada a vigorosa por semana, repartidos en al menos 3 días a la semana, con no más de 2 días consecutivos sin actividad. Duraciones más cortas (mínimo 75 minutos/semana) de entrenamiento de intensidad vigorosa o de intervalos pueden ser suficientes para personas más jóvenes y en mejor forma física. 5.30 Los adultos con diabetes tipo 1 (C) y diabetes tipo 2 (B) deben realizar de 2 a 3 sesiones por semana de ejercicios de fuerza en días no consecutivos. 5.31 Todos los adultos, y en particular aquellos con diabetes tipo 2, deben disminuir la cantidad de tiempo que dedican al comportamiento sedentario diario. (B) La posición sentado prolongada debe interrumpirse cada 30 minutos para obtener beneficios de glucosa en sangre. (C) 5.32 Se recomienda el entrenamiento de la flexibilidad y el entrenamiento del equilibrio 2 o 3 veces por semana para los adultos mayores con diabetes. El yoga y el tai chi pueden incluirse según las preferencias individuales para aumentar la flexibilidad, la fuerza muscular y el equilibrio. (C) 5.33 Evaluar la actividad física basal y el tiempo sedentario. Promover el aumento de las actividades no sedentarias por encima de la línea de base para las personas sedentarias con diabetes tipo 1 (E) y diabetes tipo 2. (B) Los ejemplos incluyen caminar, yoga, tareas domésticas, jardinería, natación y baile. |
| Dejar de fumar: tabaco y cigarrillos electrónicos |
|
Recomendaciones 5.34 Aconseje a todas las personas que no usen cigarrillos y otros productos de tabaco o cigarrillos electrónicos. (A) 5.35 Después de identificar el uso de tabaco o cigarrillos electrónicos, incluir asesoramiento para dejar de fumar y otras formas de tratamiento como un componente de rutina del cuidado de la diabetes. (A) |
| Atención Psicosocial |
|
Recomendaciones 5.38 Se debe brindar atención psicosocial a todas las personas con diabetes, con el objetivo de optimizar la calidad de vida relacionada con la salud y los resultados de salud. Dicha atención debe integrarse con la atención médica de rutina y ser brindada por profesionales de la salud capacitados mediante un enfoque colaborativo, centrado en la persona y culturalmente informado. (A) Cuando esté indicado y disponible, los profesionales de salud mental calificados deben proporcionar atención de salud mental específica adicional. (B) 5.39 Los equipos de atención de la diabetes deben implementar protocolos de detección psicosocial que pueden incluir, entre otros, actitudes sobre la diabetes, expectativas de tratamiento y resultados, estado de ánimo general y relacionado con la diabetes, estrés y/o calidad de vida relacionada con la salud, recursos disponibles (financieros, sociales, familiares y emocional) y/o antecedentes psiquiátricos. La detección debe realizarse a intervalos periódicos y cuando haya un cambio en la enfermedad, el tratamiento o las circunstancias de la vida. (C) 5.40 Cuando esté indicado, derivar a profesionales de la salud mental u otros profesionales capacitados para una evaluación y tratamiento adicionales de los síntomas de angustia por diabetes, depresión, tendencias suicidas, ansiedad, miedo a la hipoglucemia relacionado con el tratamiento, trastornos alimentarios y/o capacidades cognitivas. Dicha atención psicosocial especializada debe utilizar herramientas y enfoques de tratamiento estandarizados y validados apropiados para la edad. (B) 5.42 Supervise de forma rutinaria a las personas con diabetes, a los cuidadores y a los miembros de la familia en busca de angustia por la diabetes, en particular cuando no se alcanzan los objetivos del tratamiento y/o al comienzo de las complicaciones de la diabetes. Consulte a un profesional de salud mental calificado u otro profesional sanitario capacitado para una evaluación y tratamiento adicionales si está indicado. (B) |
Consulte la declaración de posición de la ADA "Atención psicosocial para personas con diabetes" para obtener una lista de herramientas de evaluación y detalles adicionales y el Conjunto de herramientas de salud mental de la ADA para cuestionarios de evaluación y encuestas.
| Salud del sueño |
|
Recomendación 5.55 Considerar la detección de la salud del sueño en personas con diabetes, incluidos los síntomas de los trastornos del sueño, las interrupciones del sueño debido a los síntomas de la diabetes o las necesidades de control, y las preocupaciones sobre el sueño. Derivar a medicina del sueño y/o a un profesional de la salud del comportamiento calificado, según se indique. (B) |
Las asociaciones entre los problemas del sueño y la diabetes son complejas: los trastornos del sueño son un factor de riesgo para desarrollar diabetes tipo 2 y posiblemente diabetes mellitus gestacional (DMG). Además, los trastornos del sueño se asocian con una menor participación en el autocontrol de la diabetes y pueden interferir con el logro de los objetivos glucémicos entre las personas con diabetes tipo 1 y tipo 2.
| 6. Objetivos glucémicos |
| Evaluación del control glucémico |
El control glucémico se evalúa mediante la medición de A1C, la monitorización continua de la glucosa (CGM) utilizando el tiempo en rango (TIR) y/o el indicador de control de la glucosa (GMI) y la monitorización de la glucosa en sangre (BGM).
| Evaluación glucémica |
|
Recomendaciones 6.1 Evaluar el estado glucémico (A1C u otra medida glucémica como TIR o GMI) al menos dos veces al año en pacientes que cumplen los objetivos del tratamiento (y que tienen un control glucémico estable). (E) 6.2 Evaluar el estado glucémico al menos trimestralmente y según sea necesario en pacientes cuya terapia haya cambiado recientemente y/o que no estén alcanzando los objetivos glucémicos. (E) |
| Evaluación de glucosa por monitorización continua de la glucosa (CGM) |
|
Recomendaciones 6.3 Los informes de glucosa estandarizados de una sola página de los dispositivos de CGM con señales visuales, como el perfil de glucosa ambulatorio (AGP), deben considerarse como un resumen estándar para todos los dispositivos de CGM. (E) 6.4 El tiempo en rango (TIR) está asociado con el riesgo de complicaciones microvasculares y puede usarse para evaluar el control glucémico. Además, el tiempo por debajo del rango (TBR) y el tiempo por encima del rango (TAR) son parámetros útiles para la evaluación del plan de tratamiento. (C) |
| Objetivos glucémicos |
|
Recomendaciones 6.5a Es apropiado un objetivo de A1C para muchos adultos (no embarazadas) de <7 % (53 mmol/mol) sin hipoglucemia significativa. (A) 6.5b Si se utiliza AGP/GMI para evaluar la glucemia, un objetivo paralelo para muchas mujeres adultas no embarazadas es una TIR de >70 % con una TBR <4 % y un tiempo <54 mg/dl <1 %. Para aquellos con fragilidad o alto riesgo de hipoglucemia, se recomienda un objetivo de >50% TIR con <1% TBR. (B) 6.6 Sobre la base del juicio del profesional de la salud (HCP) y la preferencia del paciente, el logro de niveles de A1C más bajos que la meta del 7 % puede ser aceptable e incluso beneficioso si se puede lograr de manera segura sin hipoglucemia significativa u otros efectos adversos del tratamiento. (B) 6.7 Los objetivos de A1C menos estrictos (como <8% [64 mmol/mol]) pueden ser apropiados para pacientes con una expectativa de vida limitada o donde los daños del tratamiento son mayores que los beneficios. Los profesionales de la salud deben considerar la desintensificación de la terapia, si corresponde, para reducir el riesgo de hipoglucemia en pacientes con objetivos de A1C estrictos e inapropiados. (B) |
Figura 6.1
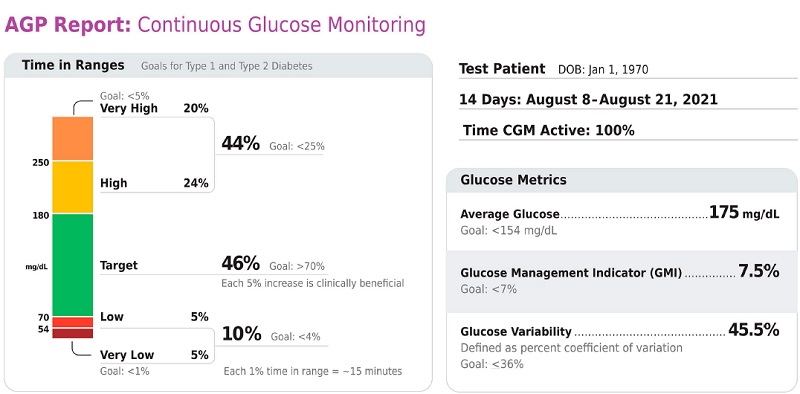
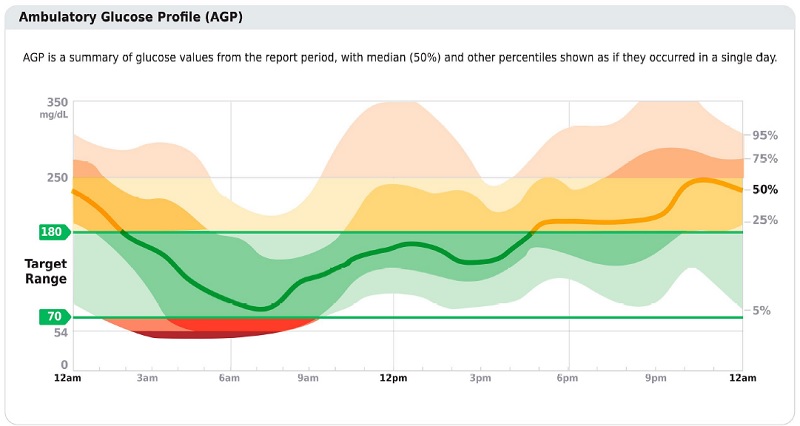
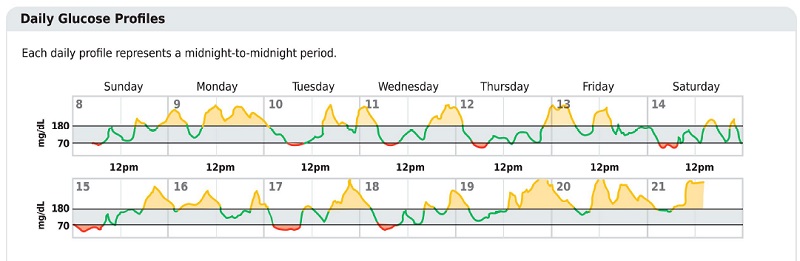
Puntos clave incluidos en el informe AGP estándar. Reimpreso de Holt RIG, DeVries JH, Hess-Fischl A, et al. Cuidado de la diabetes 2021;44:2589–2625.
Tabla 6.3
| Resumen de recomendaciones glucémicas para adultos con diabetes |
| A1C | <7,0 % (53 mmol/mol) |
| Glucosa plasmática capilar prepandial | 80-130 mg/dL (4,4 -7,2 mmol/L) |
| Pico de glucosa plasmática capilar posprandial | <180 mg/dL (10,0 mmol/L) |
| Hipoglucemia |
Las recomendaciones con respecto a la clasificación de la hipoglucemia se describen en la Tabla 6.4. Consulte los Estándares de atención completos de 2023 para conocer las estrategias detalladas contra la hipoglucemia.
Tabla 6.4
| Clasificación de la hipoglucemia |
| Criterios glucémicos/Descripción | |
| Nivel 1 | Glucosa <70 mg/dL (3,9 mmol/L) y ≥54 mg/dL (3,0 mmol/L) |
| Nivel 2 | Glucosa <54 mg/dL (3,0 mmol/L) |
| Nivel 3 | Un evento grave caracterizado por alteración del estado mental y/o físico que requiere asistencia para el tratamiento de la hipoglucemia |
Reimpreso de Agiostratidou G, Anhalt H, Ball D, et al. Cuidado de la diabetes 2017;40:1622–1630.
|
Recomendaciones 6.10 La ocurrencia y el riesgo de hipoglucemia deben revisarse en cada encuentro e investigarse según se indica. Se debe considerar el conocimiento de la hipoglucemia utilizando herramientas validadas. (C) 6.11 La glucosa (aproximadamente 15–20 g) es el tratamiento preferido para el individuo consciente con glucosa en sangre <70 mg/dL (3,9 mmol/L), aunque se puede usar cualquier forma de carbohidrato que contenga glucosa. Quince minutos después del tratamiento, si el monitoreo de glucosa (BGM) muestra hipoglucemia continua, se debe repetir el tratamiento. Una vez que la BGM o el patrón de glucosa tienen una tendencia ascendente, la persona debe consumir una comida o un refrigerio para evitar la recurrencia de la hipoglucemia. (B) 6.12 Se debe prescribir glucagon a todas las personas con mayor riesgo de hipoglucemia de nivel 2 o 3, para que esté disponible en caso de que sea necesario. Los cuidadores, el personal escolar o los miembros de la familia que brindan apoyo a estas personas deben saber dónde está y cuándo y cómo administrarlo. La administración de glucagón no se limita a los profesionales de la salud. (E) 6.13 El desconocimiento de la hipoglucemia o uno o más episodios de hipoglucemia de nivel 3 debe desencadenar la educación para evitar la hipoglucemia y la reevaluación y el ajuste del plan de tratamiento para disminuir la hipoglucemia. (E) 6.14 Se debe recomendar a los pacientes tratados con insulina que no se dan cuenta de la hipoglucemia, un evento hipoglucémico de nivel 3 o un patrón de hipoglucemia de nivel 2 inexplicable que eleven sus objetivos glucémicos para evitar estrictamente la hipoglucemia durante al menos varias semanas para revertir parcialmente la falta de conciencia de la hipoglucemia y reducir el riesgo de futuros episodios. (A) 6.15 Se sugiere una evaluación continua de la función cognitiva con una mayor vigilancia de la hipoglucemia por parte del médico, el paciente y los cuidadores si se encuentra deterioro o disminución de la cognición. (B) |
| 7. Tecnología para la diabetes |
La tecnología para la diabetes incluye dispositivos de administración de insulina como bombas de insulina (también llamadas infusión subcutánea continua de insulina [CSII]) y plumas (pen) de insulina conectadas, dispositivos de monitoreo de glucosa a través de sistemas CGM y medidores de glucosa, sistemas automatizados de administración de insulina (AID) que integran CGM y administración de insulina con algoritmos para modular la administración de insulina y software de apoyo para el autocontrol de la diabetes.
| Principios generales del dispositivo |
|
Recomendaciones 7.1 Los tipos y la selección de dispositivos deben individualizarse en función de las necesidades, preferencias y nivel de habilidad específicos de una persona. En el entorno de un individuo cuya diabetes es controlada parcial o totalmente por otra persona (p. ej., un niño pequeño o una persona con deterioro cognitivo o destreza, limitaciones psicosociales y/o físicas), las habilidades y preferencias del cuidador son parte integral de la decisión. (E) 7.2 Al prescribir un dispositivo, asegúrese de que las personas con diabetes/cuidadores reciban educación y capacitación inicial y continua, ya sea en persona o de forma remota, y una evaluación continua de la técnica, los resultados y su capacidad para utilizar datos, incluida la carga de datos para monitorear y ajustar la terapia. (C) 7.5 El inicio de CGM, CSII y/o AID en una etapa temprana del tratamiento de la diabetes puede ser beneficioso según las necesidades y preferencias de la persona/cuidador. (C) |
| Monitoreo de glucosa (BGM) |
|
Recomendaciones 7.7 Se debe alentar a las personas que reciben insulina usando monitoreo de glucosa (BGM) a controlar sus niveles de glucosa en sangre cuando sea apropiado en función de su terapia con insulina. Esto puede incluir el control en ayunas, antes de las comidas y meriendas, después de las comidas, a la hora de acostarse, antes del ejercicio, cuando se sospecha hipoglucemia, después de tratar los niveles bajos de glucosa en sangre hasta que sean normoglucémicos, cuando se sospecha hiperglucemia y antes y durante el ejercicio o tareas críticas como conducir. (B) 7.9 Aunque el BGM en personas que reciben terapias sin insulina no ha mostrado reducciones clínicamente significativas en la A1C de manera constante, puede ser útil cuando se modifica el plan de nutrición, la actividad física y/o los medicamentos (en particular, los medicamentos que pueden causar hipoglucemia) junto con un programa de ajuste del tratamiento. (E) |
|
Recomendaciones 7.11 Se debe ofrecer monitoreo de glucosa a través de sistemas (CGM) en tiempo real (rtCGM) (A) o CGM escaneado intermitentemente (isCGM) (B) para el control de la diabetes en adultos con diabetes que reciben múltiples inyecciones diarias (MDI) o CSII que son capaces de usar los dispositivos de manera segura (ya sea solos o con un cuidador). La elección del dispositivo debe hacerse en función de las circunstancias, preferencias y necesidades de la persona. 7.12 Se debe ofrecer rtCGM A o isCGM C para el control de la diabetes en adultos con diabetes que reciben insulina basal y que son capaces de usar los dispositivos de manera segura (ya sea solos o con un cuidador). La elección del dispositivo debe hacerse en función de las circunstancias, preferencias y necesidades de la persona. 7.15 En personas con diabetes en MDI o CSII, los dispositivos rtCGM deben usarse lo más cerca posible del día a día para obtener el máximo beneficio. Los dispositivos isCGM deben escanearse con frecuencia, como mínimo una vez cada 8 horas. A Las personas con diabetes deben tener acceso ininterrumpido a sus suministros para minimizar las brechas en CGM. (A) 7.17 El uso periódico de rtCGM o isCGM o el uso de CGM profesional puede ser útil para el control de la diabetes en circunstancias en las que el uso continuo de CGM no es apropiado, deseable o no está disponible. (C) 7.18 Las reacciones de la piel, ya sea por irritación o alergia, deben evaluarse y abordarse para ayudar en el uso exitoso de los dispositivos. (E) |
| Cuidado de paciente hospitalizado |
|
Recomendación 7.30 Las personas con diabetes que son competentes para usar de manera segura dispositivos para la diabetes, como bombas de insulina y sistemas CGM, deben recibir apoyo para continuar usándolos en un entorno de pacientes hospitalizados o durante procedimientos ambulatorios, una vez que se establezca la competencia y se disponga de la supervisión adecuada. (E) |
