La aprobación de VIZZ por la FDA constituye un avance terapéutico importante considerando las últimas décadas sin noticias en este campo de la oftalmología. Se trata de la primera formulación oftálmica basada en aceclidina aprobada para la indicación de presbicia.
A diferencia de tratamientos previos, como la pilocarpina HCl al 1,25 %, VIZZ actúa de manera selectiva sobre el músculo esfínter del iris, generando una miosis leve que produce el denominado "efecto estenopeico" (pinhole effect). Este mecanismo mejora la profundidad de foco sin inducir miopización ni afectar la visión a distancia.
Según LENZ Therapeutics, VIZZ se administra una vez al día y proporciona hasta 10 horas de mejora en la visión cercana. La eficacia para el tratamiento de la presbicia se demostró en dos estudios controlados, aleatorizados y doble ciego, CLARITY-1 y CLARITY-2.
En total, se aleatorizaron 466 participantes de 45 a 75 años con presbicia. Los participantes tenían un rango refractivo de -4,00 a +1,00 D en esfera, con astigmatismo de hasta 2,00 D, y un equivalente esférico no más miope que -4,00 D.
Ambos estudios incluyeron participantes que estaban poscirugía refractiva o pseudofáquicos. Se instruyó a los participantes que instilaran 2 gotas de VIZZ (o control) en cada ojo una vez al día, una gota en cada ojo seguida de una segunda gota en cada ojo dos minutos después. Los participantes fueron tratados durante 42 días. Se realizaron evaluaciones de la eficacia oftálmica en el Día 1, Día 15 y Día 28 del estudio en varios momentos a través de 10 horas después de la dosis.
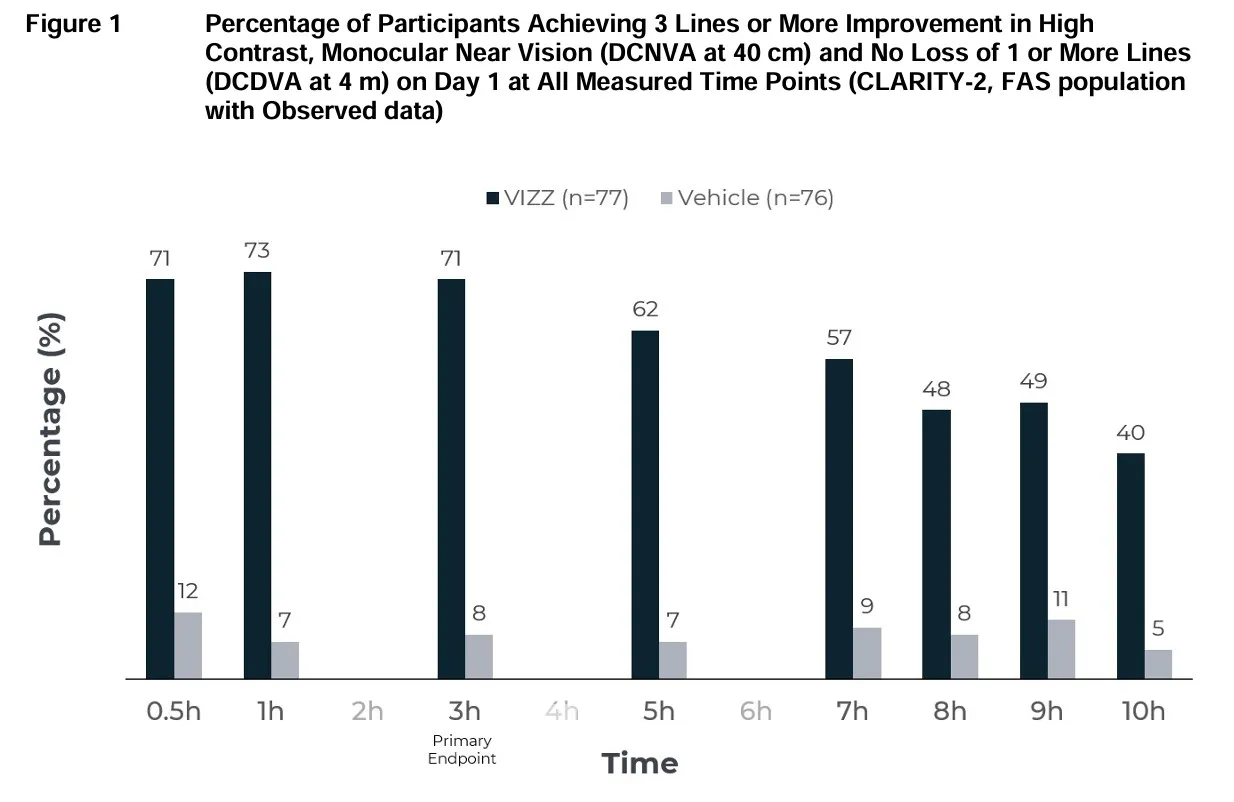
En cada estudio, la proporción de participantes que ganaron 3 líneas o más en la agudeza visual cercana corregida en alto contraste a 40 cm, sin perder 1 línea o más (≥5 letras) de agudeza visual corregida a distancia a 4 metros, fue estadísticamente mayor en el grupo VIZZ en comparación con el grupo de control en el Día 1.
El CEO de LENZ, Eef Schimmelpennink, destacó que "la aprobación de VIZZ representa un momento definitorio para la compañía y una mejora transformadora en las opciones terapéuticas disponibles para los adultos con presbicia". Asimismo, el investigador clínico Marc Bloomenstein, del Schwartz Laser Eye Care Center (Scottsdale, Arizona), señaló que "este tratamiento podría convertirse en el nuevo estándar de atención, dada su eficacia y perfil de seguridad".
La diferencia farmacodinámica entre aceclidina y pilocarpina es clave. Mientras que la segunda activa el músculo ciliar, lo que puede provocar efectos secundarios, como cefalea frontal o alteraciones vítreo-retinianas poco frecuentes, VIZZ evita esta estimulación, reduciendo el riesgo de miopización transitoria y otros efectos adversos.
La disponibilidad comercial de VIZZ está prevista para el cuarto trimestre de 2025 en Estados Unidos, posicionándose como el primer y único tratamiento aprobado por la FDA que utiliza aceclidina como agente miótico selectivo para la presbicia.
Este tipo de terapias tópicas representa una tendencia creciente en oftalmología, orientada a ofrecer soluciones no invasivas, reversibles y de acción rápida para condiciones visuales relacionadas con la edad.
Aunque los datos clínicos provienen de estudios patrocinados por la farmacéutica, se espera la publicación de resultados en revistas revisadas por pares en los próximos meses.