Un estudio reciente publicado en la revista Cell sugiere que dos fármacos utilizados en oncología —letrozol para cáncer de mama e irinotecán para cáncer de colon y de pulmón— podrían revertir algunos de los cambios moleculares y funcionales asociados al alzhéimer, incluso restaurando capacidades cognitivas en modelos animales.
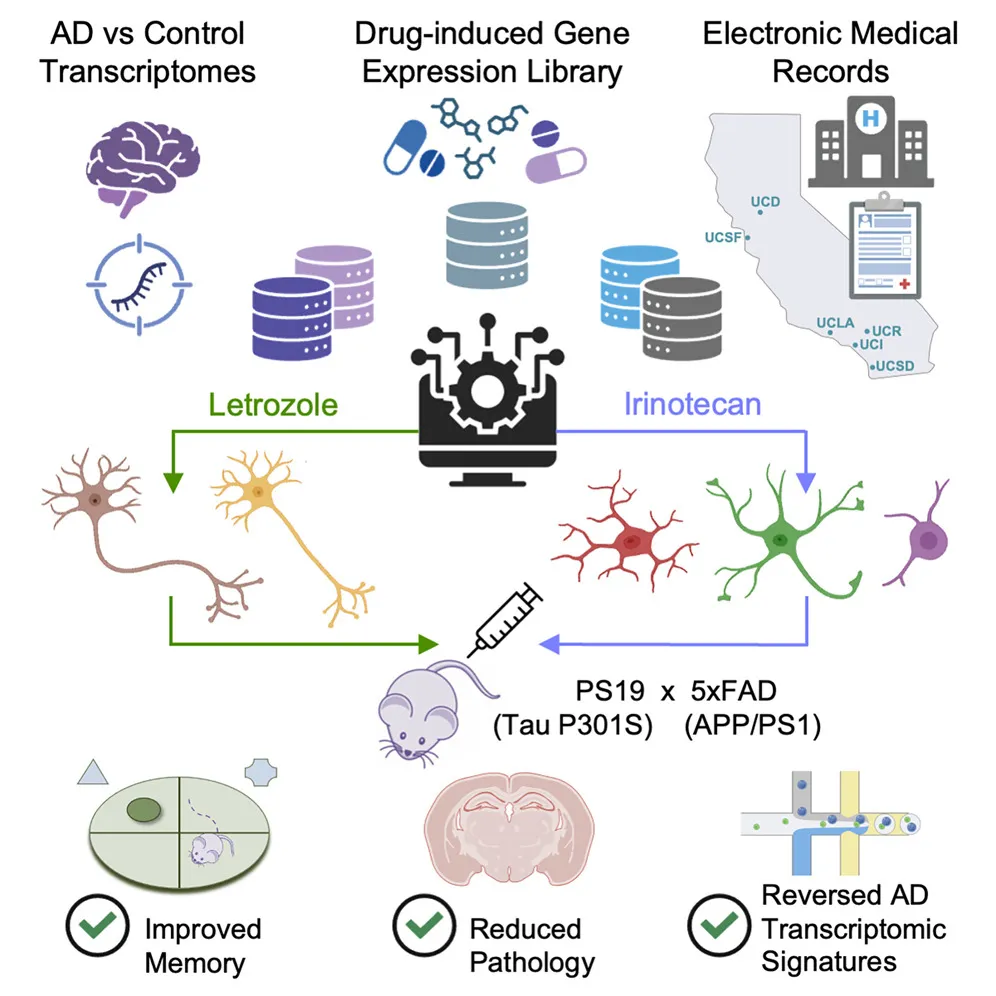
El equipo de investigación, liderado por la Dra. Marina Sirota (UCSF) y el Dr. Yadong Huang (Gladstone Institutes), empleó un enfoque computacional para comparar las firmas de expresión génica de células cerebrales afectadas por la enfermedad con los efectos de más de 1300 fármacos aprobados por la FDA. El objetivo era identificar aquellos compuestos capaces de invertir los patrones de expresión génica alterados en neuronas y células gliales.
Mediante el análisis de datos de expresión génica a nivel de célula única —obtenidos de cerebros de donantes con y sin alzhéimer— y su cruce con la base de datos Connectivity Map, los científicos identificaron 86 fármacos que revertían las alteraciones en al menos un tipo celular. De estos, solo 10 estaban ya aprobados para uso clínico en humanos. Posteriormente, al examinar registros médicos electrónicos de 1,4 millones de personas mayores de 65 años, observaron que algunos de estos fármacos se asociaban con un menor riesgo de desarrollar alzhéimer en pacientes que los recibían por otras indicaciones.
Los investigadores seleccionaron los dos fármacos con mayor potencial: letrozol, que actuaría principalmente en neuronas, e irinotecán, con efectos beneficiosos en células gliales. Para evaluar su eficacia, utilizaron un modelo murino de alzhéimer agresivo, con múltiples mutaciones relacionadas con la enfermedad. Los resultados fueron prometedores:
- La combinación de ambos fármacos revirtió las firmas de expresión génica alteradas por la enfermedad.
- Se redujo la formación de agregados tóxicos de proteínas (como la beta-amiloide y tau hiperfosforilada).
- Disminuyó la degeneración cerebral y, lo más relevante, se restauró la memoria en los animales tratados.
"Es emocionante ver cómo datos computacionales independientes, como los de expresión génica y registros clínicos, nos llevan a los mismos mecanismos y fármacos, y luego validarlos en un modelo genético. Esto sugiere que estamos en el camino correcto”, señaló la Dra. Sirota.
El alzhéimer se considera una enfermedad multifactorial, con alteraciones en múltiples genes y proteínas que, en conjunto, comprometen la salud cerebral. Tradicionalmente, el desarrollo de fármacos se ha centrado en blancos únicos, lo que explica en parte los repetidos fracasos terapéuticos.
En cambio, esta estrategia aprovecha el efecto pleiotrópico de los fármacos oncológicos, capaces de modular vías biológicas compartidas entre el cáncer y las enfermedades neurodegenerativas, como la inflamación crónica y el estrés oxidativo, la disfunción mitocondrial y el metabolismo energético alterado, la acumulación de proteínas mal plegadas y los fallos en su degradación.
El letrozol, un inhibidor de la aromatasa, podría actuar reduciendo la neuroinflamación, mientras que el irinotecán —un inhibidor de la topoisomerasa I— interferiría con la proliferación celular aberrante y la respuesta al daño del ADN, procesos también implicados en la patogénesis de la enfermedad.
Los investigadores destacan el potencial del reposicionamiento de fármacos (drug repurposing), una estrategia que acelera la traducción clínica al evitar las fases iniciales de desarrollo preclínico. Si estos resultados se confirman en humanos, podríamos tener una terapia combinada lista para millones de pacientes en un plazo relativamente corto.
No obstante, se requieren ensayos clínicos controlados para evaluar la seguridad y eficacia en pacientes humanos, especialmente considerando los posibles efectos adversos de fármacos citotóxicos en una población frágil. Además, será clave determinar las dosis óptimas y la duración del tratamiento, así como identificar biomarcadores que permitan seleccionar a los pacientes con mayor probabilidad de respuesta.
En contexto, el hallazgo se suma a una creciente evidencia que vincula mecanismos oncogénicos con enfermedades neurodegenerativas. Por ejemplo, vías como mTOR, p53 y Wnt/β-catenina, hiperactivadas en cáncer, también están desreguladas en el alzhéimer. Otros estudios previos han explorado el uso de fármacos antineoplásicos —como los inhibidores de HDAC o los agentes alquilantes— en modelos de demencia, aunque con resultados menos prometedores.
Li Y, Sirota M, Huang Y, et al. Cell-type-directed network-correcting combination therapy for Alzheimer’s disease. Cell. 2025; DOI: 10.1016/j.cell.2025.06.035.