Leucemia linfocítica crónica
| Introducción |
Leucemia linfocítica crónica (LLC) es la leucemia adulta más común en el mundo occidental. Su complejidad ha aumentado sustancialmente en los últimos años como consecuencia del advenimiento de nuevos agentes biológicos, la identificación de marcadores predictivos moleculares, y la introducción de técnicas más sensibles y sofisticadas para evaluar la enfermedad residual mínima.
| Epidemiología |
En el mundo occidental, la LLC representa casi el 25% de todas las leucemias y el 1,3% de todos los cánceres. Su incidencia es sustancialmente menor entre las personas asiáticas y más elevada entre los judíos Ashkenazi.
Se estima que su incidencia continuará su tendencia ascendente. Afecta sobre todo a personas mayores, (más del 70% son >65 años; la mediana de la edad en el momento del diagnóstico es 72 años). Los hombres y las personas de raza blanca son más frecuentemente afectados que las mujeres y otras razas.
| Etiología |
Se piensa que existe una predisposición genética para la LLC, con mayor prevalencia entre los familiares de pacientes con LLC esporádica, y se conocen hasta 6 polimorfismos de nucleótidos únicos que confieren mayor riesgo de desarrollar LLC.
Recientemente, un estudio de secuenciación de todo el genoma informó que las mutaciones de la LLC pueden atribuir a 3 procesos de mutación clave: 2 tipos de firmas de deaminasa de citidina inducida por la activación e y una firma genética del envejecimiento, que funcionan en diferentes momentos, a lo largo de la evolución de la LLC.
La frecuencia de la LLC aumenta progresivamente con la edad, lo que sugiere que también la exposición persistente a un antígeno del envejecimiento propio o no propio puede ser un factor predisponente.
Se destaca que, entre los pacientes con hepatitis C, la incidencia de LLC es significativamente mayor que en la población general. Aunque las personas que viven en granjas o expuestas al Agente Naranja están en mayor riesgo de desarrollar LLC y la exposición al sol protege su inicio, nunca se ha comprobado una clara asociación entre la LLC y la exposición a la radiación ionizante.
| Presentación clínica |
Los pacientes con LLC tienen presentaciones clínicas variadas. La mayoría son asintomáticos y la LLC es diagnosticada solo por un hallazgo incidental de linfocitosis en un hemograma, que puede ir acompañada, en un grado variable, con anemia y/o trombocitopenia.
En algunos casos, los pacientes también pueden tener linfadenopatías palpables y/o hepatoesplenomegalia, que en casos raros puede provocar síntomas secundarios a una compresión local.
Las presentaciones extraganglionares y/o extramedulares son raras, siendo más frecuente la participación de la piel y del sistema nervioso central.
Una minoría de pacientes presentará síntomas constitucionales, como fiebre persistente, sudores nocturnos, y/o pérdida de peso involuntaria, mientras que la fatiga es un síntoma común.
Finalmente, la LLC puede diagnosticarse como consecuencia de la aparición de signos y síntomas clínicos secundarios a sus complicaciones y no por su participación directa, incluyendo las enfermedades autoinmunes, las infecciones o segundos cánceres.
| Diagnóstico |
La biopsia de la médula ósea no es necesaria para diagnosticar la LLC, pero se puede hacer cuando existe anemia y/o trombocitopenia
El diagnóstico de LLC requiere la presencia de al menos 5 × 109/ de linfocitos B en la sangre periférica y de una población clonal de células B, detectada por citometría de flujo, positiva para la restricción de cadenas ligeras (kappa o lambda), CD5, CD23, CD79b y, la expresión de inmunoglobulina de superficie y bajos niveles de CD20.
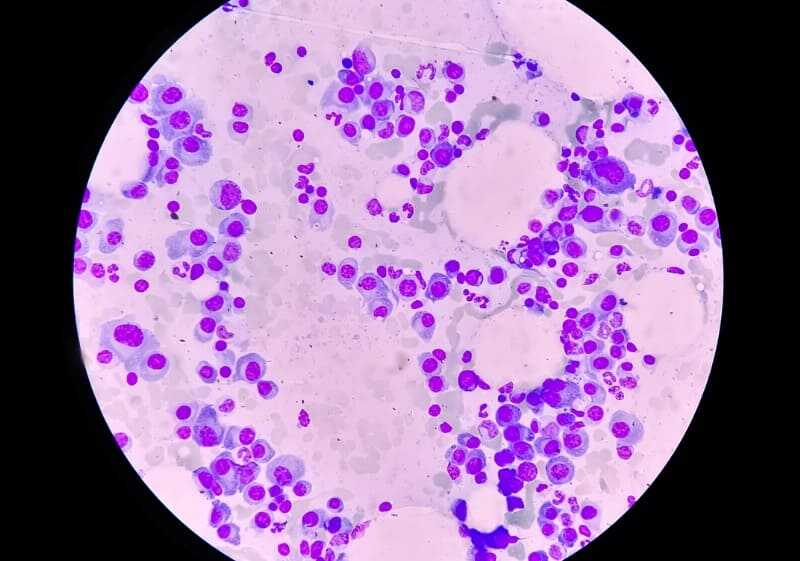
Al examen microscópico simple, las células tienen un aspecto típico de células manchadas, que corresponden a artefactos de los linfocitos dañados durante la preparación de la diapositiva.
Raramente, las células de la LLC pueden tener una morfología atípica definida, como más del 15% de células con núcleos hendidos y/o características linfoplasmocitoides, y un inmunofenotipo atípico, con un puntaje modificado de Matutes <4 (basado en la expresión atípica de CD5, CD23, FMC7, inmunoglobulina de superficie, CD22, y/o CD79b); esta entidad a veces es denominada LLC atípica o variante.
Las principales entidades que deberían ser incluidas en el diagnóstico diferencial de la LLC son el linfoma de células del manto (LCM), el linfoma de la zona marginal esplénica, y la leucemia prolinfocítica de células B. La detección de t(11;14) mediante la hibridación fluorescente in situ (FISH, del inglés)) permite diferenciar la LCM de la LLC.
A diferencia de esta última, el linfoma del margen esplénico, rara vez es positivo para CD23, mientras que puede ser positivo para CD5 en el 5% a 10% de los casos, e invariablemente nunca involucra la médula ósea,
Finalmente, la leucemia prolinfocítica de células B se presenta con >55% de prolinfocitos en la sangre periférica y es CD5 positiva, pero CD23 negativa. Es raro que las características de otros trastornos linfoproliferativos se superpongan a la LLC.
Cuando se detecta una población clonal de células B en los ganglios linfáticos agrandados, en ausencia de linfocitos clonales periféricos, el término que debe usarse es el de linfoma linfocítico pequeño, identificando a una variante clínica de la misma entidad histopatológica.
La presencia de una población clonal de células B en sangre periférica <5 × 109/l de células B y ningún otro signo de un trastorno linfoproliferativo identifica a una tercera entidad denominada linfocitosis monoclonal de células B.
La biopsia de la médula ósea no es necesaria para diagnosticar la LLC, pero se puede hacer cuando existe anemia y/o trombocitopenia, para diferenciar entre la autoinmunidad y la mieloptisis, con implicancias terapéuticas.
| Pronóstico |
Dada la gran heterogeneidad de las manifestaciones clínicas de la LLC, se ha intentado identificar factores pronósticos, con el fin de asesorar mejor a los pacientes. La primera herramienta pronóstica fue proporcionada hace más de 4 décadas por Rai y Binet, quienes desarrollaron 2 sistemas de estadificación separados que hoy llevan sus nombres basados en parámetros clínicos simples, como el recuento completo de las células sanguíneas y el examen físico.
Las 5 etapas identificadas por Rai y las 3 identificadas por Binet se asocian claramente con diferentes resultados clínicos. Más tarde, se establecieron otros parámetros fácilmente medibles, como la duplicación en el tiempo del recuento absoluto de linfocitos y el patrón de invasión de la médula ósea, pero su poder es limitado.
| Sistemas de estadificación de Rai y Binet para la leucemia linfática crónicaa | |
| Estadios Rai | Estadios Binet |
| 0 Solo linfocitosis | A <3 linfadenopattías |
| I Linfadenopatías | B ≥3 linfadenopatías |
| II Esplenomegalia o hepatomegalia | |
| III Anem ia (Hb <11g/dl) | C Hemoglobina <11g/dl) y/o recuento de plaquegtas <100 × 109/l |
| IV Trombocitopenia (recuento de plaquegtas <100 × 109/l) | |
| aFactores de conversión SI: para convertir valores de Hb a g/l multiplicar por 100 | |
Las técnicas más nuevas, como los ensayos inmunoenzimáticos, la citometría de flujo, la citogenética y la biología molecular han brindado marcadores pronósticos más confiables.
Los parámetros séricos medidos mediante el análisis inmunoenzimático simple, incluyen la b2-microglob47ulina (B2M) y los niveles de timidinacinasa.
Un nivel de B2M >3,5 mg/l y un nivel de timidinacinasa >8,5 U/l se asocian con una carga mayor de la enfermedad y una supervivencia más corta.
Los 3 marcadores pronósticos más comúnmente empleados basados en la citometría de flujo son la expresión de CD38, ZAP70 (que son proteínas involucradas en la señalización del receptor de células B) y CD49d (una integrina de superficie). Su expresión es un factor independiente que se relaciona con una supervivencia más corta. Se destaca que CD49d también puede estar asociado a linfadenopatías.
Dado que la tasa mitótica celular en la LLC es baja, a diferencia del análisis de bandas cromosómicas convencional, la FISH es la técnica más común para evaluar las aberraciones genéticas recurrentes en estos pacientes.
Los pacientes con deleción 17p y/o eliminación 11q experimentan un curso clínico más agresivo que los pacientes con deleción 13q, trisomía 12, o ninguna anormalidad de la FISH. Por otra parte, deleción 11q y la trisomía 12 también se asocian con linfadenopatía, y la trisomía 12 puede aumentar el riesgo de síndrome de Richter y segundos cánceres.
A pesar de sus limitaciones, últimamente el análisis citogenético convencional ha recuperado importancia pronóstica para la LLC, mostrando que los cariotipos complejos se asocian con peores resultados, incluyendo un riesgo mayor de síndrome de Richter. Las aberraciones genómicas también pueden detectarse mediante técnicas basadas en la reacción en cadena de la polimerasa.
Los receptores de células B raramente son evaluados en la práctica clínica. Se ha intentado integrar a todos los factores pronósticos antes descritos en un único puntaje pronóstico.
Una revisión sistemática y un metaanálisis han informado que la evidencia publicada es suficiente para recomendar el FISH y el análisis del gen variable de inmunoglobulina de cadenas pesadas (IGHV, del inglés) como pruebas clínicas estándar para todos los pacientes con LLC recién diagnosticada.
Por otra parte, se ha formulado un índice pronóstico internacional en base a la edad, los niveles de B2M, el estadio Rai, la presencia de 17p (o de la mutación TP53) detectada por FISH y el estado mutacional IGHV62. Sin embargo, en las guías aún no se recomienda utilizar el puntaje pronóstico, ya que no contempla las comorbilidades, un factor importante en el curso clínico de los pacientes con LLC, dado la mediana de la edad en el momento del diagnóstico (72 años). Además del pronóstico, muchos de estos marcadores también pueden tener un valor predictivo y guiar las decisiones terapéuticas.
| Indicaciones para el tratamiento |
No todos los pacientes con LLC requieren tratamiento en el momento del diagnóstico, y la mayoría puede someterse a una vigilancia activa durante muchos años antes de requerir un tratamiento. Las indicaciones se basan principalmente en 3 elementos: síntomas, hemograma completo y hallazgos del examen físico.
| Indicaciones para iniciar el tratamiento de la leucemia linfática crónica |
| Indicaciones terapéuticas |
| • Síntomas constitucionales progresivos • Insuficiencia progresvia de la médula ósea: anemia y/o trombocitopenia • Linfadenopatías progresivas (al menos 10 cm) • Hepatomegalia o esplenomegalia progresivas • Linfocitosis progresiva (tiempo de duplicación <6 meses) • Anemia hemolítica autoinmune refractaria a los esteroides y/o trombocitopenia inmunológica |
Los síntomas constitucionales, definidos como fiebre persistente e inexplicable (temperatura >38°C) y/o pérdida de peso (>10% del peso base en el transcurso de menos de 6 meses) y/o sudores nocturnos severos, pueden representar una primera indicación para el tratamiento.
La linfocitosis progresiva, la hemoglobina <10 g/dl o un recuento de plaquetas <100 ×n 109/l representan otra indicación de tratamiento. Se destaca que, en lugar del número absoluto de linfocitos, las guías recomiendan la duplicación de los linfocitos en el tiempo (la duplicación rápida es cuando ocurre en menos de 6 meses).
Por otra parte, en presencia de anemia y/o trombocitopenia, siempre se debe descartar una etiología autoinmune, y solo la anemia hemolítica autoinmune refractara y/o la púrpura trombocitopénica idiopática requieren una pronta iniciación de la terapia específica para la LLC. Finalmente, el tratamiento está recomendado en presencia de linfadenopatía progresiva y/o sintomática (>10 cm) y/o hepatoesplenomegalia.
Es importante destacar que la falta de datos para apoyar la intervención temprana deriva de la era quimioinmunoterapéutica; hay varios ensayos en curso dirigidos a esclarecer este dogma, particularmente en relación con los pacientes de alto riesgo, utilizando agentes nuevos menos tóxicos, como el ibrutinib.
| Evaluación de la respuesta |
La evaluación de la respuesta sigue los lineamientos emitidos por las guías de 2008, aunque su calendario y la validez pueden ser cuestionados por el advenimiento de nuevos agentes biológicos.
Según la experiencia de la era de la quimioinmunoterapia, la respuesta debe evaluarse 2 a 3 meses después de finalizada la terapia y debe basarse en el recuento completo de células sanguíneas, los hallazgos del examen físico y de la biopsia de médula ósea; no se recomienda la tomografía computarizada fuera de los ensayos clínicos.
Es interesante que el beneficio de la remisión clínica completa con la recuperación incompleta de la médula ósea parece ser comparable al de la remisión completa. Si se cumplen los criterios de resolución completa pero la médula ósea incluye nódulos linfocíticos, el término recomendado es remisión parcial nodular, y el pronóstico es más parecido al de la remisión parcial.
En los últimos años, ha ganado cada vez más importancia la erradicación de la enfermedad residual mínima, medida por citometría de flujo de 4 colores, con una sensibilidad <0,01%.
En particular, la negativización de la enfermedad residual mínima después de la quimioinmunoterapia ha sido prospectivamente asociada con una supervivencia libre de progresión prolongada y una supervivencia general con evidencia retrospectiva de que la erradicación temprana puede dar lugar a la interrupción del tratamiento.
Sin embargo, aún no se han obtenido datos similares con agentes más nuevos como el ibrutinib, el idelalisib y el venetoclax. Las guías estándar no recomiendan el monitoreo y el éxito de la enfermedad residual mínima.
| Tratamiento |
En los últimos años, el tratamiento de la LLC ha avanzado mucho, pero todavía no se ha alcanzado un manejo óptimo de los pacientes de alto riesgo, en particular los que padecen la enfermedad recidivante, que tienen deleción 17p.
Comentarios
Para ver los comentarios de sus colegas o para expresar su opinión debe ingresar con su cuenta de IntraMed.