Tiroidectomía robóticamente asistida vs. endoscópica convencional
Introducción
La tiroidectomía convencional abierta utilizando un abordaje directo a través del cuello, brinda un medio efectivo y seguro para el manejo quirúrgico de la enfermedad de la glándula tiroides, pero deja una cicatriz perceptible en un área altamente visible [1]. Dado que la incidencia de la patología tiroidea es alta en las mujeres, y que ha aumentado la necesidad de mejorar la calidad de vida postoperatoria, se han hecho muchos esfuerzos para eliminar la cicatriz visible en el cuello [2-23]. Después de que Garnier describiera por primera vez la cirugía endoscópica del cuello en 1996, los procedimientos endoscópicos basados en varios abordajes, han sido ampliamente aplicados para minimizar las cicatrices [2-18,24]. La adopción de un procedimiento endoscópico, brinda una mejor apariencia cosmética y ofrece varias ventajas extras, por ejemplo, disminución de la hiperestesia o parestesia en la cara anterior del cuello y menor malestar durante la deglución al evitar la incisión transversal transversa [2,4-18]. Como resultado de esos beneficios, la tiroidectomía endoscópica es considerada por muchos cirujanos, como una buena opción de tratamiento para la enfermedad tiroidea benigna [2-5,7,8,10,11,13,16,18,22,23].
Recientemente, algunos investigadores aplicaron la tiroidectomía endoscópica en pacientes con carcinoma de tiroides, con pronóstico favorable [4,6-9,13-15,17,23]. Después de probar la factibilidad de la tiroidectomía endoscópica en casos seleccionados, sugirieron cuidadosamente a la tiroidectomía endoscópica, como una opción de tratamiento en pacientes con carcinoma tiroideo bien diferenciado, de bajo riesgo [4,6-9,13-15,17,23].
Sin embargo, a pesar de sus ventajas, la tiroidectomía endoscópica tiene algunas limitaciones técnicas, que comparte con muchos otros tipos de cirugía mínimamente invasiva [19-21,25,26], Los instrumentos endoscópicos rígidos, rectos, sin articulaciones y una visión bidimensional (2-D), son radicalmente diferentes de la situación en la cirugía convencional, realizada por exquisitas manos de cirujano [6,8,19-21,23,25,26], Asimismo, particularmente en el área de cabeza y cuello, el espacio de trabajo durante la cirugía endoscópica es estrecho y confinado [3,6,7,23].
En muchos campos, los cirujanos han introducido técnicas robóticas para procedimientos mínimamente invasivos y han superado gradualmente esas limitaciones [19-21,25,26], La reciente introducción del sistema quirúrgico robótico da Vinci (Intuitive, Inc., Sunnyvale, CA) en la tiroidectomía endoscópica, mejoró la destreza instrumental y le brindó al cirujano un sistema operatorio ergonómicamente diseñado [19-21,25,26].
El objetivo de este estudio fue demostrar la superioridad y excelencia de la cirugía tiroidea robótica mediante la comparación de los resultados quirúrgicos tempranos de la tiroidectomía endoscópica asistida robóticamente, versus la tiroidectomía endoscópica convencional utilizando un abordaje transaxilar sin aire, en el microcarcinoma tiroideo papilar (MCTP).
Pacientes y métodos
Pacientes
Desde noviembre de 2001 hasta julio de 2009, 1.489 pacientes con carcinoma tiroideo papilar fueron sometidos a cirugía tiroidea endoscópica, utilizando un abordaje transaxilar, sin gas, en el Departamento de Cirugía del Yonsei University Medical Center. La tiroidectomía endoscópica convencional fue introducida por primera vez en noviembre de 2001 y la tiroidectomía robóticamente asistida en octubre de 2007 [6,8,13,19-21].
Las seguridades oncológicas de los procedimientos endoscópicos convencionales y robóticos no han sido completamente establecidas y, en consecuencia, los candidatos fueron limitados al carcinoma tiroideo bien diferenciado, con bajo riesgo [6,8,13,19-21].
Las evaluaciones preoperatorias de los nódulos tiroideos fueron hechas mediante biopsia con aguja fina (BAF), estadificación ecográfica de alta resolución y tomografía computada (TC) de cuello. El examen ecográfico incluyó ambos lóbulos tiroideos y todos los niveles del cuello (I-VI) [27]. En todos los pacientes se diagnosticó preoperatoriamente un carcinoma tiroideo papilar bien diferenciado. El tamaño de los tumores, invasión extratiroidea, infiltración tumoral de las estructuras adyacentes y compromiso ganglionar, fueron evaluados mediante ecografía preoperatoria [27]. Un hallazgo ecográfico, tal como la pérdida de ecogenicidad de la cápsula tiroidea en el sitio de contacto del tumor primario, o el contacto con la cápsula tiroidea adyacente a lo largo de más del 25% del perímetro de un tumor, indicaron extensión extratiroidea [27].
Los casos de MCPT (tamaño del tumor ≤ 1,0 cm) sin invasión tumoral extratiroidea definida, fueron enrolados en este estudio. Los casos con múltiples metástasis ganglionares laterales en el cuello, infiltración periganglionar en un ganglio linfático metastático o con metástasis a distancia, fueron excluidos. Los casos con un tumor localizado en el área tiroidea dorsal (particularmente en la muesca traqueo-esofágica) con invasión capsular posterior o extensión a una estructura adyacente, también fueron excluidos, debido a la posible lesión de la tráquea, esófago o nervio laríngeo recurrente (NLR), durante el procedimiento.
Desde noviembre de 2001 a julio de 2009, 706 pacientes fueron tratados con tiroidectomía endoscópica convencional y, de ellos, 570 pacientes con MCTP fueron enrolados en este estudio (grupo endoscópico convencional: GE). Desde octubre de 2007 a julio de 2009, se efectuó la tiroidectomía endoscópica robóticamente asistida en 783 pacientes, utilizando el sistema robótico da Vinci y 580 de esos pacientes con MCTP fueron también enrolados (grupo robótico: GR).
La extensión de la tiroidectomía se determinó de acuerdo con las guías establecidas por la American Thyroid Association. Los pacientes con lesiones múltiples, lesiones bilaterales, invasión capsular tiroidea durante la cirugía, antecedentes de radioterapia de cabeza o cuello, o antecedentes familiares de primer grado de cáncer tiroideo, fueron sometidos a tiroidectomía total. La disección profiláctica ipsilateral del compartimiento central del cuello fue realizada en todos los pacientes. En los pacientes con un ganglio linfático lateral en el cuello con sospecha de metástasis, se realizó una disección ganglionar linfática selectiva. Los pacientes con biopsia por congelación negativa fueron incluidos, pero aquellos sometidos a una disección radical modificada del cuello combinada, debido a las metástasis en los ganglios laterales, fueron excluidos.
A todos los pacientes se les administró levotiroxina para la supresión de la hormona estimulante tiroidea (TSH por thyroid stimulating hormone), inmediatamente después de la cirugía. A los pacientes con indicación de terapia con iodo radioactivo, se los sometió al procedimiento a las 4 a 6 semanas después de la tiroidectomía total. Los niveles de tiroglobulina sérica fueron controlados y se efectuó una ecografía cada 3 o 6 meses.
Métodos operatorios
Los procedimientos utilizados en los 2 grupos fueron idénticos hasta la colocación del retractor externo para mantener un espacio de trabajo adecuado. Los autores han descrito previamente ambos procedimientos en detalle [6,8,13,19-21].
El paciente fue colocado en posición supina con el cuello levemente extendido. El brazo del lado de la lesión es elevado dentro del rango de movilidad del hombro, para evitar la parálisis del plexo braquial. El brazo es fijado para lograr la distancia más corta entre la axila y la cara anterior del cuello. Después de realizar una incisión vertical de 5 a 6 cm, a lo largo del borde lateral del músculo pectoral mayor en la axila, se preparó un colgajo de piel subplatismal desde la axila al cuello anterior, a través de la bifurcación del músculo esternocleidomastoideo (ECM). El retractor externo es colocado después de levantar el colgajo muscular hasta visualizar la tiroides contralateral.
Procedimiento endoscópico
Después de colocar el retractor externo, se efectúa una segunda incisión en piel (0,5 cm de longitud) sobre el lado medial de la pared torácica anterior, justo por debajo de la cabeza de la clavícula y lateral a la cabeza esternal del músculo ECM, para la inserción del material endoscópico. Luego se coloca una cámara endoscópica de 45º en extremo cefálico de la incisión axilar. Mientras un asistente sostiene la cámara, la glándula tiroidea es retraída utilizando instrumentos endoscópicos. La glándula tiroidea es retraída y disecada utilizando un disector endoscópico y un bisturí armónico Harmonic Scalpel (Johnson & Johnson Medical, Cincinnati, OH), que permiten que el cirujano use ambas manos. Los detalles del procedimiento endoscópico convencional fueron descritos en reportes previos de los autores [6,8,13] (Figs. 1A, B).
• FIGURA 1, A, B. Tiroidectomía endoscópica convencional
Procedimiento robótico
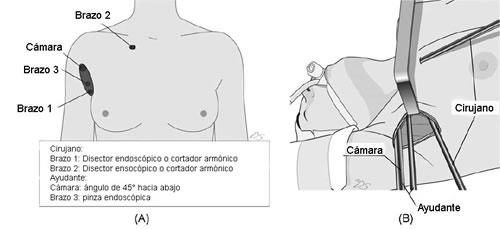
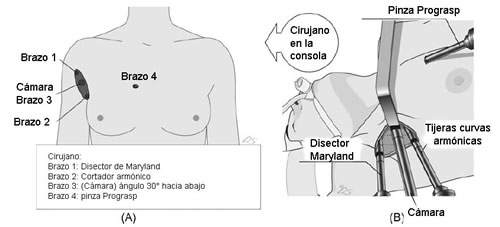
Se realiza una segunda incisión en piel de 0,8 cm para la inserción de los 4 brazos robóticos, sobre la pared torácica anterior, del lado del tumor (2-4 cm superiormente y 6-8 cm medialmente al pezón y lejos del esternón). El atraque robótico se realiza después de colocar el retractor externo. Un telescopio de 30º de doble canal, controlado por el cirujano, se coloca luego en el centro de la incisión. Un disector de Maryland y tijeras curvas conectadas al bisturí armónico (ambos de Intuitive Surgical) son colocados después en ambos extremos laterales de la incisión axilar. Una pinza Prograsp (Intuitive Surgical) es insertada luego, a través de una segunda incisión. en la pared anterior del tórax y colocada lateralmente a la rama esternal del músculo ECM. La glándula tiroides es retraída utilizando una pinza Prograsp en el 4º brazo robótico y la disección es realizada utilizando una tijera curva armónica y un disector de Maryland. Este procedimiento le permite al cirujano usar 3 brazos robóticos durante la tiroidectomía robóticamente asistida. Los detalles del procedimiento robótico fueron descritos en reportes previos de los autores [19-21] (Fig. 2A, B).
• FIGURA 2, A, B. Tiroidectomía robóticamente asistida
Análisis estadístico
Las características clínico-patológicas, resultados quirúrgicos, tales como tiempos operatorios, estadía hospitalaria postoperatoria, número de ganglios linfáticos recuperados, complicaciones postoperatorias y completitud quirúrgica, y los tipos de operación en los 2 grupos, fueron comparados retrospectivamente.
Los datos continuos, cuantitativos, son expresados como medias ± desvío estándar y los datos categóricos, cualitativos, como frecuencias y porcentajes. Los grupos fueron comparados utilizando la prueba de x2, la de U de Mann-Whitney, la de t de Student o la exacta de Fisher, para las variables cualitativas o cuantitativas, según lo apropiado. Los valores de P < 0,05 fueron considerados estadísticamente significativos. Todos los análisis estadísticos fueron realizados utilizando el programa SPSS, versión 15.0 (SPSS, Chicago, IL).
Resultados
Las características clínicas de los 2 grupos se muestran en la Tabla 1. La edad media fue más baja en el GE que en el GR (38,5 ± 9,2 años en GE y 40,3 ± 9,5 años en el GR, P = 0,001). Los tipos de operaciones realizadas fueron también significativamente diferentes en los 2 grupos. Menos que una tiroidectomía total fue efectuado en 499 pacientes (87,5%) en el GE y en 445 pacientes (76,7%) en el GR. La tiroidectomía total fue realizada en 71 pacientes (12,5%) en el GE y en 135 pacientes (23,3%) en el GR y, por lo tanto, la tiroidectomía total fue efectuada significativamente más frecuentemente en el GR (P < 0,001). No hubo casos de conversión en cada grupo. Las estadías hospitalarias postoperatorias no fueron significativamente diferentes.
• TABLA 1: Características clínicas de los pacientes en los 2 grupos del estudio
| Tiroidectomía endoscópica convencional (n = 570) |
Tiroidectomía endoscópica robóticamente asistida (n = 580) |
P | |
| Edad (años) | 38,5 ± 9,2 | 40,3 ± 9,5 | 0,001 |
| Relación de género (M:F) | 15:555 (1:37) | 39:541 (1:13,9) | 0,001 |
| Tipo de operación Menos que tiroidectomía total Tiroidectomía total |
499 (87,5%) 71 (12,5%) |
445 (76,7%) 135 (23,3%) |
< 0,001 |
| Estadía hospitalaria (días) | 3,4 ± 2,8 | 3,3 ± 0,8 | 0,241 |
| Tiempo de atraque (minutos) | - | 5,6 ± 2,7 | |
| Tiempo total de operación (min) - Menos que tiroidectomía total - Tiroidectomía total |
127,1 ± 40,8 158,4 ± 50,5 |
126,8 ± 34,5 151,7 ± 35,4 |
0,907 0,268 |
| Tiempo real de operación (min) Menos que tiroidectomía total Tiroidectomía total |
127,1 ± 40,8 158,4 ± 50,5 |
121,6 ± 34,1 146,7 ± 34,5 |
0,028 0,052 |
| Recuperación de ganglios centrales (N) | 3,6 ± 3,2 | 4,3 ± 3,6 | < 0,001 |
Los tiempos operatorios totales fueron similares en los 2 grupos (P = 0,907 para menos que una tiroidectomía total y P = 0,268 para la tiroidectomía total). No obstante, los tiempos operatorios difirieron en el armado en los 2 grupos. El “tiempo de atraque” requerido para la cirugía robótica fue de 5,6 ± 2,7 minutos y, cuando fue excluido, el “tiempo operatorio real”, esto es, el tiempo pasado por el cirujano, fue significativamente más corto en el GR en los casos de menos que una tiroidectomía total (127,1 ± 40,8 minutos en GE vs. 121,6 ± 34,1 minutos en GR; P = 0,028).
Asimismo, para la tiroidectomía total, el tiempo real de operación tendió a ser más corto en el GR (158,4 ± 50,5 minutos en GE vs. 146,7 ± 34,5 minutos en GR; P = 0,052). Finalmente, el número de ganglios centrales recuperados fue significativamente mayor en el GR (3,6 ± 3,2 vs. 4,3 ± 3,6; P < 0,001).
Los 2 grupos fueron comparados también en términos de características histopatológicas (Tabla 2). Los tamaños tumorales medios en el GE y en el GR fueron 0,56 ± 0,20 cm y 0,58 ± 0,21 cm, respectivamente, lo que no fue significativamente diferente (P = 0,082). Las metástasis en los ganglios centrales (P = 0,003) y la invasión capsular (P = 0,014) fueron más frecuentes en el GR, pero la multiplicidad (P = 0,115) y bilateralidad (P = 0,281) fueron similares en ambos grupos. Un estadio tumoral avanzado (lesión T3) fue más frecuente en el GR (P = 0,046). Dos pacientes tuvieron una lesión T4a en ambos grupos. En el GE, un caso mostró adherencia traqueal con sospecha de invasión traqueal durante la inspección macroscópica, lo que no había sido sugerido por los estudios por imágenes preoperatorios. La tráquea fue desgarrada durante la disección con un coagulador ultrasónico y seguidamente reparada mediante la sutura primaria endoscópica, sin filtración aérea postoperatoria. En otros 2 casos (1 en GE y 2 en GR) se observó la invasión del tumor al NLR, lo que no había sido sugerido preoperatoriamente por la ecografía. Los 3 casos fueron tratados mediante el rasurado del nervio y sólo 1 paciente mostró ronquera transitoria en el GR y ninguno experimentó parálisis permanente del nervio. Los estadios TNM fueron más avanzados en el GR (P = 0,009).
• TABLA 2: Características histopatológicas de los 2 grupos del estudio
| Tiroidectomía endoscópica convencional |
(n = 570) Tiroidectomía |
P |
|
| Tamaño del tumor (cm) | 0,56 ± 0,20 | 0,58 ± 0,21 | 0,082 |
| Metástasis ganglionar central No Si |
|
409 (70,5%) 171 (29,5%) |
0,003 |
| Invasión capsular No Si |
365 (64,0%) 205 (36,0%) |
330 (56,9%) 250 (443,1%) |
0,014 |
| Multiplicidad No Si |
472 (82,8%) 98 (17,2%) |
459 (78,1%) 121 (43,1%) |
0,115
|
| Bilateralidad No Si |
529 (92,8%) 41 (7,2%) |
|
0,281 |
| Estadio T 1 3 4ª |
365 (64,0%) 203 (35,6%) 2 (0,4%) |
|
0,046 |
| Estadio N 0 1a |
446 (78,2%) 124 (21,8%) |
409 (70,5%) 171 (29,5%) |
0,003 |
| Estadio TNM 1 3 4a |
503 (88,2%) 65 (11,4%) 2 (0,4%) |
484 (83,4%) 96 (16,6%) 0 (0,0%) |
0,009 |
Comentarios
Para ver los comentarios de sus colegas o para expresar su opinión debe ingresar con su cuenta de IntraMed.