Enfermedad de Parkinson
|
Resumen
|
| Introducción |
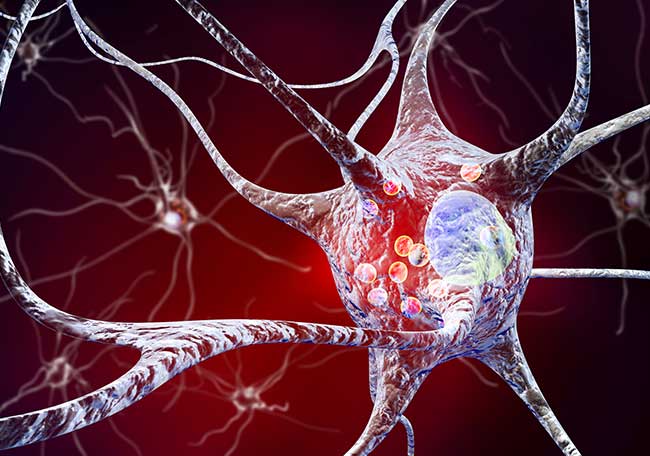
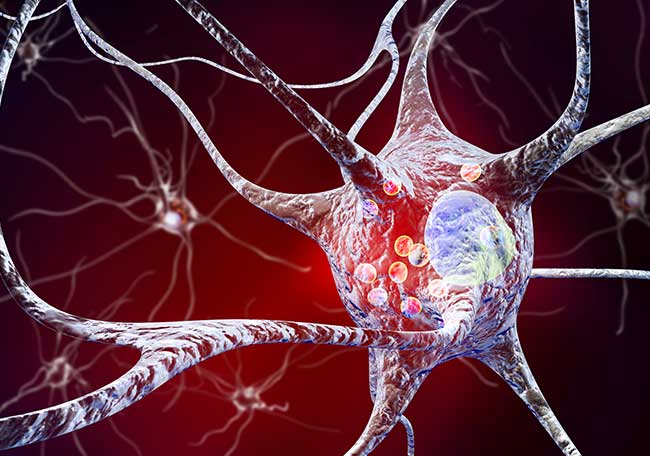
La enfermedad de Parkinson (EP) es una enfermedad neurológica frecuente y compleja. Es una afección neurodegenerativa con muerte precoz de las neuronas dopaminérgicas en la parte compacta de la sustancia negra (substantia nigra pars compacta; SNpc).
El resultado es la deficiencia de dopamina en los ganglios basales que genera un trastorno del movimiento caracterizado por los síntomas motores parkinsonianos clásicos. La EP también se asocia con numerosos síntomas no motores, algunos de los cuales aparecen más de una década antes de la disfunción motora.
No existen pruebas que permitan el diagnóstico definitivo en las primeras etapas de la enfermedad
El pilar del tratamiento de la EP es el tratamiento sintomático con fármacos que aumentan las concentraciones de dopamina o estimulan directamente los receptores de dopamina. La enfermedad afecta además a otros neurotransmisores y regiones del sistema nervioso fuera de los ganglios basales.
En la actualidad la EP se considera como un trastorno neurodegenerativo de progresión lenta que comienza años antes de que se pueda hacer el diagnóstico, implica múltiples zonas neuroanatómicas, se produce por una combinación de factores genéticos y ambientales y se manifiesta con una amplia gama de síntomas.
No existen pruebas que permitan el diagnóstico definitivo en las primeras etapas de la enfermedad. El criterio diagnóstico de referencia es la presencia de degeneración de la SNpc y la patología de Lewy en el examen posmortem.
Esta última consiste en acúmulos anormales de una proteína a-sinucleína, llamados cuerpos de Lewy y neuritas de Lewy. Las estrategias terapéuticas para muchas de las características discapacitantes que aparecen en las etapas tardías de la enfermedad son malas.
Estas características incluyen síntomas motores que no responden a los tratamientos dopaminérgicos o aparecen como complicaciones del empleo prolongado de fármacos dopaminérgicos, como así también un conjunto de síntomas no motores.
La mayor necesidad terapéutica no cubierta son tratamientos que disminuyan la velocidad de la neurodegeneración o detengan el proceso de la enfermedad. No obstante, los conocimientos sobre la patogénesis de la EP están aumentando y por lo tanto ayudando a identificar posibles blancos para modificar la enfermedad.
| Cuadro clínico |
Los síntomas motores clásicos de la enfermedad fueron descritos por James Parkinson en el siglo XIX y más tarde perfeccionados por Jean-Martin Charcot. Estos síntomas son bradicinesia, rigidez muscular, temblor de reposo y alteración postural y de la marcha (cuadro 1).
Las características motoras en los pacientes con enfermedad de Parkinson son heterogéneas y aún no hay consenso en la clasificación de los subtipos de la enfermedad. Las observaciones clínicas sugieren dos subtipos principales:
- con predominio del temblor (y ausencia relativa de otros síntomas motores) y
- sin predominio motor (que incluye fenotipos descritos como síndrome acinético-rígido y trastorno de la marcha con inestabilidad postural).
Otro grupo de pacientes tiene un fenotipo mixto o indeterminado con varios síntomas motores de gravedad comparable.
|
Cuadro 1: Criterios diagnósticos del UK Parkinson’s Disease Society Brain Bank Paso 1: Diagnóstico del síndrome parkinsoniano
Paso 2: Criterios de exclusión de la EP como causa de parkinsonismo. Uno o más de los siguientes sugieren otro diagnóstico
*Este criterio ya no se aplica . Paso 3: Criterios positivos prospectivos que apoyan el diagnóstico de enfermedad de Parkinson Se necesitan tres o más para el diagnóstico definitivo de EP
|
El curso y el pronóstico de la enfermedad difieren entre los subtipos; la enfermedad con predominio del temblor a menudo se asocia con menor velocidad de progresión y menos discapacidad funcional que la EP sin predominio del temblor.
Los trastornos del estado de ánimo y la constipación duplican el riesgo de sufrir EP
Las características no motoras son disfunción olfativa, deterioro cognitivo, síntomas psiquiátricos, trastornos del sueño, disfunción neurovegetativa dolor y fatiga. Estos síntomas son frecuentes al inicio de la enfermedad de Parkinson y se asocian con disminución de la calidad de vida relacionada con la salud. Las características no motoras con frecuencia están presentes antes del inicio de los clásicos síntomas motores.
Esta fase premotora o prodrómica de la enfermedad se puede caracterizar por alteración del olfato, constipación, depresión, somnolencia diurna excesiva y trastorno de conducta del sueño REM (movimientos rápidos de los ojos).
Se considera que los trastornos del estado de ánimo y la constipación duplican el riesgo de sufrir EP. La fase premotora puede ser prolongada, hasta de 12 - 14 años. Se supone que el proceso patológico que causa la EP está en marcha durante esta fase.
Es importante detectar esta etapa prodrómica ya que el tratamiento modificador, cuando esté disponible, podría prevenir o retardar la progresión de la enfermedad.
Al principio la enfermedad se puede controlar con tratamiento sintomático, pero a la medida que avanza, surgen complicaciones relacionadas con el tratamiento sintomático prolongado, entre ellas fluctuaciones motoras y no motoras, discinesia y psicosis que constituyen un desafío terapéutico.(Cuadro 2)
|
Cuadro 2: Complicaciones a largo plazo de los tratamientos dopaminérgicos para la EP Fluctuaciones motoras Alteraciones entre los períodos de buen control de los síntomas motores y períodos de poco control de estos síntomas Fluctuaciones no motoras Alteraciones entre los períodos de buen control de los síntomas no motores y los períodos de disminución del control de estos síntomas Discinesia Movimientos coreiformes o distónicos involuntarios, más frecuentes cuando las concentraciones de levodopa están en su máximo Psicosis inducida por los fármacos Las alucinaciones pueden ser fenómenos menores, como la sensación de que alguien está pasando por su campo visual periférico; también pueden ser alucinaciones visuales bien formadas y con menos frecuencia alucinaciones no visuales (auditivas, táctiles, olfativas; también puede haber delirios (a menudo con paranoia) |
En las fases avanzadas de la EP se observa inestabilidad postural, rigidez de la marcha, caídas, disfagia y trastornos de la palabra. Los síntomas no motores son: incontinencia urinaria, constipación e hipotensión postural. Las probabilidades de demencia son del 83% si la enfermedad ha durado alrededor de 20 años. Cuando el paciente es resistente a la levodopa necesita internación en una institución especializada y su expectativa de vida es limitada.
| Factores de riesgo |
La EP es la enfermedad neurodegenerativa más frecuente después de la enfermedad de Alzheimer. Su incidencia es de 10 - 18 por 100.000 años -persona. El género y la edad son factores de riesgo: es más frecuente en los hombres y aumenta exponencialmente con la edad llegando a su máximo después de los 80 años. Con el aumento de la expectativa de vida, se calcula que aumentará considerablemente en las décadas futuras.
Otros factores de riesgo son los ambientales:
- Exposición a pesticidas.
- Antecedentes de traumatismo de cráneo.
- Consumo de beta-bloqueantes.
- Actividad agraria y consumo de agua de pozo.
Los factores que reducen el riesgo son:
- Tabaquismo.
- Consumo de alcohol y de café.
- Antiinflamatorios no esteroides y bloqueantes de los canales del calcio.
Investigaciones mostraron que los pacientes con EP pueden dejar de fumar más fácilmente que los controles, lo que sugiere que la asociación negativa con el tabaquismo podría deberse a una menor respuesta a la nicotina durante la fase prodrómica de la EP.
Existe una tendencia hereditaria en la EP y se han detectado varios genes con mutaciones, la más importante es la mutación en GBA que codifica para beta-cerebrooxidasa, pero hay varios locus también implicados.
El riesgo de sufrir EP es multifactorial y recién se está descifrando el complicado interjuego entre los diversos factores.
| Anatomía patológica |
La principal alteración anatomopatológica en la EP es la pérdida de neuronas dopaminérgicas en la SNpc. La pérdida de dichas neuronas en esta zona es probablemente la causa de los síntomas motores en los casos avanzados de EP.
Muchas otras regiones del cerebro presentan pérdida neuronal como el locus ceruleus, el núcleo basal de Meynert, el núcleo pedunculopontino, el rafe, el núcleo motor dorsal del vago, la amígdala y el hipotálamo. Otro signo patognomónico de la EP son los cuerpos de Lewy.
Braak et al, propusieron 6 etapas de cuerpos de Lewy, que se inician en el sistema nervioso periférico y van afectando en forma progresiva el sistema nervioso central. Existe relación entre el avance de los cuerpos de Lewy y la sintomatología. Las etapas 1 y 2 corresponderían al inicio de los síntomas premotores, la etapa 3 sería con la presencia de los síntomas motores debido a la deficiencia de dopamina nigroestriada y las etapas 4 a 6 coinciden con los síntomas no motores (alteraciones cognitivas) de la enfermedad.
Varios estudios post mortem mostraron una fuerte relación entre la demencia y la intensidad de patología por cuerpos de Lewy corticales. Estas formaciones serían las causales de la pérdida neuronal.
Sin embargo, en estudios más recientes se observó la presencia de otras moléculas como la alfa-sinucleína que forma una variedad de tipos de acúmulos. Uno de ellos serían ciertas formas oligoméricas de la alfa-sinucleína que podrían ser tóxicas para las neuronas.
También se detectaron otros acúmulos proteicos no relacionados con a-sinucleína, como placas beta-amiloide y ovillos neurofibrilares que contienen tau, las inclusiones proteicas características de la enfermedad de Alzheimer, con la misma cantidad y distribución que en esta.
Así, inclusiones de otras proteínas distintas a la a-sinucleína podrian actuar sinérgicamente con la patología de Lewy y contribuir a la expresión clínica dela EP.
Por último, con la identificación y caracterización de formas monogénicas de la EP, se halló que la enfermedad puede existir sin patología de Lewy. Esto sugiere que otras formas de acúmulos de a-sinucleína, así como inclusiones que contienen proteínas distintas a esta, son características anatomopatológicas importantes de la EP.
La neuroinflamación es otra característica anatomopatológica de la EP. Tanto la gliosis reactiva debida a los astrocitos activados como la microgliosis producida por activación de la microglía se hallan en las zonas de neurodegeneración.
Astrocitos y microglía participan en la eliminación de residuos extracelulares, lo que podría contribuir a la supervivencia de las neuronas. La microglía activada puede liberar factores tróficos, pero también especies reactivas del oxígeno y el nitrógeno y citosinas proinflamatorias. Aún no se ha determinado si el equilibrio entre estas acciones es favorable o perjudicial para las neuronas.
| Genética |
En los últimos 15 años se efectuaron importantes descubrimientos en la genética de la EP. El primer gen identificado relacionado con la EP fue SNCA y las mutaciones del mismo se asocian con el parkinsonismo autosómico dominante. Las mutaciones causantes de enfermedad incluyen las mutaciones de sentido erróneo, que producen sustituciones de los aminoácidos y multiplicaciones del locus del gen.
Las sustituciones de los aminoácidos debidas a estas mutaciones de sentido erróneo o al aumento de la expresión de las proteínas producido por las multiplicaciones del locus del gen hacen que la a-sinucleína sea proclive a formar acúmulos.
La EP relacionada con SNCA es rara, pero el reconocimiento de las mutaciones de SNCA como causa genética de la EP condujo a identificar a una a-sinucleína como el componente principal de los cuerpos de Lewy y las neuritas. Además, ese hallazgo dio lugar al descubrimiento de un listado creciente de genes asociados con las formas monogénicas de la EP
Comentarios
Para ver los comentarios de sus colegas o para expresar su opinión debe ingresar con su cuenta de IntraMed.