Diagnóstico del síndrome de Cushing

Hace más de un siglo, Harvey Cushing introdujo el término "síndrome pluriglandular" para describir un trastorno caracterizado por el desarrollo de obesidad central, hipertensión arterial, debilidad muscular proximal, diabetes mellitus, oligomenorrea, hirsutismo, piel delgada y equimosis. Cushing sabía que este síndrome estaba asociado con el cáncer suprarrenal y sospechaba que algunos casos podrían tener un componente hipofisario.
El 6 de septiembre de 1911 realizó una craneotomía en uno de sus pacientes (conocido como Caso XLV) pero no halló ningún tumor hipofisario. En su descripción del caso, continúa diciendo que "posiblemente estaremos en el camino hacia el reconocimiento de las consecuencias del hiperadrenalismo." Con el tiempo, quedó claro que el trastorno podría estar causado por pequeños adenomas basófilos de la hipófisis. Este síndrome pluriglandular se conoce como síndrome de Cushing.
Fuller Albright proporcionó el siguiente avance conceptual en un informe extraordinario publicado en el primer volumen de la Conferencia de la Hormona Laurentiana, "Los efectos de las hormonas sobre la osteogénesis en el hombre ":
Ha sido nuestro concepto que el protoplasma en general, como la matriz protoplasmática ósea, se anaboliza constantemente y se cataboliza al mismo tiempo. Un factor que aumente el catabolismo conduciría al mismo resultado neto que un factor que inhiba el anabolismo, pero podría haber diferencias. Yo creo que la hormona "S" [cortisol], más que catabólica es antianabólica… En el síndrome adreno-genital, el antianabolismo... está contrarrestado con el anabolismo aumentado debido a un exceso de hormona "N" [testosterona]. Este antianabolismo del protoplasma en el síndrome de Cushing da cuenta no solo de la osteoporosis, sino también de la debilidad muscular, la piel delgada, la probable tendencia a los hematomas y, posiblemente, la atrofia del tejido linfoide y del timo.
No obstante, en los años transcurridos, el examen físico de los pacientes con sospecha de un exceso de glucocorticoides se centró en los cambios anabólicos, sobre todo excluyendo los cambios antianabólicos. Con el rápido aumento de la tasa de obesidad en la población general, el síndrome de Cushing ya no puede ser separado confiablemente del síndrome metabólico de la obesidad simple solo sobre la base de los signos anabólicos. Sin embargo, en el síndrome de Cushing los cambios antianabólicos sirven para hacer esta diferenciación.
Examen físico
Casi un tercio de la población estadounidense es obesa. Se estima que la prevalencia mundial del síndrome metabólico entre las personas obesas es 10%. El cuadro clínico de este síndrome es casi el mismo que el del síndrome de Cushing, La prevalencia de pacientes con síndrome de Cushing no diagnosticado es de alrededor de 75 casos/1 millón de personas.
Según estas estimaciones de prevalencia, la posibilidad de que 1 persona con obesidad, hipertensión, hirsutismo, diabetes tipo 2 y dislipidemia tenga el síndrome de Cushing es de 1 en 500. En la época de Harvey Cushing, cuando la obesidad era rara, el diagnóstico del síndrome de Cushing era el aspecto más certero del manejo de este trastorno. Hoy en día, respecto del cuidado de los pacientes con síndrome de Cushing el establecimiento del diagnóstico es el aspecto menos seguro.
El síndrome metabólico causado por la hipersecreción de glucocorticosteroides puede ser diferenciado del síndrome metabólico asociado a la obesidad mediante una cuidadosa evaluación de los efectos antianabólicos del cortisol. Estos efectos-osteopenia, piel delgada y equimosis-están presentes en los pacientes con síndrome de Cushing pero no en los pacientes con obesidad simple.
Los pacientes en los que se diagnostica osteoporosis radiográficamente tienen más probabilidad de tener síndrome de Cushing que aquellos que no tienen osteoporosis, con un cociente de probabilidad positivo de 11. Hoy en día, un puntaje z-2 en la columna lumbar apoya este criterio. Para esta medición, comúnmente se utiliza la piel que cubre la falange proximal del dedo medio de la mano no dominante.
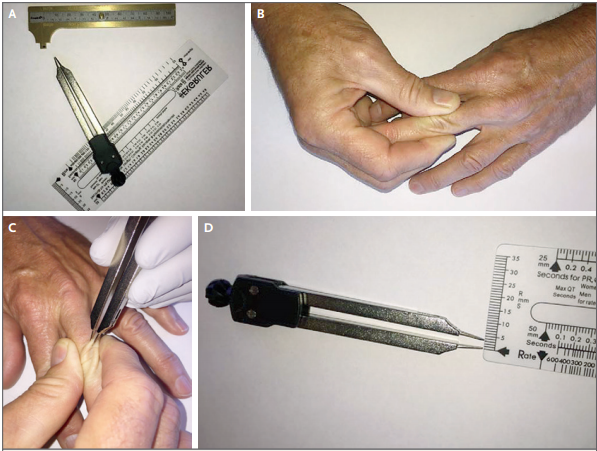
Medición del grosor del pliegue cutáneo.
La medición se hace con un calibre y un micrómetro o regla milimétrica (Panel A). Se crea un pliegue cutáneo (Panel B) y se mide con el calibre (Panel C). El grosor del pliegue cutáneo se lee en la regla. En este caso, el grosor es de 3 mm (Panel D).
Se considera que la piel es delgada si el grosor es <2 mm. Los pacientes con la piel más delgada son más proclives a tener síndrome de Cushing, con un cociente de probabilidad positivo de 116. Finalmente, los pacientes que tienen ≥3 equimosis >1 cm de diámetro y no están asociadas a traumatismos como la venopunción son más propensos a tener el síndrome de Cushing que los pacientes sin estos hallazgos, con un cociente de verosimilitud de 4.
Si se conoce la prevalencia de casos de síndrome de Cushing no diagnosticados en la población de personas con síndrome metabólico relacionado con la obesidad, se puede comenzar a calcular la probabilidad de que una persona tenga síndrome de Cushing usando el cociente de probabilidad de las características antianabólicas observadas en el examen físico. Los cocientes de probabilidad pueden ser convertidos en probabilidades usando el teorema de Bayes. Esta conversión es notablemente facilitada por el nomograma de Fagan para este propósito.
La prevalencia del síndrome de Cushing no diagnosticado se desconoce, pero se puede estimar. Dos personas/1 millón de habitantes mueren cada año por cáncer suprarrenal. La expectativa de vida actual para los pacientes con carcinoma adrenocortical, después del diagnóstico, es de 2 a 4 años. Asumiendo que se tarda 3 años para hacer el diagnóstico, la prevalencia dl síndrome no diagnosticado es de 6 casos/millón. En la mayoría de las series de casos de síndrome de Cushing, un promedio del 8% de los pacientes tiene carcinoma suprarrenal.
El autor calcula que si 6 personas/millón corresponden al 8% del grupo, el grupo de síndrome de Cushing total es de 75 personas/millón, o sea, 24.000 personas. Si los 24.000 pacientes están incluidos en el grupo de síndrome metabólico, compuesto por 12 millones de personas, la prevalencia del síndrome de Cushing es 0,002 o 0,2%. Con una proba4bilidad de 0,2% y un cociente de verosimilitud de 116 para la piel delgada, 18 para la osteopenia y 4 para equimosis, la probabilidad de que un paciente con estos 3 hallazgos tenga el síndrome de Cushing es del 95%.
Cortisol libre urinario
El diagnóstico de todas las enfermedades endocrinas requiere una presentación clínica que sea compatible con la enfermedad, así como la identificación de las causas fisiopatológicas. Una evaluación de los efectos del exceso de glucocorticoides puede realizarse mediante el nivel de cortisol libre en la orina de 24 horas. Hay 2 tipos de cortisol libre: el cortisol no ligado a las proteínas plasmáticas y el cortisol no conjugado al ácido sulfúrico o hialurónico. El cortisol no ligado a las proteínas se filtra en el glomérulo y luego se reabsorbe en el túbulo colector. Alrededor del 3% del cortisol filtrado se elimina por orina.
Por lo tanto, el cortisol libre urinario no está conjugado y su nivel en la orina refleja el nivel de cortisol bioactivo libre en el plasma. El nivel de cortisol libre se mide en una muestra de orina de 24 horas, promediando la secreción aumentada del cortisol de la mañana y la secreción disminuida del cortisol de la tarde y la noche. También se mide la creatinina urinaria para determinar si la recolección está completa. Los niveles de creatinina <1,5 g/día en los hombres y <1 g/día en las mujeres indican que la recolección fue incompleta, y la prueba debe ser repetida.
El cortisol no conjugado puede extraerse directamente de la orina con un disolvente lipídico no polar. Después de la extracción, el cortisol se purifica mediante la cromatografía líquida de alta presión y luego, usualmente se cuantifica mediante un radioinmunoensayo. El cortisol libre también puede ser medido directamente por medio de la espectroscopia de masas. Los análisis de elección del cortisol libre urinario utilizan la separación por cromatográfica líquida de alta presión, seguida de la cuantificación por espectrometría de masas. Con este ensayo, el cortisol libre urinario en los adultos los sanos oscila entre 8 y 51 μg/24 horas.
La depresión clínica aumenta la excreción urinaria de cortisol libre, y en los pacientes con síntomas y signos clínicos típicos de depresión, la mayoría de los estudios muestra un nivel de cortisol que oscila entre 10 y 60 μg/día. Si el punto de corte utilizado es <60 μg/día entre los valores normales (<60 μg/día) y los valores elevados (≥ 60 μg/día), un cortisol libre urinario ≥62 μg/día da un cociente de probabilidad positivo de 11. Así, en un paciente que presenta obesidad, hipertensión, diabetes tipo 2 e hirsutismo y tiene piel delgada, osteopenia y equimosis, y un nivel de cortisol urinario elevado, la probabilidad de tener síndrome de Cushing es 1 (100%). En estos casos, el médico debe pasar directamente a evaluar un diagnóstico diferencial.
Prueba de supresión con dexametasona
Esta prueba se utiliza comúnmente para el diagnóstico del síndrome de Cushing. Fue desarrollada por Grant Liddle a principios de la década de 1960 como prueba diagnóstica para distinguir el síndrome de Cushing corticotrofina-dependiente del mismo síndrome pero corticotrofina-Independiente. En la actualidad, el diagnóstico se realiza midiendo el nivel de corticotrofina plasmática. Lamentablemente, dice el autor, la prueba de supresión con dexametasona se ha seguido usando para detectar el síndrome de Cushing.
El grupo de control para esta prueba comprende a los pacientes con obesidad y depresión en quienes la secreción de cortisol no se suprime en respuesta a una dosis oral de 1 mg de dexametasona a la medianoche. De la actual población estadounidense de 360 millones de personas, así un tercio son obesos. De los que son obesos, el 10% tiene depresión. En la mitad de estos pacientes, la prueba de supresión con dexametasona será negativa. Basado en sus estimaciones, el autor sostiene que “si la prevalencia actual de pacientes con síndrome de Cushing es de 24.000 casos y la estimación de la población en riesgo es de 6 millones de personas, entonces el valor predictivo positivo de la prueba de supresión con dexametasona es solo del 0,4%. Por lo tanto, acota, esta prueba no debe influir en las decisiones del médico y no se debe seguir usando para este propósito.”
Cuadros atípicos
En los pacientes con evidencia convincente de síndrome de Cushing en el examen físico y con niveles elevados de cortisol libre en orina de 24 horas, se debe hacer el diagnóstico diferencial siguiendo el proceso descrito más adelante por el autor. Sin embargo, un pequeño grupo de pacientes no cumple estos criterios.
Algunos pacientes tienen un examen físico muy característico pero con una excreción de cortisol libre urinario baja o nula. En estos pacientes, los niveles de corticotrofina plasmática están suprimidos. Se deben identificar los glucocorticoides exógenos que el paciente está recibiendo. Se debe identificar el glucocorticoide para luego planificar su descontinuación. A veces, el glucocorticoide es administrado por un tercero (por ej., un padre a su hijo), y no se puede constatar el antecedente de su administración. Sin embargo, el glucocorticoide debe ser identificado y descontinuado.
Comentarios
Para ver los comentarios de sus colegas o para expresar su opinión debe ingresar con su cuenta de IntraMed.