Shock circulatorio

Introducción
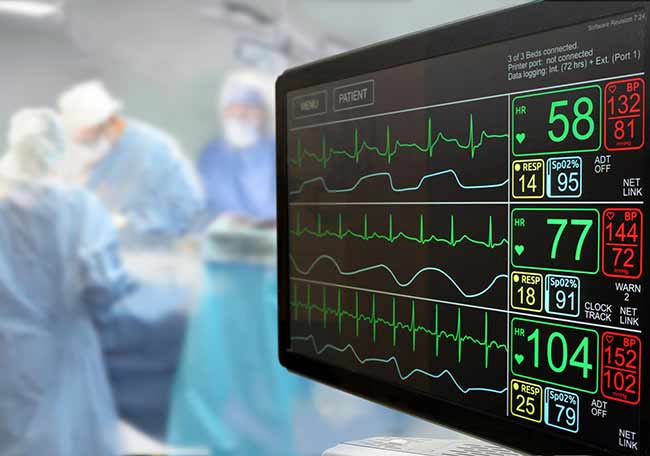
El shock es la expresión clínica de la insuficiencia circulatoria, que lleva a la utilización inadecuada del oxígeno celular. Es frecuente en las unidades de cuidados intensivos (UCI), donde afecta a alrededor de un tercio de los pacientes. El diagnóstico de shock se basa sobre signos clínicos, hemodinámicos y bioquímicos, que se pueden resumir en tres componentes.
|
Mecanismos fisiopatológicos
El shock se puede producir por cuatro mecanismos fisiopatológicos no necesariamente exclusivos:
- Hipovolemia (por pérdida de líquidos interna o externa)
- Factores cardiogénicos (e.g., infarto agudo de miocardio, miocardiopatía terminal, enfermedad valvular avanzada, miocarditis o arritmias cardíacas)
- Obstrucción (e.g., embolia pulmonar, taponamiento cardíaco o neumotórax a tensión)
- Factores distributivos (e.g., sepsis o anafilaxia graves debido a la liberación de mediadores inflamatorios).
Los tres primeros mecanismos se caracterizan por bajo gasto cardíaco y, por lo tanto, insuficiente transporte de oxígeno. En el shock distributivo, la insuficiencia principal está en la periferia, con disminución de la resistencia vascular sistémica y alteración de la extracción de oxígeno. En estos casos el gasto cardíaco es alto, aunque puede ser bajo si también hay depresión miocárdica. En los pacientes con insuficiencia circulatoria aguda a menudo estos mecanismos se asocian.
Diagnóstico diferencial
El shock séptico es la forma más frecuente de shock entre pacientes en la UCI, seguido del shock cardiogénico y el shock hipovolémico, mientras que el shock obstructivo es relativamente raro. En un estudio de más de 1600 pacientes con shock, el 62% sufría shock séptico, el 16% shock cardiogénico, el 16% shock hipovolémico, el 4% otros tipos de shock distributivo y el 2% shock obstructivo.
El tipo y la causa del shock pueden ser evidentes por la historia clínica, el examen físico o los exámenes complementarios.
En el examen físico se deben evaluar el color y la temperatura de la piel, la distensión de la vena yugular y el edema periférico.
El diagnóstico se puede refinar con la evaluación del ecocardiograma en el lugar de atención, que incluye la evaluación para derrame pericárdico, la medición del tamaño y la función de ambos ventrículos, la determinación de las variaciones respiratorias en las dimensiones de la vena cava y el cálculo de la integral velocidad aórtica-tiempo, que mide el volumen sistólico. Siempre que se pueda, se debe efectuar ecocardiograma focalizado lo antes posible en todo paciente que llega a la consulta en shock.
Conducta inicial frente al paciente con shock
El apoyo hemodinámico precoz y adecuado de los pacientes en shock es esencial para prevenir que empeoren la disfunción y la insuficiencia orgánica. Se debe iniciar la reanimación incluso cuando todavía se está investigando la causa. Una vez identificada, la causa se debe corregir rápidamente (e.g., control de la hemorragia, angioplastia intraluminal coronaria para los síndromes coronarios, trombolisis o embolectomía para la embolia pulmonar masiva y antibioticoterapia y control del origen para el shock séptico).
Se deben insertar un catéter arterial para controlar la presión arterial y tomar muestras de sangre y un catéter venoso central para administrar líquidos y agentes vasoactivos.
El tratamiento inicial del shock se orienta hacia los problemas que produce, independientemente de la causa. Los componentes importantes de la reanimación son la administración de oxígeno, la reanimación con líquidos y la administración de agentes vasoactivos.
Apoyo respiratorio
Uso de O2
Se debe administrar oxígeno inmediatamente para aumentar su suministro y prevenir la hipertensión pulmonar. El monitoreo de las gases en sangre es preferible para determinar con precisión las necesidades de oxígeno, ya que la oximetría de pulso puede no ser fiable debido a la vasoconstricción periférica.
Intubación endotraqueal y ARM
Se debe efectuar intubación endotraqueal para proporcionar apoyo respiratorio mecánico en casi todos los pacientes con disnea intensa, hipoxemia o acidemia persistente o que empeora (pH, <7,30). La asistencia respiratoria mecánica tiene la ventaja de disminuir la demanda de oxígeno de los músculos respiratorios, así como la poscarga del ventrículo izquierdo al aumentar la presión intratorácica. La disminución abrupta de la presión arterial tras iniciar la asistencia respiratoria mecánica sugiere hipovolemia y disminución del retorno venoso. El empleo de sedantes se debe reducir al mínimo a fin de evitar más descenso de la presión arterial y del gasto cardíaco.
Reanimación con líquidos
El tratamiento con líquidos para mejorar el flujo sanguíneo microvascular y aumentar el gasto cardíaco es una parte esencial del tratamiento de cualquier forma de shock. Se lo debe controlar estrechamente, ya que el exceso de líquidos implica el riesgo de edema.
En general, el objetivo es que el gasto cardíaco pueda ser independiente de la precarga (i.e., en la porción en meseta de la curva de Frank–Starling), pero esto es difícil de evaluar clínicamente.
En pacientes que reciben ventilación mecánica, los signos de respuesta a los líquidos se pueden identificar ya sea directamente por mediciones del volumen sistólico latido a latido con el empleo de monitores del gasto cardíaco o indirectamente por las variaciones observadas en la presión del pulso en el trazado de la presión arterial durante el ciclo del respirador. No obstante, estas deducciones a la cabecera del paciente tienen algunas limitaciones, en especial que el paciente debe recibir asistencia respiratoria con volúmenes corrientes relativamente grandes, no tener esfuerzo respiratorio espontáneo (lo que exige la administración de sedantes o incluso relajantes musculares), no sufrir arritmia importante ni disfunción ventricular derecha. La prueba de levantamiento pasivo de la pierna es otro método, pero exige un dispositivo de respuesta rápida, ya que el efecto es transitorio.
La prueba de sobrecarga de líquidos se debe emplear para determinar la respuesta del paciente a los líquidos y al mismo tiempo limitar los riesgos de efectos adversos. La prueba incorpora cuatro elementos que se deben definir por anticipado:
- El tipo de líquido. Las soluciones con cristaloides son de primera elección, por ser bien toleradas y baratas.
- La velocidad de administración. Los líquidos se deben administrar rápidamente para inducir una respuesta rápida. En general se administran 300 - 500 ml de líquidos en 20 - 30 minutos.
- Se debe definir el objetivo de la prueba de sobrecarga de líquidos. En el shock, el objetivo es el aumento de la presión arterial, aunque también podría ser la disminución de la frecuencia cardíaca o el aumento de la diuresis.
- Por último, se deben definir los límites de la seguridad. El edema pulmonar es la complicación más grave de la administración de líquidos. En general se considera como límite una presión venosa central de algunos milímetros de mercurio por encima del valor basal, a fin de prevenir la sobrecarga de líquidos.
Se debe evitar la estimulación del paciente y cualquier otro cambio en el tratamiento durante la prueba.
Fármacos vasoactivos
"La administración de dopamina se puede asociar con mayores tasas de muerte que la norepinefrina entre pacientes con shock séptico, por lo que ya no se la recomienda para los pacientes con shock"
Vasopresores
Si la hipotensión es grave o persiste a pesar de la administración de líquidos, están indicados los vasopresores. Se puede administrar un vasopresor temporariamente mientras se efectúa la reanimación, para suspenderlo, si es posible, después de corregir la hipovolemia.
Los agonistas adrenérgicos son los vasopresores de primera línea debido a su comienzo de acción rápido, su gran potencia y su semivida breve, que permite ajustar fácilmente la dosis. La estimulación de cada tipo de receptor adrenérgico tiene efectos que pueden ser beneficiosos y perjudiciales.
Por ejemplo, la estimulación β-adrenérgica puede aumentar el flujo sanguíneo, pero también aumenta el riesgo de isquemia miocárdica debido al aumento de la frecuencia y la contractilidad cardíacas. Por ello, el empleo de isoproterenol, un β-adrenérgico puro, está limitado al tratamiento de pacientes con bradicardia grave.
En el otro extremo, la estimulación α-adrenérgica aumenta el tono vascular y la presión arterial, pero también puede disminuir el gasto cardíaco y afectar el flujo sanguíneo tisular, especialmente en la región hepatoesplácnica. Debido a esto, la fenilefrina, un α-adrenérgico casi puro, raras veces está indicada.
La norepinefrina es el vasopresor de primera elección; tiene propiedades predominantemente α-adrenérgicas, pero sus efectos β-adrenérgicos modestos ayudan a mantener el gasto cardíaco. Su administración en general produce el aumento significativo de la presión arterial media, con escaso cambio de la frecuencia cardíaca o el gasto cardíaco. La dosis es 0,1 – 2,0 μg por kilo y por minuto.
La dopamina tiene efectos predominantemente β-adrenérgicos a dosis bajas y efectos α-adrenérgicos a dosis altas, pero ambos son relativamente débiles.
Los efectos dopaminérgicos a dosis muy bajas (<3 μg por kilo y por minuto, por vía intravenosa) pueden dilatar selectivamente las circulaciones hepatoesplácnica y renal, pero estudios controlados no mostraron efecto protector sobre la función renal. La estimulación dopaminérgica también puede tener efectos endocrinos indeseados sobre el sistema hipotalámico-hipofisario y producir inmunosupresión, principalmente por reducción de la liberación de prolactina.
En un estudio aleatorizado, controlado, doble ciego reciente, la dopamina no tuvo ninguna ventaja sobre la norepinefrina, pero indujo más arritmias y se asoció con aumento de la tasa de mortalidad a 28 días entre pacientes con shock cardiogénico. La administración de dopamina también se puede asociar con mayores tasas de muerte que la norepinefrina entre pacientes con shock séptico, por lo que ya no se la recomienda para los pacientes con shock.
La epinefrina tiene efectos predominantemente β-adrenérgicos a dosis bajas. Los efectos α-adrenérgicos son más significativos a dosis más altas. Sin embargo, la administración de epinefrina se puede asociar con mayor tasa de arritmias y disminución del flujo sanguíneo esplácnico y puede aumentar el lactato sanguíneo. Estudios prospectivos, aleatorizados, no mostraron que la epinefrina tenga mayores efectos favorables que la norepinefrina en el shock séptico.
Comentarios
Para ver los comentarios de sus colegas o para expresar su opinión debe ingresar con su cuenta de IntraMed.