Tratamiento breve para tuberculosis
Antecedentes
Los regímenes basados en rifapentina tienen una potente actividad antimicobacteriana que puede permitir un curso más corto en pacientes con tuberculosis pulmonar susceptible a fármacos.
Métodos
En un ensayo controlado, aleatorizado, de fase 3, abierto en el que participaron personas con tuberculosis pulmonar recién diagnosticada de 13 países, comparamos dos regímenes basados en rifapentina de 4 meses con un régimen estándar de 6 meses que consistía en rifampicina, isoniazida, pirazinamida y etambutol (control) utilizando un margen de no inferioridad de 6,6 puntos porcentuales.
En un regimen de 4 meses, la rifampicina se reemplazó por rifapentina; en el otro, la rifampicina se reemplazó por rifapentina y el etambutol por moxifloxacino.
El resultado primario de eficacia fue la supervivencia libre de tuberculosis a los 12 meses.
Resultados
Entre 2.516 participantes que habían sido aleatorizados, 2.343 tenían un cultivo positivo para Mycobacterium tuberculosis que no era resistente a isoniazida, rifampicina o fluoroquinolonas (población microbiológicamente elegible; 768 en el grupo de control, 791 en el grupo de rifapentina-moxifloxacina y 784 en el grupo de rifapentina-moxifloxacina grupo rifapentina), de los cuales 194 estaban coinfectados con el virus de la inmunodeficiencia humana y 1.703 tenían cavitación en la radiografía de tórax.
Se pudo evaluar un total de 2.234 participantes para el resultado primario (población evaluable; 726 en el grupo de control, 756 en el grupo de rifapentina-moxifloxacina y 752 en el grupo de rifapentina). La rifapentina con moxifloxacina no fue inferior al control en la población microbiológicamente elegible (el 15,5% frente al 14,6% tuvo un resultado desfavorable; diferencia, 1,0 punto porcentual; intervalo de confianza [IC] del 95%, -2,6 a 4,5) y en la población evaluable 11,6% frente a 9,6%; diferencia, 2,0 puntos porcentuales; IC del 95%, −1,1 a 5,1).
La no inferioridad se mostró en los análisis secundarios y de sensibilidad. La rifapentina sin moxifloxacina no mostró ser inferior al control en ninguna de las poblaciones (17,7% frente a 14,6% con un resultado desfavorable en la población microbiológicamente elegible; diferencia, 3,0 puntos porcentuales [IC del 95%, −0,6 a 6,6]; y 14,2 % vs. 9,6% en la población evaluable; diferencia, 4,4 puntos porcentuales [IC del 95%, 1,2 a 7,7]).
Los eventos adversos de grado 3 o superior ocurrieron durante el período de tratamiento en el 19,3% de los participantes en el grupo de control, el 18,8% en el grupo de rifapentina-moxifloxacina y el 14,3% en el grupo de rifapentina.
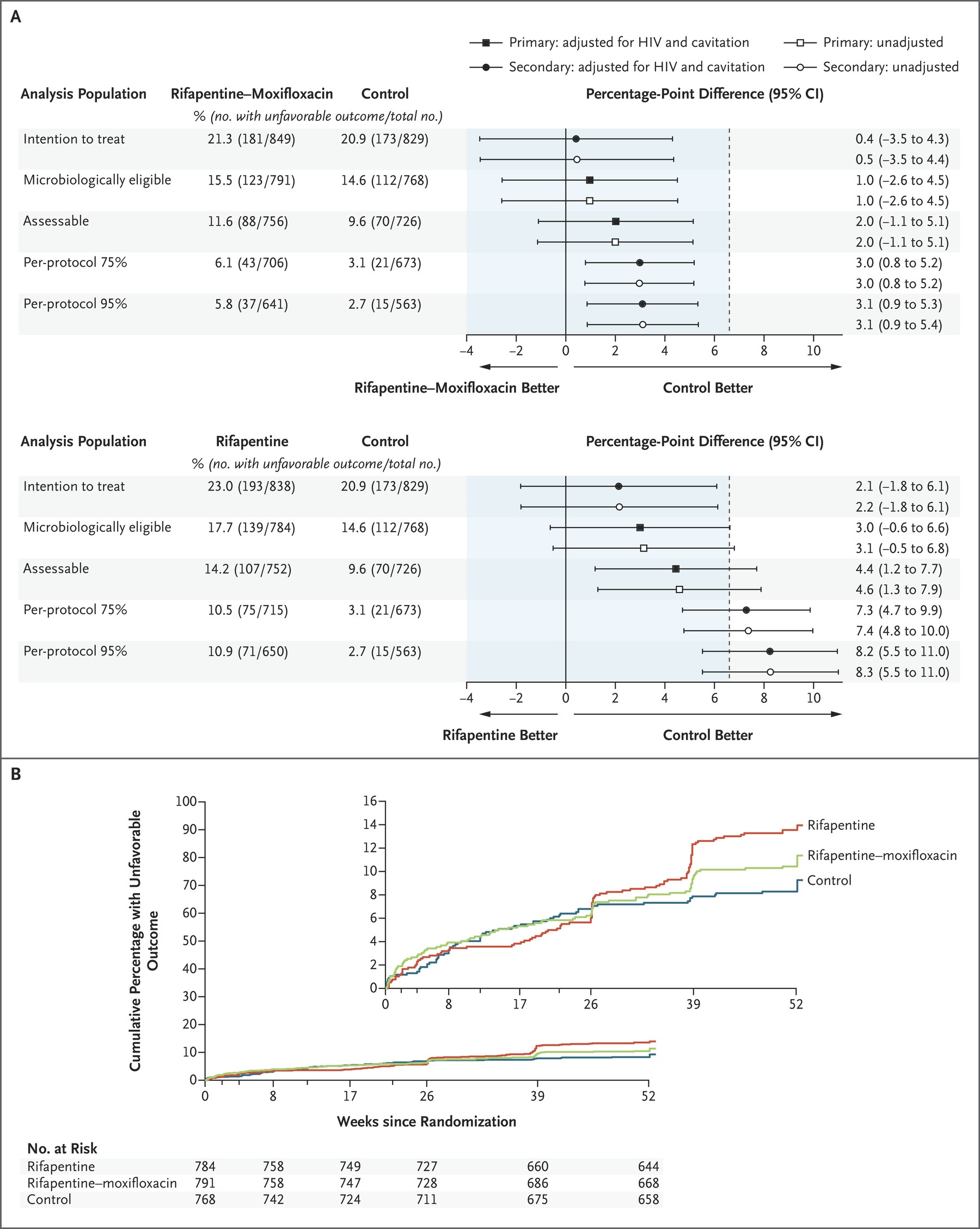
Análisis de eficacia primaria y secundaria y tiempo hasta un resultado desfavorable. El panel A muestra los resultados del análisis de eficacia primario en las poblaciones de análisis evaluables y microbiológicamente elegibles y de los análisis secundarios en las poblaciones de análisis por intención de tratar y por protocolo (superior, régimen de rifapentina-moxifloxacina frente a régimen de control; abajo, régimen de rifapentina frente a régimen de control). El margen de no inferioridad de 6,6 puntos porcentuales está designado por la línea vertical discontinua. Los participantes se clasificaron como con un resultado desfavorable si tenían cultivos positivos para M. tuberculosis de dos muestras de esputo obtenidas en la semana 17 o después sin un cultivo negativo intermedio, murieron o se retiraron del ensayo o se perdieron durante el seguimiento durante el período de tratamiento. , tenía un cultivo positivo para M. tuberculosis cuando se vio por última vez, murió de tuberculosis durante el seguimiento posterior al tratamiento o recibió tratamiento adicional para la tuberculosis. La población de análisis microbiológicamente elegible incluyó a todos los participantes excepto aquellos que no tenían evidencia de cultivos positivos para M. tuberculosis, que tenían tuberculosis resistente a isoniazida, rifampicina o fluoroquinolonas, o que se inscribieron en violación de los criterios de elegibilidad; los participantes con un estado de resultado que no fue evaluable se reclasificaron por haber tenido un resultado desfavorable. La población de análisis evaluable incluyó a los participantes de la población microbiológicamente elegible, excepto aquellos cuyo estado de resultado se había reclasificado de no evaluable a desfavorable. Las poblaciones de análisis por protocolo del 75% y por protocolo del 95% incluyeron a los participantes en la población evaluable, excepto aquellos que no completaron el 75% o el 95% de las dosis de tratamiento asignadas, respectivamente, a menos que el motivo del tratamiento inadecuado fuera la muerte o fracaso del tratamiento bacteriológico. El panel B muestra los resultados del tiempo hasta un resultado desfavorable para la población microbiológicamente elegible. Se censuraron los datos de los participantes que no pudieron ser evaluados. VIH denota virus de inmunodeficiencia humana. El recuadro muestra los mismos datos en un eje y expandido.
Comentarios
Para ver los comentarios de sus colegas o para expresar su opinión debe ingresar con su cuenta de IntraMed.






