Seguridad y eficacia de la vacuna de ARNm Pfizer/BioNTech
Antecedentes
La infección por coronavirus 2 (SARS-CoV-2) del síndrome respiratorio agudo severo y la enfermedad resultante por coronavirus 2019 (Covid-19) han afectado a decenas de millones de personas en una pandemia mundial. Se necesitan con urgencia vacunas seguras y eficaces.
Métodos
En un ensayo pivotal de eficacia multinacional, controlado con placebo, ciego al observador y en curso, asignamos al azar a personas de 16 años o más en una proporción de 1: 1 para recibir dos dosis, con 21 días de diferencia, de placebo o de la vacuna candidata BNT162b2 (30 μg por dosis).
BNT162b2 es una vacuna de ARN modificada con nucleósidos, formulada con nanopartículas lipídicas, que codifica una proteína de pico de longitud completa del SARS-CoV-2, estabilizada por prefusión y anclada a la membrana.
Los criterios de valoración principales fueron la eficacia de la vacuna contra Covid-19 confirmado en laboratorio y la seguridad.
Resultados
Un total de 43.548 participantes fueron aleatorizados, de los cuales 43.448 recibieron inyecciones: 21.720 con BNT162b2 y 21.728 con placebo.
Hubo 8 casos de Covid-19 que comenzaron al menos 7 días después de la segunda dosis entre los participantes asignados a recibir BNT162b2 y 162 casos entre los asignados a placebo; BNT162b2 fue 95% efectivo en la prevención de Covid-19 (intervalo creíble del 95%, 90,3 a 97,6).
Se observó una eficacia similar de la vacuna (generalmente del 90 al 100%) en los subgrupos definidos por edad, sexo, raza, etnia, índice de masa corporal inicial y la presencia de afecciones coexistentes.
Entre los 10 casos de Covid-19 grave que comenzaron después de la primera dosis, 9 ocurrieron en receptores de placebo y 1 en un receptor de BNT162b2.
El perfil de seguridad de BNT162b2 se caracterizó por dolor a corto plazo de leve a moderado en el lugar de la inyección, fatiga y dolor de cabeza.
La incidencia de eventos adversos graves fue baja y similar en los grupos de vacuna y placebo.
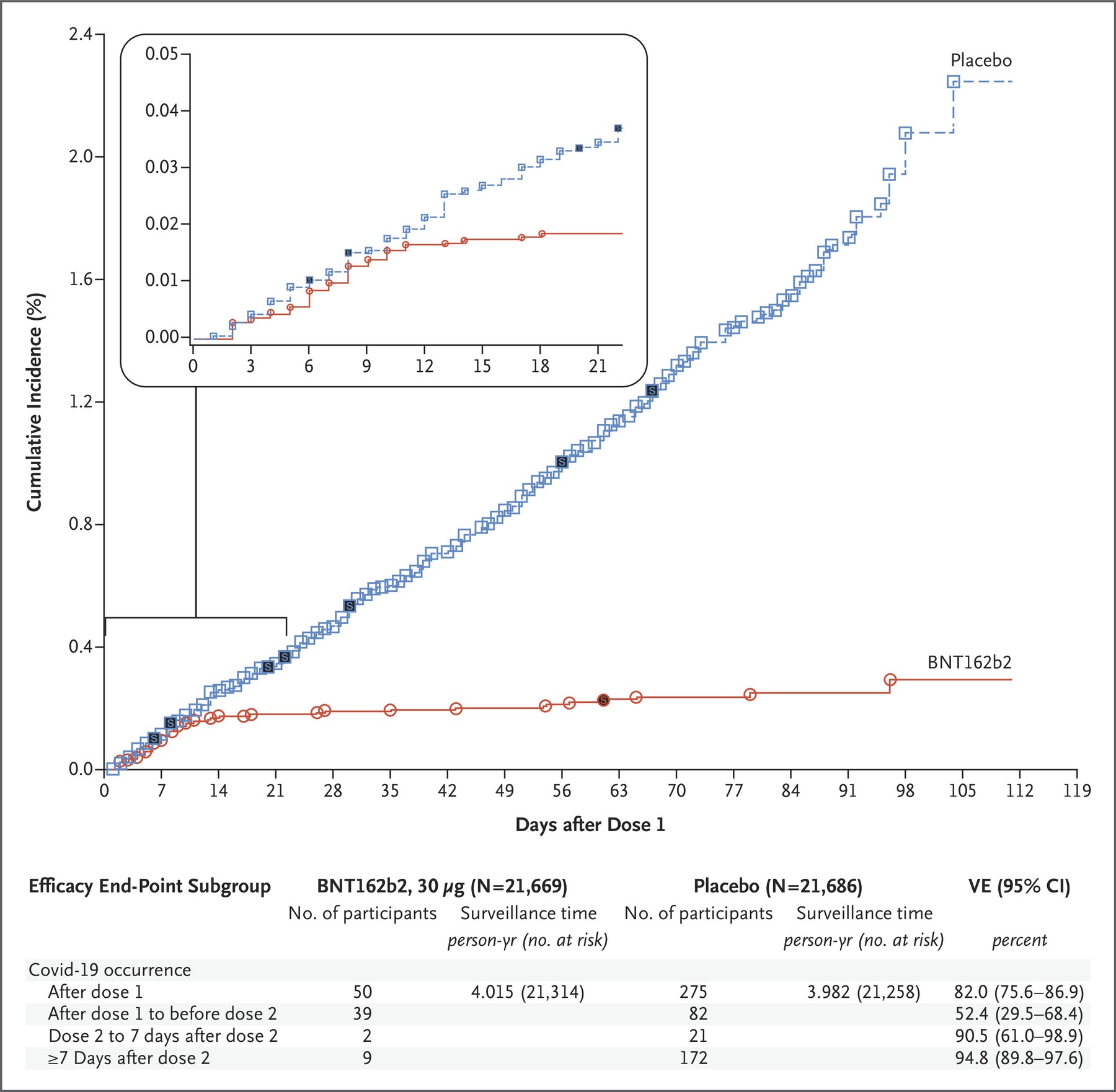
Eficacia de BNT162b2 contra Covid-19 después de la primera dosis. Se muestra la incidencia acumulada de Covid-19 después de la primera dosis (población modificada por intención de tratar). Cada símbolo representa los casos de Covid-19 que comienzan en un día determinado; Los símbolos rellenos representan casos graves de Covid-19. Algunos símbolos representan más de un caso debido a la superposición de fechas. El recuadro muestra los mismos datos en un eje y ampliado, durante 21 días. El tiempo de vigilancia es el tiempo total en 1000 personas-año para el punto final dado en todos los participantes dentro de cada grupo en riesgo para el punto final. El período de tiempo para la acumulación de casos de Covid-19 es desde la primera dosis hasta el final del período de vigilancia. El intervalo de confianza (IC) para la eficacia de la vacuna (VE) se obtiene de acuerdo con el método Clopper-Pearson.
|
Conclusiones
|
Discusión
Se encontró que un régimen de dos dosis de BNT162b2 (30 μg por dosis, administrados con 21 días de diferencia) era seguro y tenía una eficacia del 95% contra Covid-19.
La vacuna cumplió con los dos criterios de valoración principales de eficacia, con más de un 99,99% de probabilidad de una verdadera eficacia de la vacuna superior al 30%. Estos resultados cumplieron con nuestros criterios de éxito preespecificados, que consistían en establecer una probabilidad superior al 98,6% de que la verdadera eficacia de la vacuna fuera superior al 30%, y excedieron en gran medida los criterios mínimos de autorización de la FDA.
Aunque el estudio no tenía el poder para evaluar definitivamente la eficacia por subgrupo, las estimaciones puntuales de eficacia para los subgrupos según la edad, el sexo, la raza, la etnia, el índice de masa corporal o la presencia de una afección subyacente asociada con un alto riesgo de complicaciones de Covid-19 también son altas. Para todos los subgrupos analizados en los que ocurrieron más de 10 casos de Covid-19, el límite inferior del intervalo de confianza del 95% para la eficacia fue más del 30%.
La incidencia acumulada de casos de Covid-19 a lo largo del tiempo entre los que recibieron placebo y la vacuna comienza a divergir 12 días después de la primera dosis, 7 días después de la mediana del período de incubación viral estimado de 5 días, lo que indica el inicio temprano de un efecto parcialmente protector de inmunización.
Comentarios
Para ver los comentarios de sus colegas o para expresar su opinión debe ingresar con su cuenta de IntraMed.






