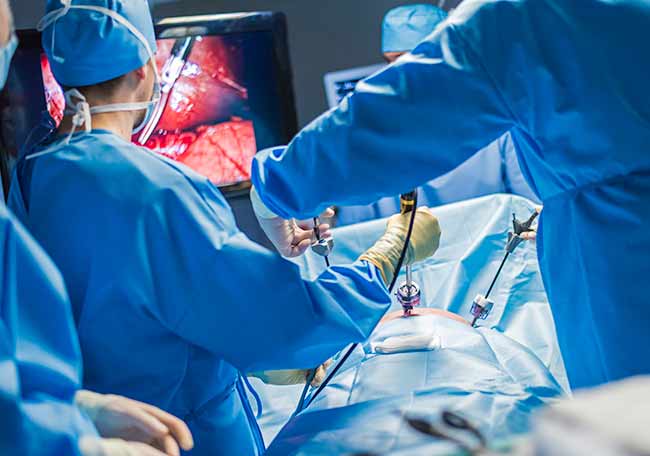
Resección laparoscópica vs abierta para metástasis hepáticas colorrectales
| Introducción |
El hígado es el sitio más común para el cáncer colorrectal (CCR) metastásico. A pesar de los avances en el tratamiento oncológico, la resección de las metástasis es aún la única opción curativa, con tasas de sobrevida a 5 años del 40% al 57% después de la resección de las metástasis hepáticas [1-3].
El uso de quimioterapia neoadyuvante ha incrementado la proporción de pacientes a los que se les puede ofrecer la resección hepática, mientras que los avances en las técnicas quirúrgicas y cuidados perioperatorios ha disminuido la mortalidad a 30 días de la cirugía hepática, desde el 24% en 1970 a menos del 2% en la actualidad [4-6].
Aunque la cirugía laparoscópica para el CCR primario está bien documentada y es ampliamente utilizada [7], la cirugía laparoscópica para las metástasis hepáticas ha tenido una lenta implementación [8]. Estudios previos han sugerido que la resección hepática laparoscópica es oncológicamente equivalente a la resección abierta, pero con ventajas a corto plazo en términos de menos complicaciones y reducción de la estadía y costos hospitalarios totales [9-19].
Un ensayo controlado randomizado de la resección hepática laparoscópica y abierta (Orange II, NCT 00874224) fue suspendido recientemente después de fracasar en el reclutamiento de pacientes [20]. Por lo tanto, las resecciones hepáticas laparoscópicas y abiertas no han sido comparadas nunca en un ensayo controlado y randomizado (ECR).
En el ensayo Oslo de resección hepática laparoscópica versus abierta para metástasis colorrectales (OSLO-COMET), los autores reportaron la tasa de complicaciones a 30 días, márgenes de resección y costo-beneficio en pacientes asignados al azar para ser sometidos a resección hepática abierta o laparoscópica.
| Métodos |
• Diseño del ensayo y supervisión
En este ensayo abierto, de superioridad, iniciado por el investigador, de un único centro asistencial, los autores asignaron al azar a pacientes para resección hepática laparoscópica (grupo experimental) o para resección abierta (grupo control). El ensayo fue diseñado por el comité de protocolo y realizado en el Hospital Universitario de Oslo, Noruega. El protocolo del ensayo ha sido publicado previamente [21] y aprobado por el Regional Ethical Committee of South Eastern Norway (REK Sør-Øst B 2011/1285) y la Data Protection Officer del Hospital Universitario de Oslo.
Los datos fueron recolectados por los autores, asistidos por asistentes de investigación que recibieron pago de los fondos del ensayo. Los autores analizaron los datos, escribieron el manuscrito, y avalaron la precisión de los análisis y la fidelidad del ensayo al protocolo. La South Eastern Norway Regional Health Authority financió el ensayo, pero no tuvo ningún rol en el diseño, recolección de datos, análisis de los datos, o escritura del manuscrito (identificación NCT01516710 en Clinicaltrials.gov).
• Pacientes
Los pacientes fueron elegibles para el ensayo si tenían diagnóstico de metástasis hepáticas de CCR que podían ser resecadas radicalmente mediante una resección hepática con preservación del parénquima, definida como una resección menor de 3 segmentos hepáticos consecutivos. Las resecciones múltiples fueron permitidas. Los pacientes con metástasis recidivadas después de una resección hepática previa (abierta o laparoscópica) fueron elegibles, así como los pacientes con metástasis pulmonares o en las suprarrenales resecables.
Los pacientes con otras metástasis extrahepáticas de CCR fueron excluidos, así como los pacientes programados para ablación concomitante, reconstrucción vascular o biliar, o resección sincrónica de un tumor primario. Un equipo multidisciplinario decidió la elegibilidad mediante la evaluación de la historia médica del paciente, tomografía computada (TC) de tórax y abdomen con contraste iodado, y resonancia magnética nuclear del hígado con gadoxetato disódico (Eovist, Bayer HealthCare). Todos los pacientes recibieron información escrita y oral sobre el ensayo, por uno de los investigadores, antes de brindar su consentimiento por escrito.
La secuencia de randomización fue generada con un programa creado específicamente para este ensayo. El programa fue diseñado y operado por el Departamento de Tecnología de la Información del Hospital Universitario de Oslo, y la secuencia de randomización fue archivada en una base de datos segura, accesible sólo por los investigadores.
La asignación de un procedimiento laparoscópico o abierto fue realizada aproximadamente 2 semanas antes de la cirugía. Los participantes no fueron informados del tipo de procedimiento hasta el día de la operación. Los pacientes elegibles fueron asignados al azar en una relación 1:1, para ser sometidos a resección hepática laparoscópica o abierta. No hubo estratificación.
• Procedimientos
Los pacientes recibieron quimioterapia de acuerdo con lo indicado en la reunión del equipo multidisciplinario, adhiriendo a las guías noruegas. Cuando se recomendó la quimioterapia neoadyuvante, la randomización fue realizada después de la evaluación de la respuesta radiológica. La indicación para la quimioterapia adyuvante fue la misma para ambos grupos.
Los pacientes recibieron información preoperatoria relacionada con la cirugía hepática y el ensayo por los investigadores del estudio (A.A.F y V.J.D), estandarizando de esa manera el manejo preoperatorio. Los pacientes siguieron un protocolo perioperatorio de vía rápida, que fue idéntico para ambos grupos. Las operaciones fueron programadas como parte de las listas quirúrgicas rutinarias del departamento, por lo que los cirujanos fueron asignados para las operaciones con base en la disponibilidad del departamento y de la complejidad del procedimiento.
Se suministró a los pacientes una única dosis intravenosa de doxiciclina (400 mg) y metronidazol (1,5 g) antes de comenzar la cirugía. Todas las operaciones fueron efectuadas o supervisadas por cirujanos consultantes especializados en cirugía hepato-pancreato-biliar, diestros en la técnica empleada. Los cirujanos podían cambiar la estrategia desde la resección con conservación del parénquima a la hemihepatectomía o ablación durante la cirugía, a su discreción, de ser necesario.
La técnica quirúrgica fue descrita en el protocolo [21], y la complejidad de los procedimientos fue evaluada usando versiones modificadas del Liver Surgery Complexity Score [22] y del sistema Iwate de puntaje [23]. Las modificaciones fueron realizadas de acuerdo con los autores de cada sistema de puntaje. El puntaje modificado incluyó el puntaje para la resección más compleja, con la adición de 1 punto por cada resección adicional que fuera necesaria.
• Resultado primario
Las complicaciones fueron registradas por un asesor “ciego” que estudió el sistema electrónico de documentación brindado por enfermería. Esos registros no incluyeron información sobre técnicas quirúrgicas, sino que en lugar de ello describían el estado postoperatorio del paciente en 3 reportes diarios. Los registros incluyeron también documentación de las entrevistas telefónicas entre el personal de enfermería y los pacientes, a 1, 8 y 28 días después del egreso.
Las complicaciones postoperatorias fueron registradas como una variable dicotómica (si/no) utilizando el sistema Accordion para calificar y definir [24]. Las complicaciones de Grado 1 son difíciles de registrar consistentemente, y a menudo tienen un impacto mínimo sobre la evolución postoperatoria. Por lo tanto, los autores enmendaron el protocolo para especificar que el resultado primario fue una complicación Grado 2 de Accordion o superior.
• Resultados secundarios
Las complicaciones fueron evaluadas también usando el Comprehensive Complications Index (CCI), que calcula todas las complicaciones que experimenta un paciente, dentro de un índice que va desde 0 a 100 [25]. El puntaje CCI registrado en este estudio, no obstante, fue modificado en comparación con la publicación original, porque las complicaciones de Grado 1 no fueron registradas en el ensayo y, por lo tanto, no fueron añadidas al cálculo del CCI.
Las conversiones a laparoscopía asistida con la mano o laparotomía, incidentes desfavorables intraoperatorios, duración de la cirugía, pérdida de sangre, transfusiones, y detalles sobre el procedimiento, fueron registradas en un formulario en papel. La pérdida de sangre fue documentada directamente por el cirujano principal después de la operación, basado en la cantidad de sangre en el recipiente del aspirador, más un estimado de la sangre en las compresas quirúrgicas. Cuando los pacientes fueron transferidos al hospital derivante para el cuidado postoperatorio, la duración de la estadía hospitalaria registrada incluyó la estadía en ambos hospitales.
Todos los especímenes resecados fueron enviados para evaluación histopatológica y de biobanco. Los márgenes de resección fueron evaluados macroscópicamente y microscópicamente por anatomopatólogos, y la presencia de células tumorales dentro de 1 mm del margen de resección fue definida como una resección R1.
• Seguimiento
Los pacientes fueron vistos ambulatoriamente por 1 de los investigadores a 1 y 4 meses del postoperatorio. Se realizó un examen clínico en ambas visitas y una TC toracoabdominal en la visita del 4º mes postoperatorio.
• Costos
Los costos se estimaron en una perspectiva de atención médica de 4 meses, con foco sobre los costos de las operaciones, costo de la estadía hospitalaria inicial y costos debidos a las complicaciones. El uso de recursos fue cuantificado principalmente usando los registros médicos de los pacientes.
Se realizó un estudio de microcostos para estimar los costos de las operaciones, y se usaron cuestionarios para los pacientes para evaluar el uso de recursos entre el mes y los 4 meses del seguimiento alejado. Los costos fueron estimados sobre la base de valor actual usando el dólar americano de 2014, con la tasa promedio de cambio en 2014 (1 USD = 6,3019 NOK).
• Calidad de vida relacionada con la salud
La calidad de vida relacionada con la salud (CdVRS) fue medida utilizando el formulario de 36 ítems Medical Outcomes Study Short Form (SF-36, versión noruega 2.0), en la línea de base y a los 1 y 4 meses del seguimiento alejado. Se calculó el SF-6D mediante un algoritmo de evaluación del Reino Unido, para estimar la CdVRS de los pacientes [26]. El SF-6D mide la CdVRS sobre una escala anclada en muerte (0) y salud perfecta (1), y está combinado con el tiempo, una medición de los años de vida de los pacientes ajustados por la calidad (AVAC).
• Análisis estadístico
Basado en los datos del departamento, los autores anticiparon una tasa de complicación del 27% en el grupo de cirugía abierta y una reducción potencial estimada del 13% en el grupo de cirugía laparoscópica [1]. Para mostrar esa diferencia o una mayor, con un intervalo de confianza (IC) del 95% y un poder de prueba de superioridad, era necesaria una muestra de 254 pacientes. Se esperó una tasa de abandono del 10% y se planificó incluir a 280 pacientes.
La tasa de complicaciones dentro de los 30 días fue comparada entre los 2 grupos de tratamiento usando una prueba Mid-P de Fisher para asociación. La diferencia entre las probabilidades del grupo de tratamiento de tener una complicación dentro de los 30 días (la diferencia de riesgo) fue estimada con un IC híbrido Newcombe de 95%.
Los resultados intraoperatorios y postoperatorios fueron analizados con una regresión mediana, que brindó un IC de 95% para la diferencia entre las medianas de los 2 grupos de tratamiento y un valor de P para la hipótesis nula de medianas iguales. Se usó una prueba de t de 2 muestras cuando la mediana no fue una medición relevante para comparar los grupos de tratamiento.
Las diferencias de costos fueron testeadas mediante un modelo lineal generalizado con una función de enlace del registro y distribución gama, y se estimó un IC de 95% como percentiles 2,5 y 97,5 usando un proceso de remuestreo con 10.000 repeticiones. Los valores de CdVRS perdidos fueron imputados mediante comparación predictiva de medias utilizando imputaciones múltiples con ecuación encadenada [27].
Las diferencias en la CdVRS y los AVAC fueron estimadas empleando pruebas t. Los AVAC fueron ajustados para las diferencias de base [28]. Se estimó una relación costo-beneficio incremental (RCBI) dividiendo la diferencia de costos por la diferencia de efecto de la cirugía laparoscópica y abierta, y se usó un umbral de disposición de pago de $95.000 [29]. La incertidumbre del RCBI fue estimada mediante remuestreo con 1.000 repeticiones.
De la muestra de remuestreo, aumentando los valores de umbral, se estimó tanto la probabilidad de la cirugía hepática laparoscópica como de la cirugía hepática abierta de ser costo-efectivas (curvas de aceptabilidad de costo-beneficio) y el valor individual esperado de la información perfecta (VEIP) [30]. El VEIP expresa el costo esperado de la incertidumbre, y cuantifica el valor máximo que la sociedad debería estar dispuesta a pagar, para eliminar la incertidumbre relacionada con la adaptación de la nueva tecnología (cirugía hepática laparoscópica), dado el conocimiento actual [31]. No hubo descuento debido a la perspectiva de corto plazo.
Comentarios
Para ver los comentarios de sus colegas o para expresar su opinión debe ingresar con su cuenta de IntraMed.