El hemostático de colágeno reduce el tiempo de hemostasia comparado con la celulosa

Introducción
En la cirugía de bypass arterial, es más difícil lograr la hemostasia, dado que las suturas d las arterias y de los injertos, y las anastomosis, deben ser cuidadosamente realizadas; frecuentemente, ello se efectúa bajo una alta dosis de medicación antiplaquetaria por las comorbilidades cardiovasculares. La falta de elasticidad del politetrafluoroetileno (PTFE), un material para el injerto del bypass ampliamente usado, cuando no hay disponible vena safena autóloga, puede causar sangrado por el orificio de la sutura, que puede ser controlado con éxito variado, mediante diferentes hemostáticos [1-5].
Los estudios preclínicos sugieren fuertemente que los hemostáticos de colágeno son más efectivos que aquellos hechos con celulosa regenerada oxidada [6]. Aunque ambos han sido usados clínicamente por muchos años, aun no se ha realizado una comparación clínica directa. Por lo tanto, el ensayo COBBANA (Control of bleeding after bypass anastomoses [control del sangrado después de anastomosis del bypass]) fue diseñado para mostrar la superioridad del colágeno microfibrilar en ese escenario quirúrgico.
Métodos
Para asegurar la transparencia, el protocolo de estudio del ensayo COBBANA ya ha sido registrado (www.clinicaltrials.gov), publicado [7] y aprobado en su versión final por el Comité de Ética del Landersärztekammer Hessen, Frankfurt, Alemania. Fue financiado y efectuado por Aesculap AG, Tuttlingen, Alemania. El Centro de Coordinación para Ensayos Clínicos (Koordinierungszentrum für Klinische Studien), Heidelberg, Alemania, fue responsable por el mantenimiento de la base de datos y por los datos biométricos. Los pacientes fueron enrolados en 1 centro en Alemania (Klinikum Hanau GmbH).
Objetivos del estudio
El objetivo primario de este ensayo fue mostrar que el Lyostypt (Aesculap AG, Tuttlingen, Alemania), un hemostático microfibrilar de colágeno, es más efectivo que el Surgicel (Johnson & Johnson Medical Ltd., North Yorkshire, UK), un hemostático de celulosa oxidada, para detener el sangrado por el orificio de sutura, después de la cirugía de bypass arterial. El objetivo final primario fue el tiempo de hemostasia, que fue determinado desde la liberación de la pinza hemostática, hasta el momento en que la herida estaba completamente o suficientemente seca, juzgado por un único investigador.
Para evaluar la seguridad del hemostático, las complicaciones (por ej., recidiva del sangrado, infección y oclusión de la prótesis de PTFE, estenosis, trombosis de la arteria de la pierna, reoperación, infecciones de la herida y desórdenes de cicatrización) dentro de los 30 ± 10 días después de la cirugía, fueron usadas como objetivos finales secundarios. La forma y moldeado del hemostático y su adherencia tisular son importantes para permitir una manipulación adecuada, lo que es esencial para el control del sangrado [5]. Por lo tanto, el número de hemostáticos requeridos, manipulación quirúrgica y adherencia (clasificada en términos de facilidad de uso), fueron evaluados como objetivos finales secundarios.
La base para los puntajes fue una escala de Likert modificada. Para la adherencia, fueron posibles las siguientes categorías: “adherencia inmediata”, “adherencia después de un breve tiempo”, “reposicionamiento” o “sin adherencia” y para la manipulación quirúrgica: “fácil colocación/sin necesidad de reposicionamiento”, “fácil colocación/reposicionamiento posible”, “dificultad de colocación-reposicionamiento/sin necesidad de producto adicional” o “colocación difícil (por ej., adherencia a los instrumentos o guantes)/necesidad de producto adicional”. Además, se registró la mortalidad postoperatoria dentro de los 30 días.
Elegibilidad e intervención
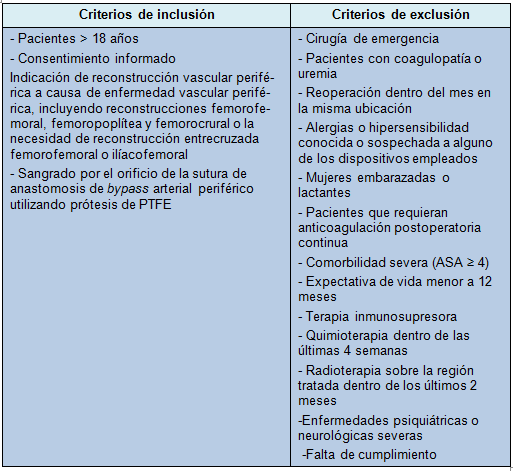
Los criterios de inclusión y exclusión (Tabla 1) y los procedimientos quirúrgicos, son descritos en detalle en el protocolo del estudio publicado [7]. Se obtuvo el consentimiento informado por escrito de todos los pacientes participantes.
• TABLA 1: Elegibilidad
Se usó el mismo procedimiento estándar en cada caso. No se usó vena safena en los pacientes participantes. En todos los pacientes randomizados se indicó el uso de una prótesis de PTFE. Se implantó una prótesis de PTFE con un diámetro de 6 u 8 mm usando material de sutura no absorbible (polipropileno; United States Pharmacopeia 5-0). El cirujano realizó primero la anastomosis distal. Luego liberó el clamp y controló el sangrado en la línea de sutura. Si la misma continuaba sangrado, cerraba el clamp y abría un sobre de randomización conteniendo el material en estudio. Luego removía el clamp en la anastomosis distal y aplicaba el hemostático randomizado, cortado por la mitad, alrededor de la anastomosis, durante 3 minutos controlados por cronómetro.
Observando la línea de sutura, se registró el tiempo requerido para lograr la hemostasia. Si no se la obtuvo en 3 minutos, se colocó otro hemostático del mismo tipo sobre la herida y se controló la hemostasia a los 5 y 10 minutos. Si la misma no se alcanzaba dentro de los 10 minutos o si se requería una intervención adicional, se consideró como fracaso del tratamiento. En la anastomosis proximal, se repitió el mismo procedimiento. El número y tipo de hemostáticos y el tiempo después de la remoción del clamp fueron registrados. Ambos dispositivos fueron removidos después de la hemostasia.
La pared arterial fue descrita como normal en 5 pacientes; en 23 pacientes, se registró una placa blanda y en 1 una placa calcificada. Todos los pacientes recibieron heparina (3.000 U) de manera estándar, independientemente del índice de masa corporal, pero sin protamina. Los hemostáticos, Lyostypt (5 x 8 cm) y Surgicel (5 x 7,5 cm) fueron usados.
El Lyostypt es un hemostático esterilizado con rayos x, absorbible, estable, hecho con colágeno de piel de ganado de una manada controlada en Alemania, sacrificado en mataderos controlados y tratado con hidróxido de sodio y acetona, para inactivar el agente productor de temblor (factor de reducción > 6 log10). Su biocompatibilidad fue demostrada en pruebas, de acuerdo con la norma ISO 10993.
Randomización
Se usaron sobres opacos sellados, numerados secuencialmente (1-32) para asignar a los pacientes, de acuerdo con una lista de randomización preparada por un estadístico, para recibir el colágeno microfibrilar (COLL) o la celulosa oxidada (ORC). Los pacientes fueron divididos en 4 grupos grandes iguales: grupo 1: COLL distal / ORC proximal; grupo 2: ORC distal / COLL proximal; grupo 3: ORC distal y proximal; grupo 4: COLL distal y proximal.
No se incluyó un grupo control sin tratamiento por la naturaleza del estudio y porque los estudios en animales han mostrado claramente que el tiempo de hemostasia aumenta si no se usa un hemostático [8-12]. Los productos hacen imposible la condición de ciego para el estudio.
Estimación del tamaño de la muestra
Este estudio utilizó un diseño en 2 etapas. Los tiempo de sangrado obtenidos de las evaluaciones preclínicas sirvieron como base para el cálculo del tamaño de la muestra (datos internos no publicados). Se estimó que sería necesario enrolar 28 pacientes. La comprobación fue realizada con un nivel de significación de α 1 = 0,0102. El número exacto dependió del número de pacientes con anastomosis sangrantes, por lo que se fueron sumando hasta que se registró 56 veces de aplicación randomizada del hemostático.
La prueba principal se llevó a cabo con los parámetros descritos en la sección de análisis estadístico. El ensayo iba a ser detenido por éxito, si se rechazaba la hipótesis nula con un valor de p de un solo lado, menor de α 1, y por futilidad si era mayor de 0,50. Para el análisis final, aplicando el abordaje de Bauer y Köhne [13], el nivel de significación fue establecido a α2 = 0,00380/p1.siendo p1 el valor de p de la prueba de un solo lado del objetivo final primario en el análisis interino. El nivel de significación fue mantenido en 0,025 y con un poder estadístico de 80%, los valores obtenidos por simulación basados en 300 repeticiones.
Análisis estadístico
Para evaluar el objetivo final primario, se usó la anastomosis como unidad observacional. El tiempo para la hemostasia, el objetivo final primario, limitado a 10 minutos, fue incluido como parámetro de respuesta en un modelo de regresión de falla acelerada del tiempo, asumiendo una distribución de Weibull [14,15] para el tiempo de sangrado, con los siguientes parámetros explicativos: tratamiento de la anastomosis (COLL/ORC), tratamiento de la anastomosis opuesta (COLL/ORC) y sitio de la anastomosis (proximal/distal). Los sujetos fueron incluidos como términos de fragilidad con una distribución logarítmica normal. La hipótesis nula formal, para ser comprobada con un nivel α = 0,025, fue la siguiente: “El tiempo de sangrado de la anastomosis bajo COLL es, al menos, tan prolongado como bajo ORC”.
El objetivo final primario fue analizado usando el PROC NLMIXED (SAS Institute Inc, Cary, NC, USA) con una distribución Weibull y usando a los sujetos como efectos aleatorios de distribución logarítmica normal. Se usaron pruebas exactas y de signo. La convergencia de problemas hizo imposible capturar la hemostasia a los 5 y 10 minutos, la tasa de complicación dentro de los 30 ± 10 días después de la cirugía y el número de hemostáticos adicionales requerido, según un modelo logístico mixto. Los sujetos fueron tratados como efectos aleatorios.
La facilidad de uso fue valorada sobre una escala de 4 puntos para la adherencia y de 5 puntos para la manipulación y modelado separadamente, utilizando un modelo lineal mixto con respuestas equidistantes. Ese modelo usó las mismas covariables que el modelo principal como efectos fijos y el cirujano y el sujeto como efectos aleatorios. Se registró cada evento adverso. Los pacientes fueron analizados usando el principio de intención de tratamiento.
Comentarios
Para ver los comentarios de sus colegas o para expresar su opinión debe ingresar con su cuenta de IntraMed.