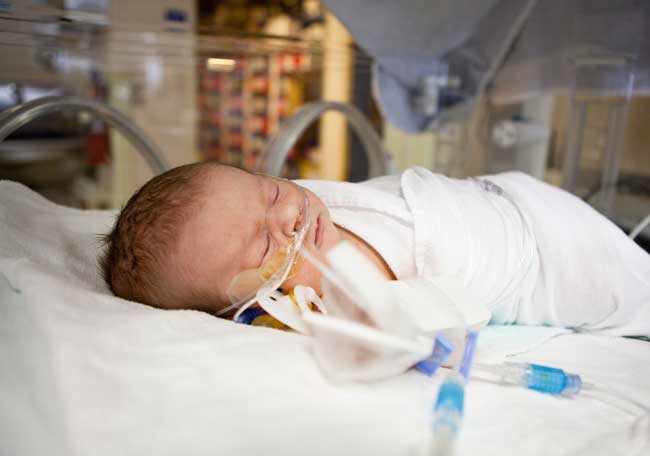
Enterocolitis necrotizante y transfusión de glóbulos rojos en prematuros

La enterocolitis necrotizante (ECN) sigue siendo una causa importante de morbilidad en recién nacidos prematuros hospitalizados. Aunque se han reconocido factores de riesgo para el desarrollo de ECN, que incluyen nacimiento prematuro y alimentación enteral, la etiología sigue siendo desconocida. Resultados de estudios recientemente publicados han sugerido una asociación entre la transfusión de concentrado de glóbulos rojos (CGR) y la ECN.
Existen varias razones biológicamente plausibles por las que las transfusiones de CGR pueden dar lugar a ECN, que incluyen la disminución en el óxido nítrico de los glóbulos rojos almacenados y una respuesta inmune intestinal exagerada a la transfusión de CGR. La anemia del prematuro y la transfusión de CGR son comunes en recién nacidos con muy bajo peso al nacer (MBPN). Debido a que no hay marcadores clínicos adecuados para la reducción del suministro de oxígeno a los tejidos, la decisión de transfundir CGR se basa por lo general en el criterio clínico y en la opinión de expertos. Es importante por lo tanto, para los médicos al cuidado de los recién nacidos prematuros, comprender los riesgos potenciales de la transfusión de CGR, incluyendo su posible asociación con ECN.
En este estudio, los autores platearon que los lactantes con MBPN que recibieron una transfusión de CGR tendrían un riesgo incrementado de desarrollar ECN. También se procuró determinar la tasa de ECN luego de la transfusión de CGR y caracterizar a los glóbulos rojos transfundidos que los niños recibieron antes de desarrollar ECN.
Métodos
Esta cohorte retrospectiva incluyó a lactantes con un peso de nacimiento <1500 g que ingresaron en el Hospital Christiana de Newark, Delaware, desde julio de 1993 hasta junio del 2007. Dicho hospital es el único con una Unidad de Cuidados intensivos Neonatales (UCIN) de nivel 3 en el estado de Delaware que ofrece atención a los niños nacidos en la institución (90%) y a los derivados. La atención neonatal en el estado de Delaware es regionalizada. Otras UCINs de nivel 3 dentro de la misma red sirven como centros de referencia para los niños con bajo peso al nacer si requieren atención quirúrgica. Los datos fueron obtenidos a partir de una base de datos informatizada y por revisión de los expedientes médicos. Toda la información fue ingresada en una base de datos por revisores entrenados, y fue controlada anualmente para detectar errores.
La edad gestacional (EG) se basó en la mejor estimación obstétrica. El examen de Ballard modificado se utilizó sólo si una estimación obstétrica no estaba disponible. El diagnóstico de ECN fue realizado por el equipo médico a cargo del niño y fue considerado sólo en los niños con estadio de Bell 2 o mayor. Los lactantes con ECN tuvieron signos sistémicos y radiográficos (neumatosis intestinal, aire venoso portal, o neumoperitoneo) de ECN. Se consideró ECN asociada a transfusión de CGR a todos los casos que se produjeron dentro de las 48 horas posteriores al inicio de la transfusión. La práctica de alimentación estándar incluyó el inicio de una nutrición enteral mínima después de alcanzar la estabilidad fisiológica. Se inició la alimentación en bolo con una frecuencia cada 3 horas y las cantidades fueron avanzando aproximadamente 20 ml/kg/día hasta llegar a un máximo volumen de 150 ml/kg/día. La leche materna fue utilizada como principal elección de la nutrición enteral. Se proporcionó leche de banco de donantes para los niños cuyas madres no suplían los requerimientos, y fórmula para prematuros para aquellos niños cuyas madres no dieron su consentimiento para la utilización de leche de banco. El porcentaje total de ingesta diaria de leche en la muestra de estudio que fue leche materna no pudo ser determinado. Los niños que fueron tratados con indometacina no recibieron alimentación oral durante el tratamiento y por un mínimo de 24 horas después de finalizar el tratamiento. Si los niños estaban recibiendo alimentación enteral, ésta no se interrumpió rutinariamente al iniciar la transfusión.
La decisión de transfundir CGR fue a discreción del neonatólogo a cargo del niño. Después de 1995, se utilizaron las guías de transfusión descriptas por Shannon y col. como parámetros generales. Todas las transfusiones de glóbulos rojos fueron citomegalovirus negativas, irradiadas, células falciformes-negativas, tipo específicas o de tipo O, Rh compatibles, y conservadas en adsol (Baxter Health Care Corp, Deerfield, IL). Todas las unidades conservadas tenían menos de 7 días de extraídas inicialmente, y se utilizaron hasta su fecha de expiración a los 42 días si fue necesario. Los glóbulos rojos fueron transfundidos a un volumen de 10 a 20 ml/kg durante 2 a 4 horas. Se administró furosemida a 1 mg/kg luego de la transfusión a discreción del neonatólogo tratante. En los niños que desarrollaron ECN en las 48 horas posteriores a la transfusión, se registraron los datos sobre el tiempo de extracción de la sangre transfundida, el hematocrito y el sexo de los donantes a partir de los registros del banco de sangre.
Las madres fueron clasificadas como receptoras de esteroides si recibieron alguna dosis de corticoides prenatales. La betametasona fue el esteroide utilizado más rutinariamente en la institución de los autores. La corioamnionitis clínica fue diagnosticada por el médico obstetra responsable en base a la presencia de fiebre, dolor uterino, y/o líquido amniótico fétido. Se diagnosticó preeclampsia de acuerdo con las Guías del Colegio Americano de Obstetricia y Ginecología. Antes del 2002, esta institución definió a la preeclampsia en base a un aumento de la presión arterial sistólica de 30 mm Hg o al aumento de la presión arterial diastólica de 15 mm Hg por encima de la línea de base con proteinuria. Después del 2002 la preeclampsia se definió como presión sistólica ≥ 140 mm Hg o diastólica ≥ 90 mm Hg luego de las 20 semanas de gestación con proteinuria definida como ≥ 0.3 g en una muestra de 24 horas.
Se cuantificó la severidad de la enfermedad de los lactantes utilizando el Score de Fisiología Aguda Neonatal (SFAN), basado en datos desde las 24 horas posteriores al nacimiento. Se realizó diagnóstico de ductus arterioso persistente (DAP) en los niños en base a los resultados ecocardiográficos. Los lactantes con DAP hemodinámicamente significativo fueron tratados con indometacina. Los niños con DAP hemodinámicamente significativo después de 2 cursos de indometacina se derivaron para ligadura quirúrgica del mismo. A los efectos de este estudio, se definió sepsis en base a hemocultivos positivos y signos y síntomas clínicos de bacteriemia. Se inició tratamiento con dopamina en los niños con hipotensión clínica significativa sin respuesta a bolos de líquido. Los neonatólogos a cargo administraron corticoides postnatales a los niños que fueron desarrollando enfermedad pulmonar crónica y a los que tenían un gradiente alvéolo-arterial de oxígeno empeorado sin respuesta a diuréticos y broncodilatadores.
Los análisis estadísticos incluyeron análisis univariables y multivariables. El análisis univariable incluyó test de x2 para las variables categóricas y análisis de varianza para las variables continuas con distribución normal. El test de Levene de homogeneidad de varianzas se utilizó para evaluar la distribución de datos. Se utilizó el test U de Mann- Whitney para las variables contínuas sin distribución normal. El análisis multivariable incluyó regresión logística. Las variables independientes en los modelos multivariables incluyeron aquellos con un valor de p < 0.15 en el análisis univariable. Un valor de p < 0.05 fue considerado estadísticamente significativo.
Resultados
Un total de 2.311 recién nacidos con MBPN fueron admitidos en la UCIN durante el periodo de estudio y constituyeron la muestra de estudio. De estos niños, un total de 122 (5.3%) desarrollaron ECN y 35 de éstos (28.7%) requirieron una intervención quirúrgica para la misma. La tasa anual de ECN no cambió durante el período de estudio. Los niños que desarrollaron ECN tenían menor edad gestacional y menor peso de nacimiento, eran más tendientes a ser varones, y menos propensos a ser nacidos de una madre con preeclampsia en comparación con los lactantes que no desarrollaron ECN. No se encontraron diferencias en la severidad de la enfermedad con el nacimiento, la etnia, la condición innata, la gestación múltiple, la corioamnionitis clínica, los corticoides prenatales, los antibióticos en atención prenatal, y la administración de magnesio e indometacina prenatales en los niños con y sin ECN.
No hubo diferencias en las puntuaciones de Apgar al minuto y a los 5 minutos en los niños que desarrollaron ECN en comparación con aquellos que no la desarrollaron. Los lactantes que desarrollaron ECN requirieron un curso más prolongado de ventilación mecánica, tuvieron mayor probabilidad de recibir surfactante, tuvieron una mayor ocurrencia de DAP y una mayor incidencia de sepsis, y recibieron corticoides postnatales con mayor frecuencia en comparación con los niños sin ECN. No hubo diferencias en el tratamiento con ligadura del DAP entre los grupos. Los niños que desarrollaron ECN fueron más tendientes a recibir una transfusión de CGR y un mayor número de transfusiones en comparación con aquellos que no desarrollaron ECN. Los lactantes que recibieron una transfusión de CGR tuvieron mayores probabilidades de desarrollar ECN de acuerdo con los análisis ajustados y no ajustados. Se crearon varios modelos multivariables diferentes. El primer modelo no incluyó otros diagnósticos postnatales, incluyendo DAP y sepsis, debido a que estas variables pueden ser parte de la vía causal con la ECN y pueden influir en la decisión de administrar transfusiones de glóbulos rojos. El segundo modelo incluyó al DAP y la sepsis y los resultados se mantuvieron sin cambios. Por último, para tener en cuenta cualquier forma de asociación temporal potencial entre las transfusiones de CGR y la ECN, los modelos se llevaron a cabo después de la exclusión de datos sobre las transfusiones administradas luego de un diagnóstico de ECN. Después que los datos de estas transfusiones fueran excluidos, la probabilidad de desarrollar una ECN se mantuvo elevada en los niños que recibieron CGR. Ninguno de los modelos multivariados se controló por el hematocrito. Los autores no controlaron el hematocrito debido a que cada niño en la muestra de estudio tenía múltiples mediciones. Los hematocritos fueron medidos en forma intermitente a discreción clínica, y la naturaleza de la relación entre hematocrito bajo y transfusión fue colineal.
La cohorte en estudio recibió un total de 2315 transfusiones de CGR. Se desarrolló ECN en el plazo de 48 horas después del 1.4% (33 de 2315) de estas transfusiones, lo que representó el 27% (33 de 122) de todos los casos de ECN. Por el contrario, el 24% (30 de 122, p= 0.61) del total de casos de ECN se produjeron en niños que nunca recibieron una transfusión. En los restantes 59 casos de ECN, los niños recibieron transfusiones de CGR pero no en las 48 horas precedentes al diagnóstico. En este último grupo, el intervalo entre la transfusión de CGR y el diagnóstico de ECN fue de 11.2 +/- 11.3 días.
Los lactantes que desarrollaron ECN en las 48 horas posteriores a la transfusión tuvieron un menor peso al nacer y una menor edad gestacional en comparación con los que desarrollaron ECN y nunca recibieron una transfusión. Además, los niños que desarrollaron ECN en el plazo de las 48 horas después de la transfusión llegaron a una alimentación completa en un momento posterior y desarrollaron ECN a una edad más tardía que los niños que desarrollaron ECN y nunca recibieron una transfusión. No hubo diferencias en la edad gestacional, peso de nacimiento, días de alimentación enteral total, o edad al diagnóstico de ECN entre los niños en los que se produjo ECN en las 48 horas después de la transfusión y los niños en los que la ECN ocurrió > 48 horas después de la transfusión. No hubo diferencias en el hematocrito o en la proporción de niños que no estaban recibiendo nutrición oral en el momento de la transfusión en recién nacidos con ECN con inicio dentro de las 48 horas de la transfusión en comparación con aquellos con ECN > 48 horas después de la transfusión. No hubo diferencias en la tasa de ECN quirúrgica entre los 3 grupos. Se compararon las características de la sangre transfundida (sexo del donante y fecha de extracción de la sangre) administrada a los niños que desarrollaron ECN dentro de las 48 horas de la transfusión de CGR con las de la sangre transfundida a niños que desarrollaron ECN > 48 horas después de la transfusión. Los donantes fueron más tendientes a ser hombres, pero no hubo diferencias en el tiempo de extracción de la sangre administrada a los niños con ECN con inicio dentro de las 48 horas después de la transfusión en comparación con la sangre administrada a los niños con ECN de inicio > 48 horas después de la transfusión.
Comentarios
Para ver los comentarios de sus colegas o para expresar su opinión debe ingresar con su cuenta de IntraMed.