Imagen quirúrgica mejorada

Introducción
La implementación de la cirugía mínimamente invasiva ha aumentado rápidamente en la última década. Muchos procedimientos son ahora realizados casi exclusivamente por vía laparoscópica. Los partidarios de la cirugía laparoscópica citan los riesgos reducidos de infección, estadía hospitalaria más corta, retorno laboral más precoz y mejor cosmética, como incentivos [1,2].
Los procedimientos mínimamente invasivos resultan en una pérdida de la retroalimentación táctil y de la valoración tridimensional para el cirujano. La laparoscopía tiene una curva empinada de aprendizaje y el aumento en las tasas de complicaciones es común al principio de la experiencia del cirujano. A medida que las indicaciones para la cirugía laparoscópica se expanden, muchos procedimientos complejos requieren de un entrenamiento avanzado adicional. Las nuevas tecnologías pueden aliviar algunas de las cargas del entrenamiento y mejorar la seguridad durante la laparoscopía.
La espectroscopia de reflectancia visible (ERV) es una modalidad comprobada para el monitoreo no invasivo de la oxigenación tisular [3-9]. La espectroscopia toma ventaja de las propiedades espectrales únicas de la hemoglobina, para inferir la oxigenación de los tejidos. La ERV es posible con una cámara 3-CCD¨, que es estándar en las torres laparoscópicas en la sala de operaciones. En este estudio, los autores usaron la respuesta espectral de una cámara 3-CCD para diferenciar los vasos renales y para monitorear la oxigenación del parénquima renal durante nefrectomías laparoscópicas realizadas a donantes (NLD) y nefrectomías laparoscópicas parciales (NLP).
Métodos
Pacientes y procedimientos
Se obtuvo un consentimiento informado de todos los pacientes que fueron sometidos ya sea a NLD (n = 15) o a NLP (n = 10). Todos los pacientes participaron con un protocolo aprobado por el Institutional Review Board . La pérdida de sangre promedio estimada para la NLD y la NLP fue de 435 ± 306 y 275 ± 241 ml, respectivamente. Los tiempos operatorios, incluyendo la anestesia, fueron de 364 ± 81 minutos para la NLD y 471 ± 51 minutos para la NLP. En promedio, se administró > 5 L de Ringer lactato para cada paciente.
Mejora de la imagen de 3-CCD
Todas las nefrectomías fueron grabadas en un DVD-R usando una torre laparoscópica de Storz equipada con una cámara 3-CCD. Un laparoscopio estándar de 10 mm y 30° fue usado en todos los pacientes. El material de video obtenido en la sala de operaciones fue transferido desde el DVD a una computadora personal, en donde se realizaron todos los análisis subsiguientes. Los videos fueron grabados en el Adobe Premier 6.0 para revisar el material y extraer cuadros individuales conteniendo la exposición de la estructura hiliar o la exposición del parénquima renal o ambas, como imágenes TIF (tagged image format). Primero, la imagen extraída (Fig. 1A) es descompuesta en las respuestas individuales a las señales de CCD. Después, la respuesta de señal CCD azul (Fig. 1C) es sustraída de la respuesta de señal CCD roja (Fig. 1B). La imagen resultante (Fig. 1D) es coloreada de manera que un color rojo intenso denota la mayor oxigenación tisular y un color azul intenso indica la falta de oxigenación tisular. Finalmente, la imagen calculada es superpuesta sobre la imagen original extraída (Fig. 1E) permitiendo el registro visual y su mejora simultáneamente.
• FIGURA 1: (A) Imagen laparoscópica original extraída del material de video de la operación. La engrampadora está en la base de la arteria y la vena está inmediatamente a la derecha de la arteria. (B) Imagen en escala de grises en formato TIF de la respuesta roja del CCD. (C) Imagen TIF en escala de grises de la respuesta azul del CCD. (D) Imagen calculada (respuesta CCD roja menos respuesta CCD azul). La vena y arteria son indicadas por líneas de puntos amarillos. (E) Imagen mejorada consistente en la imagen calculada superpuesta a la imagen laparoscópica original.
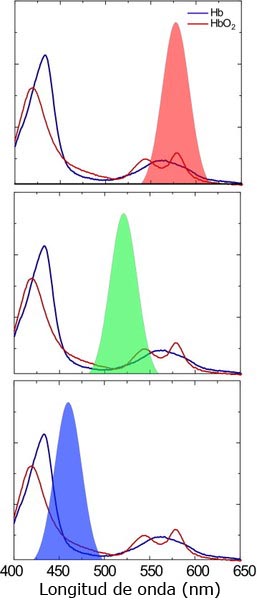
Las diferencias en las regiones oxigenadas y desoxigenadas del tejido son detectables debido a la absorción inherente de hemoglobina en la región visible del espectro electromagnético. La hemoglobina oxigenada tiene bandas de absorción mayores a 416, 541 y 577 nm y la hemoglobina desoxigenada tiene bandas de mayor absorción a 430 y 556 nm. Las respuestas individuales del CCD actúan como filtros para 3 regiones diferentes del espectro visible (Fig. 2). Mediante la sustracción de la respuesta a la señal CCD azul de la señal de respuesta CCD al rojo, los autores amplificaron efectivamente las diferencias de absorción entre la sangre oxigenada y desoxigenada en los tejidos [9]. Existe una correlación directa entre los valores de intensidad promedio de la región de interés (RDI) y la saturación de oxígeno de la sangre y la oxigenación tisular [10].
♦ CCD: siglas en inglés de charge-coupled device, dispositivo de cargas (eléctricas) interconectadas. Es un circuito integrado con un número determinado de condensadores enlazados o acoplados y constituye uno de los elementos principales de las cámaras fotográficas y de video digitales. Las cámaras con 3-CCD tienen 3 dispositivos acoplados de carga eléctrica separados, cada uno de los cuales toma una medida separada de luz roja, verde y azul (RDA).
• FIGURA 2: Espectro de absorción visible de la hemoglobina oxigenada y desoxigenada (HbO2 y Hb, respectivamente) con la superposición de las respuestas estimadas individuales del dispositivo CCD (rojo, verde y azul, desde arriba hacia abajo).
Por cada cuadro extraído, los valores promedio de intensidad fueron calculados para las RDI, esto es, áreas con una exposición hiliar o renal adecuada y resplandor mínimo. Las RDI consistieron en rectángulos conteniendo ~ 30 a 44.000 pixeles, y al menos tres RDI fueron examinadas por cada cuadro. El tamaño variable del rectángulo se atribuyó a la orientación cambiante del riñón a través de la operación, junto con los cambios en la iluminación.
Análisis estadístico
Las diferencias entre los valores promedio de intensidad de la RDI fueron evaluados utilizando la prueba de t de Student. Para las imágenes de los vasos, en donde la misma condición de imagen existía tanto para la arteria como para la vena, se usó una prueba de t para medias de muestras apareadas. Para las imágenes del parénquima renal, en donde la orientación del riñón había cambiado después del clampeo de los vasos, se empleó una prueba de t de dos colas no apareada asumiendo varianzas iguales. Las diferencias medias fueron consideradas significativas con un valor de p < 0,05; las diferencias con una p < 0,01 fueron consideradas estadísticamente significativas.
Resultados
Resultados espectroscópicos
Diferenciación de los vasos
El valor promedio global de la RDI calculado para la vena renal, 45,96 ± 8,65, fue significativamente diferente del valor medio de intensidad de la RDI calculado para la arteria, 68,40 ± 8,44 (p = 8,0 x 10-8). Como se muestra en la Figura 3, una comparación de los valores promedio de intensidad de la RDI de las arterias renales y de las venas renales para cada paciente reveló una diferencia significativa entre esos 2 valores (p < 0,05). En efecto, el valor umbral para la discriminación del tipo de vaso (venoso o arterial) puede ser calculado tomando el valor promedio de intensidad de la RDI de la vena más 1 DE (desvío estándar) y el valor promedio de intensidad de la RDI de la arteria menos 1 DE; se determinó que era de 59,00. Un vaso con un valor promedio de intensidad de la RDI > 59,00 podría ser categorizado como una arteria y cualquier vaso con un valor de intensidad promedio de la RDI < 59,00 podría ser categorizado como una vena. Los autores luego validaron el uso de este abordaje con 2 pacientes exhibiendo vasos accesorios.
• FIGURA 3: Valores promedio de intensidad de las regiones de interés (RDI) para arterias y venas en 15 nefrectomías.
Las Figuras 4A y B muestran 2 pacientes con múltiples vasos (NLP y NLD, respectivamente), con las venas y arterias claramente marcadas. Los vasos adicionales fueron identificados durante las nefrectomías por un cirujano laparoscopista experimentado, pero fueron usados para ilustrar la posibilidad de una rápida identificación en vivo de los vasos. En ambos pacientes, las imágenes mejoradas (Figs. 4C y 4D) superponen un color rojo sobre los vasos adicionales, indicando oxigenación y, por lo tanto, que son arterias. La identificación de los vasos es confirmada luego usando los valores de intensidad promedios de la RDI. Las RDI para cada vaso son perfiladas con rectángulos en blanco (vena), amarillo (arteria izquierda) y verde (arteria derecha). En el primer paciente (Figs. 4A y C), los valores promedio de intensidad de la RDI son 48,25 ± 1,30, 61,65 ± 2,32 y 66,91 ± 6,47, para la vena, arteria izquierda y arteria derecha, respectivamente. Los valores calculados asignaron correctamente cada vaso y una comparación de los vasos reveló una diferencia significativa entre la vena y las arterias izquierda y derecha (p = 0,007 y p = 0,025, respectivamente). Resultados similares se vieron en el segundo pacientes (Figs. 4B y D), con valores de intensidad promedio de la RDI de 43,35 ± 3,34, 65,14 ± 5,61 y 60,68 ± 4,85, para la vena, arteria izquierda y arteria derecha, respectivamente. Además, se hallaron diferencias estadísticamente significativas cuando se comparó la vena con las arterias izquierda y derecha (p = 0,007 y p = 0,0017, respectivamente.
• FIGURA 4: (A) Imagen laparoscópica de los vasos renales extraída del material de video de una nefrectomía parcial. Se observa la presencia de múltiples arterias. (B) Imagen 3-CCD mejorada de la vena y las arterias. Se observa la vena claramente sombreada en azul y las arterias en rojo. (C) Imagen laparoscópica de los vasos renales extraída del material de video de una nefrectomía a un donante. (D) Imagen 3-CCD mejorada que muestra claramente la vena en azul y las arterias en rojo. En ambos pacientes, las RDI usadas para los cálculos de los valores promedio de intensidad están indicadas con rectángulos en blanco, amarillo y verde (vena, arteria izquierda y arteria derecha, respectivamente).
.jpg)
Oxigenación parenquimatosa
Además de la identificación de los vasos, los valores promedio de intensidad de la RDI fueron calculados para comparaciones del parénquima renal antes de la oclusión vascular (sin isquemia) y después de la misma (con isquemia) para los 10 pacientes con NLD. El tiempo de clampeo vascular antes de la extracción del riñón varió desde 30 segundos a 2 minutos. Está claro en la Figura 5 que los valores de intensidad promedio de la RDI cambian drásticamente después de inducir la isquemia, aún después de sólo 30 segundos de isquemia (paciente 5). Las diferencias porcentuales en los valores promedio de intensidad de la RDI para las imágenes pre y post clampeo no son proporcionales al tiempo de clampeo de los vasos o a los niveles preoperatorios del clearence de creatinina. Los resultados preliminares indican que la imagen 3-CCD mejorada puede ser usada no sólo para identificar vasos accesorios sino también para monitorear la oxigenación del parénquima renal en vivo.
• FIGURA 5: Valores promedio de intensidad de la RDI calculados para el parénquima renal antes del clampeo de los vasos (negro) y después (gris) para cada nefrectomía laparoscópica de paciente donante. * p < 0,05; ** p < 0,01
Discusión
Este artículo es el primer reporte del uso de la mejora visual con 3-CCD para la diferenciación / identificación de los vasos sanguíneos. Además, esta técnica es usada para la evaluación de la oxigenación del parénquima renal durante la cirugía laparoscópica, específicamente durante NLP y NLD. Aunque esta técnica es presentada para las nefrectomías laparoscópicas, su uso potencial se extiende a todos los aspectos de la cirugía laparoscópica y abierta. Los autores presentan un método nuevo, no invasivo, capaz de monitorear la oxigenación tisular intraoperatoria en vivo, que no requiere la incorporación de equipamiento adicional en la sala de operaciones laparoscópica.
Han usado el análisis de la imagen 3-CCD mejorada para los vasos no linfáticos, logrando un valor umbral para la identificación de los mismos (Fig. 3). Un valor promedio de intensidad de RDI > 59,00 indica la presencia de una arteria y uno < a 59,00 la presencia de una vena. Cuando se aplicó a 2 pacientes sometidos a nefrectomía laparoscópica (Fig. 4) se encontraron vasos accesorios durante la disección del hilio renal que fueron identificados como arterias. Los resultados de los cálculos fueron validados por los cirujanos laparoscopistas que realizaron las nefrectomías; no habiendo revelado los cálculos, los vasos fueron correctamente identificados.
Los autores también examinaron el parénquima renal durante las 10 NLD; la imagen 3-CCD mejorada fue capaz de monitorear los valores relativos de oxigenación durante el procedimiento. Una clara caída en los valores promedio de intensidad de la RDI se observó (Fig. 5), aún con tiempos de isquemia tan cortos como 30 segundos. La imagen 3-CCD mejorada demostró la habilidad para monitorear cambios sutiles en la oxigenación del parénquima renal [10]. Aunque todas las diferencias fueron significativas, variaron para cada paciente. Esto puede ser consecuencia de variables en las imágenes, tales como la iluminación laparoscópica, la orientación del riñón y la exposición. La fisiología intrínseca renal puede también afectar los valores de oxigenación parenquimatosa. Esto se hizo aparente con la pérdida de correlación entre los valores promedio de intensidad de RDI y el tiempo de isquemia o el clearence de creatinina preoperatorio del donante.
La popularidad de la NPN y la NLP ha crecido desde su introducción en la década de 1990 [11-14]. La realización de estos procedimientos requiere entrenamiento especializado y un alto nivel de habilidad técnica [15]. En particular, la diferenciación e identificación de los vasos en laparoscopía, sin la ayuda de la retroalimentación táctil, puede ser desafiante. La tasa global de complicaciones para la NLD es de aproximadamente 2,8% y la mayoría están relacionadas con el sangrado [16]. En un estudio de comparación de NLD con arterias renales múltiples y NLD con una única arteria, Singh y col. [17], especulan sobre si la imagen preoperatoria actual es suficiente para identificar a las arterias renales múltiples. En efecto, todas las complicaciones hemorrágicas en este estudio se originaron en una arteria accesoria pasada por alto. La habilidad mejorada para identificar la anatomía vascular aberrante en un campo bi-dimensional puede disminuir las complicaciones hemorrágicas. Esta tecnología también puede ayudar a los cirujanos laparoscopistas a preservar una adecuada longitud de los vasos, un componente crítico en las nefrectomías laparoscópicas de los donantes [18]. Además, también podría reducir el tiempo aumentado de isquemia caliente y las consecuentes complicaciones ureterales asociadas con las NLD con arterias múltiples [19].
Los métodos actuales para la identificación y diferenciación de los vasos en la laparoscopía están limitados a evidencias visuales (por ej., color y pulsaciones). Esto es altamente subjetivo y depende de la experiencia del cirujano. La ecografía Doppler intraoperatoria puede ser usada pero también requiere equipamiento y personal especializados. Los cirujanos vasculares han usado la flujometría Doppler con láser [20] y el muestreo venoso [21] para investigar la adecuada perfusión y oxigenación de los tejidos, respectivamente. Estos métodos no se han adaptado al escenario laparoscópico y son limitados, porque no permiten imágenes en tiempo real. Los métodos desarrollados para la identificación de los vasos específicamente durante la cirugía laparoscópica incluyen un detector endoscópico de pulsos [22] e imágenes con infrarrojo [23]. Ambos métodos requieren equipamiento adicional que debe ser incorporado en un ya abarrotado espacio operatorio. Los autores proponen un medio nuevo de investigación intraoperatoria para la diferenciación e identificación vascular que no requiere equipamiento adicional y que le brinda a los cirujanos una forma cuantificable para la identificación y distinción entre los vasos sanguíneos.
La espectroscopia de reflectancia visual tiene claramente un amplio rango de potenciales aplicaciones en operaciones laparoscópicas y a cielo abierto. Por ejemplo, los cirujanos de transplante actualmente confían mucho en los signos visuales para determinar la capacidad funcional de un implante renal durante las operaciones y en la diuresis. Se ha señalado que los métodos usados en la actualidad para la evaluación clínica de la isquemia están subvaluados, brindando menos que deseables sensibilidades y especificidades [24]. Los métodos para evaluar la isquemia renal mediante el monitoreo serológico y urinario no son inmediatos ni están fácilmente disponibles durante un procedimiento quirúrgico. Los niveles cuantificables de oxigenación orgánica total, un verdadero indicador de la isquemia, ofrecidos en tiempo real al cirujano de transplante pueden brindar datos críticos en la sala de operaciones para maximizar la función del implante. De aquellos estudios que intentaron la medición de la oxigenación final del órgano, oxímetros [21] y sondas espectrofotométricas [25] han sido usados y se encontró que eran inefectivos o que brindaban sólo una muestra limitada de la oxigenación tisular. Muchas tecnologías usadas por otras especialidades miden el flujo a un órgano y no realmente la oxigenación tisular [26-30]. La 3-CCD mejorada permite una valoración intraoperatoria cuantificable de la oxigenación renal y podría brindar datos críticos sobre el aporte sanguíneo al riñón.
Otros ejemplos en donde la 3-CCD mejorada puede aumentar la seguridad y facilidad del procedimiento incluyen la colectomía, esplenectomía y reparación herniaria inguinal laparoscópicas. Las resecciones colónicas laparoscópicas tienen una gran demanda debido a la disminución en el tiempo de retorno de la función intestinal y de los requerimientos analgésicos y la mejora de los resultados estéticos [33-35]. De manera similar a la cirugía colónica, la cirugía laparoscópica está suplantando a la esplenectomía a cielo abierto en pacientes seleccionados [36,37]. Al igual que en las colectomías laparoscópicas, la diferenciación de los vasos y la evaluación parenquimatosa durante esta operación son elementos clave. Finalmente, la identificación de los vasos durante la reparación laparoscópica de la hernia inguinal podría ser una ayuda útil en esta operación comúnmente efectuada.
El rol de la 3-CCD mejorada también puede ser empleado en la cirugía abierta. Los cirujanos vasculares, durante las reparaciones abiertas o endovasculares de los aneurismas aórticos abdominales han buscado maneras de detectar intraoperatoriamente la colitis isquémica antes de completar el procedimiento [20,21,25,38]. Una tecnología similar está siendo investigada por los cirujanos cardíacos para evaluar la permeabilidad del implante intraoperatoriamente durante el bypass coronario [26-28]. Las imágenes infrarrojas han sido investigadas en la cirugía cardíaca, pero esta técnica no brinda realmente valores de saturación de oxígeno [27,28].
En conclusión, los resultados obtenidos por los autores demuestran la capacidad ventajosa de las imágenes 3-CCD mejoradas durante la nefrectomía laparoscópica. Con las actuales cámaras laparoscópicas que ya tienen los chips de 3-CCD, se garantiza la ausencia de costos en equipamiento, permitiendo una sencilla integración dentro del armamento de los cirujanos laparoscopistas. Las técnicas aquí presentadas permiten un análisis cuantitativo en tiempo real de la oxigenación y una evaluación de la isquemia e identificación de la anatomía vascular. A medida que más casos son abordados laparoscópicamente, los avances en la tecnología de imágenes son necesarios para facilitar la incorporación de la laparoscopía en un rango más amplio de procedimientos. Las aplicaciones de la 3-CCD mejorada continuarán creciendo a medida que los cirujanos apliquen esta tecnología en beneficio de sus pacientes y mejora de los resultados.
Comentarios
Para ver los comentarios de sus colegas o para expresar su opinión debe ingresar con su cuenta de IntraMed.