Polimialgia reumática
► Introducción
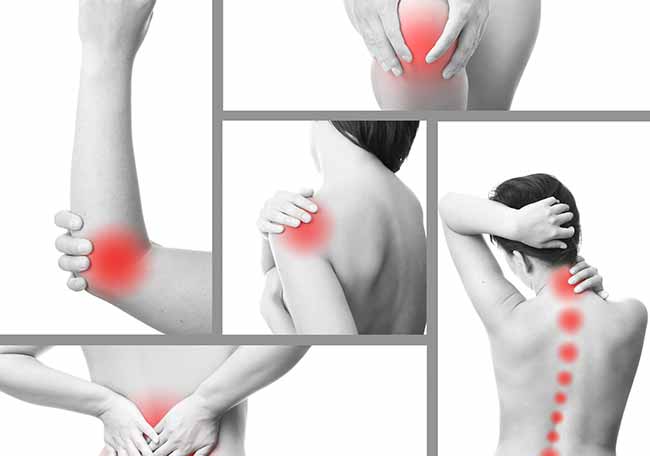
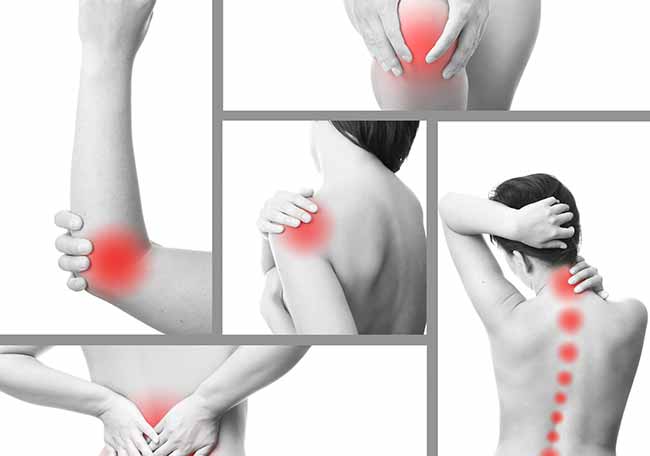
| La polimialgia reumática (PR) es un trastorno inflamatorio caracterizado por dolor intenso y rigidez en los hombros y la porción proximal de ambos brazos. El dolor y la rigidez también son comunes en el cuello. Con menor frecuencia, estos síntomas afectan la cintura pelviana y la porción proximal de los muslos. Los pacientes tienen rigidez matinal que dura más de 45-60 min y síntomas inespecíficos como fatiga y malestar. En esta enfermedad, es característico el aumento de los reactantes de fase aguda: velocidad de eritrosedimentación (VSG) y proteína C-reactiva. |
Bruce describió por primera vez esta condición en 1888. La PR, también es conocida como fibrositis secundaria, periartrosis húmeroescapular, reumatismo extra articular, síndrome miálgico de los ancianos, seudopoliartritis rizomélica y enfermedad artrítica reumatoidea─descrita por primera vez en la década de 1940. El término PR fue introducido en 1957.
►Epidemiología: incidencia, componentes genéticos y factores ambientales
La PR es una enfermedad común en los pacientes ancianos y rara vez se presenta en personas <50 años. Más de dos tercios de los pacientes son mujeres. La incidencia aumenta progresivamente con la edad en ambos sexos hasta los 80 años. La incidencia más elevada se halla en personas >65 años, con un pico entre los 70 y los 79 años.
Es más común en los países escandinavos. La incidencia media anual de PR en personas >50 años fue de 50 casos/100.000 habitantes en Gotemburgo, Suecia, entre 1985 y 1997. Cabe destacar que el condado de Olmsted, en Minnesota, EE. UU., donde la población desciende principalmente de escandinavos o europeos del norte, tiene las tasas de incidencia de PR más elevadas. En 2016, el condado de Olmsted tuvo una incidencia anual ajustada por la edad y el sexo en personas >50 años de 63,9 casos/100.000 habitantes.
La prevalencia general ajustada por la edad y el sexo entre 2015 y 2017 en el condado de Olmsted fe de 701 casos/100.000 personas (870 en mujeres y 508 en hombres/100.000 habitantes). La prevalencia de PR también es mayor en las poblaciones del norte de Europa e individuos escandinavos que en otras poblaciones. La menor incidencia se observa en Europa meridional.
La susceptibilidad a la arteritis de células gigantes, una vasculitis también común en las personas mayores y que a menudo se asocia con la PR, tiene relación con las moléculas HLA de clase I y II. A menudo, en los pacientes con PR se observa una asociación entre los alelos HLA-DRB1*04 clase II y la presencia de arteritis de células gigantes; esta asociación no parece existir en todos los pacientes con PR aislada. Los polimorfismos genéticos asociados a otras condiciones inflamatorias autoinmunes como los polimorfismos en la región promotora del gen de la interleucina 6 (IL-6) también podrían influir en el desarrollo de la PR.
En la patogénesis de la PR pueden estar implicados los agentes infecciosos. Esta hipótesis se apoya en los picos simultáneos que muestran la incidencia de arteritis de células gigantes y de PR en diferentes regiones de Dinamarca, como ocurrió en concomitantemente con las epidemias de Mycoplasma Pneumoniae, Parvovirus B19 y Chlamydophila neumoniae. Sin embargo, en un estudio prospectivo de 4 años no se halló asociación entre la infección por Parvovirus B19 y la PR. En el Reino Unido se ha hallado una modesta asociación entre cualquier infección o la infección por herpes zoster y el desarrollo de arteritis de células gigantes.
► Fisiopatología
Los estudios artroscópicos de pacientes con PR hallaron una sinovitis leve en las articulaciones proximales (principalmente hombros). El infiltrado inflamatorio encontrado en las membranas sinoviales del hombro y otras articulaciones afectadas estaba compuesto principalmente por macrófagos y linfocitos T CD4.
Esta sinovitis leve no explica por completo las manifestaciones musculoesqueléticas y el dolor difuso en las estructuras periarticulares. En vista de el compromiso inflamatorio prominente de las bolsas, algunos autores han sugerido que la PR podría ser un trastorno que afecta sobre todo a las estructuras sinoviales extraarticulares.
Los estudios de resonancia magnética (RM) y ecografía han revelado la presencia de bursitis subacromial y subdeltoidea y tenosinovitis del bíceps en asociación con la sinovitis de las articulaciones glenohumerales. Aunque el derrame de la articulación de la cadera es más común que la bursitis peripélvica, en la PR puede ocurrir cualquiera de ellos o ambos. La bursitis trocantérea, y con menor frecuencia la bursitis iliopsoas e isquioglútea también puede ocurrir como parte del espectro de la enfermedad.
Sin embargo, la bursitis isquioglútea es bastante específica de la PR. La bursitis interespinosa de la columna cervical baja y la columna lumbar también fue hallada en pacientes con PR y podría ser en parte responsable del dolor del cuello y la espalda que reportan los pacientes que sufren este trastorno. No obstante, si bien la presencia de bursitis en estas áreas es consistente con la pero no es específica.
Las citocinas proinflamatorias también podrían ser importantes en la PR. En pacientes con síntomas en los músculos vasto lateral y trapecio se comprobó el aumento de las concentraciones intersticiales de las interleucinas IL-1α e IL-β, el antagonista del receptor de la IL-1, la IL-6, la IL-8, el factor de necrosis tumoral α y la proteína 1 quimioatrayente de los monocitos, en comparación con los controles. Por lo tanto, la mayor concentración intersticial de citocinas proinflamatorias en los músculos sintomáticos puede ser importante en la patogénesis de la enfermedad.
Los linfocitos T-helper-1 y T-helper-17 (Th17) también intervienen en la patogénesis de la PR y la arteritis de células gigantes. Aunque la actividad supresora de las células T reguladoras circulantes no se altera, en ambas condiciones se observa una disminución del número de células T reguladoras y un cambio notable en la relación de las células Th17 con las células T reguladoras (hacia una respuesta aumentada de las células Th17).
En los pacientes recientemente diagnosticados con PR o arteritis de células gigantes existe una correlación inversa entre el número de células B y la VSG, la concentración de proteína C reactiva y el factor de activación de las células B sérico. Los pacientes recién diagnosticados con arteritis de células gigantes o PR tienen disminuido el número de células B circulantes en comparación con los controles sanos pero el número de células B se recupera después del tratamiento.
► Manifestaciones clínicas
| La principal característica clínica de la PR es el dolor de la cintura escapular con impotencia funcional y rigidez en pacientes >50 años. Los pacientes suelen quejarse de dolor y rigidez en la parte superior de los brazos, el cuello, la cintura pelviana, las caderas y los muslos. A menudo, estas manifestaciones clínicas son bilaterales. |
Con frecuencia, el inicio de los síntomas es rápido, generalmente en unos pocos días y en algunos casos aparecen en forma aguda, de la noche a la mañana. Los síntomas se asocian con dolor y rigidez matinal en la región musculoesquelética afectada. La presentación típica es el dolor inflamatorio y la rigidez.
Las manifestaciones constitucionales como la fiebre de bajo grado, la fatiga, la astenia, la anorexia y la pérdida de peso ocurren hasta en el 40-50% de los pacientes
Es característico que estos síntomas empeoren por la mañana y mejoren progresivamente durante el día. También empeoran después del descanso o cuando el paciente está inactivo durante un tiempo prolongado. En la PR, la rigidez matinal es típica, dura al menos 30 minutos y, por lo general dura más de 45-60 min.
Las actividades de la vida diaria como vestirse, peinarse, levantarse de la cama o de una silla, se tornan difíciles y se asocian a dolor intenso. El dolor nocturno también es típico y con frecuencia los pacientes tienen dificultades para conciliar el sueño. El dolor en el hombro está casi invariablemente presente, mientras que la afectación del cuello y la cintura pelviana aparece en el 50%-90% de casos. En algunos pacientes, al comienzo de la enfermedad los síntomas pueden ser unilaterales pero pronto se tornan bilaterales.
Las manifestaciones constitucionales como la fiebre de bajo grado, la fatiga, la astenia, la anorexia y la pérdida de peso ocurren hasta en el 40-50% de los pacientes. Un síntoma de presentación de la PR aislada podría ser la fiebre (≥38°C). La fiebre elevada persistente es más común en los pacientes con PR asociada a la arteritis de células gigantes que en aquellos con PR aislada.
En el examen físico, el movimiento activo de los hombros está restringido debido al dolor, sin signos clínicos de tumefacción articular. El rango del movimiento pasivo asistido por el examinador a veces puede ser casi normal.
El dolor en el hombro es difuso y no está localizado en estructuras específicas del hombro. La restricción dolorosa de los movimientos del cuello y las caderas también están presentes en algunos casos. También podría haber sensibilidad muscular pero no se acompaña de debilidad muscular a pesar de la mialgia.
También se pueden observar manifestaciones articulares. Los síntomas de sinovitis periférica aparecen en un porcentaje variable (23-39% de los pacientes). La artritis suele ser asimétrica y no se asocia con erosiones corticales óseas siendo las articulaciones más afectadas la rodilla y la muñeca. Una vez hecho el tratamiento con glucocorticoides, la mayoría de los pacientes experimenta la resolución de las manifestaciones articulares.
La sinovitis periférica también podría incluir la inflamación de los tejidos periarticulares (tendinitis, bursitis), especialmente en los brazos y las manos, y puede confirmarse por ecografía y otras técnicas de imagen. La ecografía ha permitido detectar el síndrome del túnel carpiano en el 14% de los pacientes con PR y la tenosinovitis distal en el 3%.En un estudio de 1998, la ecografía realizada a 117 pacientes detectó artritis periférica asimétrica en el 25% de los participantes, predominantemente en las rodillas y las muñecas.
En algunos casos, la PR podría presentarse con hinchazón distal y edema, un cuadro que puede simular la sinovitis seronegativa simétrica remitente con síndrome de edema con fóvea. El síndrome se caracteriza por sinovitis y sinovitis del tendón extensor de las manos y los pies. Los pacientes con esta condición tienen hinchazón de la extremidad distal con edema con fóvea, mayormente sobre el dorso de las manos y las muñecas, y menos comúnmente sobre los tobillos y los pies. En el 12% de los pacientes este cuadro se ha descrito como una complicación de la PR. Similar a la artritis inflamatoria en los pacientes con PR, estos síntomas se resuelven rápidamente después del tratamiento con glucocorticoides.
► Anomalías del laboratorio
La proteína C reactiva podría ser más específica y más sensible que la eritrosedimentación
El aumento de los reactantes de fase aguda es una característica típica en los pacientes con PR. Algunos consideran que una VSG ≥40 mm/hora es un criterio de clasificación. Como criterios de clasificación, otros autores recomiendan una VSG >30 mm/hora o una concentración de proteína C reactiva >6 mg/l. En 2012, la European League Against Rheumatism (EULAR) y el American College of Rheumatology (ACR) publicaron criterios de clasificación provisorios.
También se incluyeron la VSG o las concentraciones a de proteína C reactiva anormales. Hasta el 20% de los pacientes con PR tienen una VSG inicial <40 mm/hora. El porcentaje de pacientes con una VSG baja oscila entre el 7% y el 20%. Los pacientes con PR y VSG baja tienen características clínicas y una evolución de la enfermedad similares a las de los pacientes con VSG elevada. Sin embargo, las personas con VSG baja son generalmente más jóvenes y tienen menor frecuencia de fiebre, pérdida de peso y anemia que aquellos con VSG ≥40 mm/hora.
Para detectar la inflamación y evaluar la actividad de la enfermedad, la proteína C reactiva podría ser más específica y más sensible que la VSG. No está claro cuál de las dos mediciones es más útil para el diagnóstico inicial de PR. La producción de proteína C reactiva está principalmente inducida por la IL-6. Antes de comenzar el tratamiento de los pacientes con PR, las concentraciones de esta citocina están típicamente elevadas lo que también ocurre con las concentraciones séricas del factor de activación de las células B. Ambos biomarcadores séricos tienen una estrecha asociación con la actividad de la enfermedad, pero no hay evidencia disponible de que sean más útiles que la proteína C reactiva para basar las decisiones clínicas.
En los pacientes con concentraciones de proteína C reactiva y VSG normales habría que considerar otros diagnósticos alternativos. Los anticuerpos IgG contra el péptido de ferritina están presentes en la mayoría de los pacientes con arteritis de células gigantes activa y PR pero su utilidad en la práctica clínica no está bien establecida.
En los pacientes con enfermedad activa se pueden hallar otras anomalías bioquímicas asociadas a la respuesta inflamatoria, como las concentraciones elevadas de la globulina α2, la anemia normocítica normocrómica, la trombocitosis y la hipoalbuminemia, pero no son específicas de la PR.
En general, los autoanticuerpos más específicos para la artritis reumatoidea o las enfermedades del tejido conectivo, como los anticuerpos peptídicos anticitrulina, el factor reumatoideo, los anticuerpos antinucleares y los anticuerpos anticitoplasma de los neutrófilos no están presentes en los pacientes con PR. Sin embargo, las personas mayores pueden tener títulos bajos del factor reumatoideo, pero no son significativos para el diagnóstico.
► Polimialgia reumática y arteritis de células gigantes
| La arteritis de células gigantes es una vasculitis de los grandes vasos sanguíneos que ocurre en personas mayores. Esta condición es infrecuente en las personas <50 años; el pico de incidencia aparece entre los 70 y los 79 años. Como la PR, la arteritis de células gigantes tiene una estrecha asociación genética con la región HLA y tiene gran prevalencia en los países escandinavos y en individuos de ascendencia escandinava. |
La arteritis de células gigantes y la PR suelen ser condiciones concurrentes y superpuestas. Por lo tanto, en todos los pacientes con PR se deben evaluar cuidadosamente los síntomas y signos con el fin de detectar la arteritis de células gigantes, incluyendo la palpación de las arterias temporal, radial y pedia. La PR podría ser la manifestación de la arteritis de células gigantes. En una serie de pacientes con arteritis de células gigantes en quienes el diagnóstico fue confirmado mediante la biopsia de la arteria temporal, el 40-50% tenían manifestaciones de PR.
La frecuencia de la arteritis de células silente confirmada mediante la biopsia de la arteria temporal en pacientes con PR aislada es variable. La arteritis de células gigantes se diagnostica casi en el 20% de los pacientes con PR pura, y la mayoría de los estudios estima que la incidencia es del 10-30%. Clínicamente, los pacientes con PR aislada tienen recuento de plaquetas y VSG más bajos y concentraciones más elevadas de hemoglobina que las personas con PR asociada a la arteritis de células gigantes confirmada con la biopsia. La expresión de la enfermedad podría explicarse en parte por diferencias en el perfil genético y la expresión genética.
Una gran preocupación en los pacientes que inicialmente se presentan con PR aislada es el riesgo de que la arteritis de células gigantes concomitante desarrolle complicaciones isquémicas graves. Por lo tanto, es importante hacer un cuidadoso seguimiento de los pacientes con diagnóstico de PR pura aislada para identificar los síntomas de isquemia.
Es necesario investigar si las técnicas de imagen están indicadas para estudiar a todos los pacientes con PR, con el fin de evaluar la arteritis de células gigantes de las arterias craneanas y los grandes vasos. Sin embargo, la investigación se ve limitada por la experiencia local y la disponibilidad de las modalidades de imagen relevantes, así como la incertidumbre sobre el significado clínico de los resultados.
La ecografía de las arterias temporal y axilar podría revelar signos de arteritis de células gigantes oculta. Un estudio más avanzado, la tomografía por emisión de positrones (PET) con F18-fluordesooxiglucosa 18 (F¹⁸-FDG) ha revelado que un tercio de los pacientes con PR sin síntomas o signos de arteritis de células gigantes podría tener oculto el compromiso de un vaso de gran tamaño. Para detectar la aortitis en los pacientes con PR se debe recurrir a imágenes avanzadas (PET, TC o RM), si es que presentan síntomas atípicos como dolor lumbar o dolor que afecta principalmente las piernas asociado con un aumento de los reactantes en fase aguda.
► Cuadros que mimetizan a la polimialgia reumática
Los síntomas de PR no son específicos y aparecen en muchas enfermedades que la imitan, entre ellas la artritis reumatoidea, la artrosis del hombro, la enfermedad por depósito poliarticular de pirofosfato de calcio, la enfermedad del manguito rotador y la capsulitis adhesiva (hombro congelado).
► Criterios para los estudios diagnósticos y la clasificación
Se han propuesto varios conjuntos de criterios para la clasificación y el diagnóstico de la PR. Los criterios tienen características comunes, como la edad avanzada (≥50 años), la afectación típica de los hombros y la elevación de los reactantes de fase aguda. La edad avanzada (>50 años) fue propuesta como criterio por Chuang y col., por Healey y por EULAR/ACR de 2012.
En los diferentes conjuntos de criterios se ha incluido el compromiso clínico bilateral predominantemente a los hombros con rigidez matinal de al menos 45-60 minutos de duración. Para el diagnóstico y la clasificación de la PR también se requiere el aumento de la VSG, generalmente >40 mm/hora o el aumento de la concentración de proteína C reactiva.
Comentarios
Para ver los comentarios de sus colegas o para expresar su opinión debe ingresar con su cuenta de IntraMed.