Innovación en el manejo del dolor

Introducción
El dolor es un síntoma prevalente en 30% de los pacientes con cáncer al ser diagnosticados, y en más de 70% de aquéllos con enfermedad metastásica avanzada.
El tratamiento del dolor oncológico sigue basándose en el uso secuencial de fármacos, de acuerdo a la escalera analgésica de la Organización Mundial de la Salud (OMS), obteniendo alivio hasta en 90% de los pacientes.
El uso de buprenorfina se remonta al menos 30 años en el tratamiento del dolor relacionado con cáncer; no obstante, su popularidad se ha limitado por los efectos colaterales de las formulaciones parenterales y sublinguales de liberación inmediata que originalmente implicaba su uso.
Actualmente, se reconoce que la vía parenteral es una alternativa a la vía oral en el tratamiento del dolor oncológico.1 La formulación sublingual de buprenorfina produce concentraciones plasmáticas muy variables, con efectos máximos y mínimos que inducen acontecimientos adversos prevalentes, sobre todo en el anciano.2
La buprenorfina se ha identificado durante años como un opioide con efecto agonista parcial con efecto techo que limitaba su uso clínico, suposición basada solamente en estudios en animales. En la clínica humana nunca se ha demostrado un efecto techo respecto de la analgesia y ha actuado como un agonista μ puro.3,4 Además, ha mostrado una eficacia plena y potentes acciones antinociceptivas, antihiperalgésicas y antialodínicas sin efecto techo.5
La buprenorfina se une al receptor opioide μ y se caracteriza por una disociación lenta, lo que en teoría podría impedir la eficacia completa del opioide añadido; sin embargo, en el intervalo posológico analgésico produce un efecto de magnitud compatible con un tipo de interacción aditiva.6
El desarrollo reciente de un sistema de liberación transdérmico de buprenorfina ha brindado una nueva oportunidad de aprovechar este medicamento en el tratamiento de dolor crónico moderado a severo, oncológico y no oncológico.
Farmacología
La buprenorfina es un opioide semisintético derivado de la tebaína, y tiene una potencia al menos 30 veces mayor que la morfina. Su estructura es básicamente la de un opioide, pero en la posición C-7 contiene un grupo t-butilo. Este grupo ocupa su posición en el espacio cercano al grupo fenilo, lo que contribuye a que sea lipofílico.7
Las propiedades físico-químicas de la buprenorfina (notable solubilidad en agua y en lípidos, peso molecular y configuración estructural) favorecen su penetración en los tejidos, tanto en formulaciones transdérmicas como transmucosas. Sin embargo, la facilidad con la cual penetra en los tejidos contribuye aparentemente, en ocasiones, a la presentación de eventos adversos mediados centralmente, como la emesis.8,9
La presentación transdérmica permite la administración directa a través de la piel sana, con varias ventajas frente a las alternativas convencionales, con lo que se respalda directamente la recomendación de la OMS (1996) de contar con un método terapéutico de elección para el tratamiento del dolor crónico oncológico, con base en tres objetivos principales:10,11,12
1. Duración de acción prolongada
2. Fluctuaciones mínimas de las concentraciones plasmáticas del analgésico, que garanticen un alivio homogéneo del dolor y a largo plazo
3. Prevención de concentraciones plasmáticas excesivamente altas para reducir al mínimo posible el problema de los efectos adversos.
El uso de la piel como puerta de entrada para la administración sistémica del fármaco ofrece varios beneficios, tales como:
• Evitar el metabolismo hepático de primer paso y la incompatibilidad gastrointestinal.
• Control de la liberación del medicamento durante un tiempo más prolongado que al utilizar las formulaciones orales habituales.
• Mantenimiento de niveles plasmáticos constantes de la sustancia, eliminando los acontecimientos adversos al evitar los picos máximos iniciales tras la utilización de la vía intravenosa. Por otra parte, disminuye la necesidad de administraciones repetidas de rescate.
• Mayor comodidad para el paciente y un mejor cumplimiento de la terapia.
• Evita las molestias surgidas de la inyección intramuscular repetida, además del ahorro de costos (en equipos y trabajo) que conlleva mantener infusiones intravenosas.1
La buprenorfina se ha seleccionado para administrarse de forma transdérmica debido a su elevada lipofilia, a su bajo peso molecular4,6,7 y a la dosis diaria de 0.8 mg a 2 mg necesaria para la analgesia. La elevada afinidad y la baja disociación de la buprenorfina con los receptores opioides dan lugar a una duración de acción prolongada, haciéndola idónea para una formulación de liberación prolongada.
Anteriormente existían parches transdérmicos que consistían en un reservorio líquido de fármaco y una membrana de liberación controlada, en donde un daño accidental de la membrana provocaría el vertido total del contenido y la posibilidad de sobredosis, es decir, concentraciones plasmáticas elevadas y tóxicas.
En la actualidad se cuenta con un diseño básico matricial que, a diferencia del reservorio controlado con membrana, es de tecnología avanzada, desarrollado paragarantizar un control más seguro y preciso de la administración del fármaco. En este caso, la sustancia está incorporada en una matriz de polímero, lo que permite su disposición continua y elimina el riesgo de una liberación brusca o el abuso potencial en caso de daño al parche, lo que permite su fraccionamiento y la dosificación individual (Figura 1).
Figura 1
Parche transdérmico: estructura de sistema de administración
de reservorio y de sistema matricial
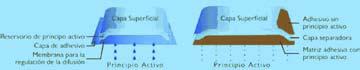
Budd K. Buprenorphine and the transdermal system.
The Ideal match in pain management. Int J Clinic Prac 2003; S 133: 9-14
Eficacia analgésica
La buprenorfina es un opioide agonista parcial, del cual se puede esperar –en teoría– un efecto techo relacionado tanto con el resultado deseado (analgesia) como con los efectos secundarios (depresión respiratoria).13
Se han realizado estudios experimentales en modelos nociceptivos, inflamatorios y neuropáticos en roedores,14 que han demostrado una muy alta potencia de la buprenorfina, entre unas 30 y 50 veces mayor que la de la morfina, con una eficacia del 100% respecto al efecto máximo posible, como con los agonistas μ puros. Esto muestra que en el intervalo posológico analgésico, la buprenorfina se comporta esencialmente como un agonista puro en lo que se refiere a eficacia analgésica, con independencia del tipo e intensidad del estímulo doloroso.
En el ser humano, la buprenorfina no muestra ningún efecto techo relevante para la inhibición del dolor en el intervalo posológico analgésico,15 lo cual también se confirma con los datos clínicos en seres humanos: por ejemplo, en un estudio en el que se utilizaron dosis altas de hasta 7 mg (esto es hasta nueve parches de 35 μg/h, y en un estudio a largo plazo en el que se usaron hasta 5.4 mg).1
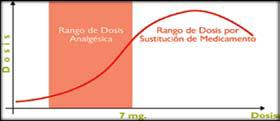
En la gráfica de la curva dosis-respuesta de buprenorfina se demuestra claramente que actúa como un agonista puro μ en el rango de dosis analgésica hasta un rango superior a los 7 mg. La curva dosis-respuesta incrementa constantemente hasta un máximo de efecto semejante a agonistas μ puros (Figura 2).
Figura 2
Curva dosis-respuesta de la buprenorfina transdérmica:
Rango de dosis analgésica menos a 7 mg al día, sin alcanzar
dosis techo
Budd K. Buprenorphine and the transdermal system. The Ideal match in
pain management. Int J Clinic Prac 2003; S 133: 9-14
Esta misma gráfica permite considerar el aumento en la depresión respiratoria, que con el efecto techo (curva dosis-respuesta en forma de campana) no se incrementa la presencia de dicha circunstancia, lo que otorga una clara ventaja de seguridad para los pacientes.
Combinación de agonistas parciales con agonistas μ puros
Debido a la alta afinidad por el receptor opioide μ y a la potencia analgésica de la buprenorfina, el efecto analgésico se consigue incluso cuando están ocupados pocos receptores μ. En el intervalo de dosis terapéuticas, los receptores libres restantes son suficientes para poder añadir un agonista μ puro, como morfina o tramadol, sin riesgo de competencia por los receptores.
Lo anterior confirma que la buprenorfina se comporta como agonista opioide μ cuando se utiliza dentro del rango analgésico de dosis, no obstante la elevada afinidad y la disociación lenta del receptor, tanto en el efecto analgésico como en los efectos secundarios de tipo opioide.
La buprenorfina puede revertirse con antagonistas de los receptores opioides. En el caso de la naloxona, al tener vida media corta, es necesaria la aplicación de una dosis mayor, dado que el efecto de la dosis estándar utilizada es más corto que el de la buprenorfina. Asimismo, en estudios clínicos se ha demostrado la posibilidad de antagonizar los efectos secundarios de la buprenorfina con la administración de un bolo o una infusión de naloxona que consiga concentraciones plasmáticas constantes y suficientes.16
Desarrollo de tolerancia y uso a largo plazo
Una de las causas posibles del desarrollo de tolerancia en el uso de opioides es la internalización del receptor, la cual implica una disminución del número de receptores μ en la superficie sináptica (fenómeno que exige ir aumentando la dosis de analgésico para mantener un efecto estable).
En estudios experimentales se demostró que la internalización del receptor se desencadena por la presencia de agonistas μ puros, como la morfina o el fentanilo. La buprenorfina no reduce el número de receptores μ de la superficie celular; al contrario, aumenta incluso ligeramente el número de receptores,17 lo que podría explicar que la probabilidad de desarrollo de tolerancia durante el tratamiento con buprenorfina sea comparativamente baja.18
Comentarios
Para ver los comentarios de sus colegas o para expresar su opinión debe ingresar con su cuenta de IntraMed.






